Вакцинация АДС-М-Биолек в Запорожье | Клиника Святого Николая
(098) 309 03 03
(099) 309 03 03
ул. Св. Николая, 53а ул. Добролюбова, 19 ул. Днепровская, 24
г. Запорожье. Работаем ежедневно с 8:00.
(093) 309 03 03
Написать в Viber
Онлайн-декларация
Эффективная вакцина для ревакцинации от дифтерии и столбняка «АДС-М-Биолек» в Клинике Святого Николая
Столбняк и дифтерия – это опасные заболевания, унесшие в годы пандемии не одну тысячу жизней. На сегодняшний день благодаря вакцинации и созданию коллективного иммунитета эти болезни встречаются все реже. Но чтобы их окончательно победить, очень важно регулярно вакцинироваться. Своевременная прививка АДС-М от «Биолек» помогает избежать заражения или смягчить течение болезни и тяжесть осложнений в случае инфицирования.
АДС-М-Биолек: состав вакцины
АДС-М – вакцина, которая используется для ревакцинации от дифтерии и столбняка.
Действующие компоненты: дифтерийный и столбнячный анатоксины по 5 единиц в 1 дозе (0,5мл). Другие вспомогательные вещества: алюминия гидроксид, тиомерсал в качестве консерванта и др.
Иммунизация от столбняка и дифтерии рекомендована в случае:
- Плановой ревакцинации взрослых по возрасту согласно календарю прививок
- Прививания взрослых, которые не были вакцинированы или не имеют доказательств этого (вводят вакцину АДС-М троекратно)
Записаться на вакцинацию
Противопоказания к вакцинации АДС-М-Биолек
Запрещено делать прививку АДС-М «Биолек» при таких состояниях:
- Обострение хронических болезней или декомпенсированная хроническая патология
- Эндокринные болезни в стадии декомпенсации (сахарный диабет, гипо-, гипертиреоз)
- Индивидуальная непереносимость вакцины, одного или нескольких ее компонентов
- Аллергическая реакция на предыдущее введение препарата
- Период проведения химиотерапии, лучевой терапии, лечения цитостатиками, гормональными средствами
- Любая острая патология независимо от причины
- Злокачественные новообразования
- Тяжелые болезни нервной системы (эпилепсия, гидроцефалия)
- Тяжелые иммунодефицитные состояния
- Беременность и лактация
- За 1 месяц до планируемой беременности
Некоторые противопоказания являются временными. После их исчезновения можно проводить иммунизацию, проконсультировавшись с врачом.
После их исчезновения можно проводить иммунизацию, проконсультировавшись с врачом.
Календарь вакцинации
Препарат АДС-М Биолек может использоваться для плановой прививки от дифтерии и столбняка каждые 10 лет с момента последней иммунизации. Концентрация антител в крови со временем падает и защитные силы организма по отношению к данным болезням слабеют. Поэтому необходима регулярная ревакцинация для поддержания активности иммунитета и эффективной защиты от дифтерии и столбняка.
Также АДС-М анатоксин «Биолек» применяют для вакцинации не вакцинированных ранее взрослых. Процедура проводится в 3 этапа: с интервалом в 1 месяц и ревакцинация через 6-9 месяцев.
График иммунизации составляется доктором Клиники Святого Николая для каждого пациента индивидуально с учетом его особенностей. Таким образом получается достичь максимальной эффективности от прививки и обеспечить надежный иммунитет.
Возможные побочные эффекты
Прививка АДС-М «Биолек» имеет гораздо меньше побочных явлений в сравнении с вакциной АКДС. Из нежелательных реакций встречаются:
Из нежелательных реакций встречаются:
- В месте инъекции – покраснение, припухлость, уплотнение, незначительные болевые ощущения
- Аллергические реакции в виде крапивницы, зуда, анафилаксии, ангионевротического отека
- Незначительная слабость, недомогание, усталость
- Кратковременное повышение температуры
Некоторые из них совершенно безобидны и не требуют медицинской помощи. А некоторые более серьезные — при возникновении отека, крапивницы, парестезий, невралгии или других тяжелых последствий нужно обязательно обратиться за консультацией к врачу.
Записаться на вакцинацию
Преимущества проведения вакцинации АДС-М-Биолек в Клинике Святого Николая
- Проверенные сертифицированные вакцины высокого качества с минимальным количеством возможных побочных эффектов
- Тщательный контроль и соблюдение всех правил хранения, транспортировки вакцин, регулярная проверка сроков годности иммунных препаратов
- Удобная запись на вакцинацию – в онлайн режиме или по телефону на подходящее время и дату
- Полное информационное сопровождение – каждый клиент имеет право узнать у медперсонала о вакцине, ее особенностях, правилах хранения, введения
- Инъекции выполняет опытная специально обученная медсестра
Удобства для посетителей Клиники Святого Николая
Собственная парковка
Оплата картой
Онлайн-запись
Аптека в здании
Собственная лаборатория
Электронная медкарта
Дифтерия.
 Существующие вакцины. Вакцины и схемы введения. Специалисты о прививкахДифтерия. Существующие вакцины. Вакцины и схемы введения. Специалисты о прививках
Существующие вакцины. Вакцины и схемы введения. Специалисты о прививкахДифтерия. Существующие вакцины. Вакцины и схемы введения. Специалисты о прививках- Библиотека
- На связи с экспертом
- Новости
Войти
Вопрос-ответ
Вакцины и схемы введения Существующие вакцины
Эффективность современных вакцин составляет 95-100%. Полный курс вакцинации создает стойкий иммунитет на протяжении 7-10 лет.
Профилактические прививки позволяют создать длительный и напряжённый антитоксический иммунитет от дифтерии.
Существующие
вакцины
В России используются следующие вакцины:
- АД-м — в комбинации со столбнячным анатоксином (АДС, АДС-м, Россия) и коклюшной вакциной (АКДС, «Бубо-Кок», «Бубо-М», Россия)
- АКДС-ГепВ — Вакцина против коклюша, дифтерии, столбняка и гепатита В адсорбированная (Россия)
- аАКДС-ГепВ+Hib — Вакцина против дифтерии, столбняка, гепатита В, коклюша бесклеточная адсорбированная, инфекции, вызываемой Haemophilusinfluenzae тип b, конъюгированная синтетическая (Россия)
бесклеточные или ацеллюлярные:
- Инфанрикс — вакцина для профилактики дифтерии,столбняка,коклюша (бесклеточная) трехкомпонентная адсорбированная жидкая (Бельгия)
- Инфанрикс Пента — вакцина дифтерийная, столбнячная, коклюшная (бесклеточная, компонентная), рекомбинантная против гепатита b, инактивированная полиомиелитная, против гемофильной палочки типа b конъюгированная (адсорбированная)(Бельгия)
- Инфанрикс Гекса — вакцина для профилактики дифтерии, столбняка, коклюша (бесклеточная), полиомиелита (инактивированная), гепатита В комбинированная, адсорбированная (Бельгия)
- Пентаксим — вакцина для профилактики дифтерии и столбняка адсорбированная, коклюша ацеллюлярная, полиомиелита инактивированная и инфекций, вызываемых Haemophilusinfluenzae тип b, конъюгированная (Франция)
- Тетраксим — вакцина для профилактики дифтерии и столбняка адсорбированная, коклюша ацеллюлярная, полиомиелита инактивированная (Франция)
- Адасель — вакцина для профилактики дифтерии (с уменьшенным содержанием антигена), столбняка и коклюша (бесклеточная), комбинированная, адсорбированная (Канада).

Некоторые вакцины имеют возрастные ограничения: АКДС применяется до 3 лет 11 месяцев, 29 дней, АДС — до 6 лет 11 месяцев, 29 дней, аАКДС-ГепВ+Hib — с 6 месяцев не привитых ранее и т.д.
Выбор вакцины для проведения иммунизации определяет врач в зависимости от наличия противопоказаний, возраста пациента и нарушения сроков вакцинации рекомендованных календарем прививок.
Схема
вакцинации
- 1-я вакцинация — в 3 мес.
- 2-я вакцинация — в 4,5 мес.
- 3-я вакцинация — в 6 мес.
- 1-я ревакцинация — в 18 мес.
- 2-я ревакцинация — в 7 лет
- 3-я ревакцинация — в 14 лет
Последующие ревакцинации — каждые 10 лет.
Применение препарата АКДС совместимо с другими вакцинами, ее можно вводить одновременно со всеми препаратами из Национального календаря в один день, в разные участки тела, за исключением вакцины БЦЖ.
Противопоказания
Временные
- острые заболевания или обострение хронической патологии спустя 2-4 недели после снижения температуры и/или окончания обострения
- при легких формах заболеваний прививки допускаются после исчезновения клинических симптомов
- иммунизация лиц с аллергическими заболеваниями проводится на фоне базисной терапии
Постоянные:
- повышенная чувствительность к любому компоненту вакцины
- прогрессирующие заболевания нервной системы
- афебрильные судороги в анамнезе (на коклюшный компонент)
- развитие на предшествующее введение комбинированных вакцин сильной реакции (повышение температуры выше 40 С, в месте введения вакцины — отек и гиперемия свыше 8 см в диаметре)
Детей, родившихся с весом менее 2 кг, прививают при нормальном физическом и психомоторном развитии; отставание в весе не является основанием к отсрочке вакцинации. Стабильные проявления аллергического заболевания (локализованные кожные проявления, скрытый бронхоспазм и т.д.) не являются противопоказаниями к вакцинации, которая может быть проведена на фоне соответствующей терапии.
Стабильные проявления аллергического заболевания (локализованные кожные проявления, скрытый бронхоспазм и т.д.) не являются противопоказаниями к вакцинации, которая может быть проведена на фоне соответствующей терапии.
Полезно знать
Ответы на сложные вопросы
Возможные реакции
В месте инъекции:
болезненность
отечность
покраснение
Общие:
повышение температуры
слабость, вялость
рвота, понос
нарушение аппетита
Возможные поствакцинальные осложнения:
редко
судороги
обычно связанные с повышением температуры
аллергические реакции
крапивница, полиморфная сыпь, отек Квинке
Реестр Консультативного комитета по вакцинам и родственным биологическим продуктам
Подача заявки на членство в Консультативных комитетах FDA
В рамках постоянных усилий Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) по набору квалифицированных экспертов с минимальным конфликтом интересов, заинтересованных в работая в консультативных комитетах FDA, FDA запрашивает кандидатуры членов для работы в своих консультативных комитетах.
Текущее количество вакансий: 0
Обратите внимание, что одна или несколько вакансий могут находиться в процессе выдвижения кандидатур или же может быть произведено окончательное назначение.
Кафедра
Хана Эль Сахли, доктор медицинских наук
Специализация: вакцины, инфекционные заболевания
Срок: 01.02.2022-31.01.2026
Профессор
Кафедра молекулярной вирусологии и микробиологии болезней 6 Секция 1 инфекционной медицины
0 Кафедра инфекционной медицины
0
Медицинский колледж Бейлора
Хьюстон, Техас 77030
Хейли Альтман-Ганс, доктор медицины
Специализация: педиатрия, инфекционные заболевания
Срок: 21.06.2019-31.01.2023
Профессор педиатрии
Кафедра педиатрии
Медицинский центр Стэнфордского университета
Stanford, CA 94305
2 9004ato, Paula *
Квалификация: Представитель отрасли
Срок: 01.02.2020-31.
 01.2024
01.2024 Вице-президент и руководитель терапевтического направления
Клинические исследования вакцин
Merck
North Wales, PA 19454
Adam C. Berger, Ph.D .
Срок: 01.02.2022-31.01.2026
Квалификация: глобальное здравоохранение/генетика
Директор отдела клинических и медицинских исследований
Управление научной политики
Офис директора
Национальные институты здравоохранения
Bethesda, MD 20892
Henry H. Bernstein, DO, MHCM, FAAP
Специализация: педиатрия
Срок: 01.02.2022-31.01.2026
Профессор педиатрии
Well Well, 6HorthStrah, Медицинская школа им. педиатрии
Детский медицинский центр Коэна
New Hyde Park, NY 11042
Archana Chatterjee, MD, Ph.D.
Специализация: педиатрия, инфекционные заболевания
Срок: 21.06.2019–31.01.2023
Декан Чикагской медицинской школы
Вице-президент по медицинским вопросам
Университет медицины и науки Розалинды Франклин
Северный Чикаго, Иллинойс 60064
75
CAPT Аманда Кон, доктор медицины
Специализация: педиатрия, вакцины
Срок: 01.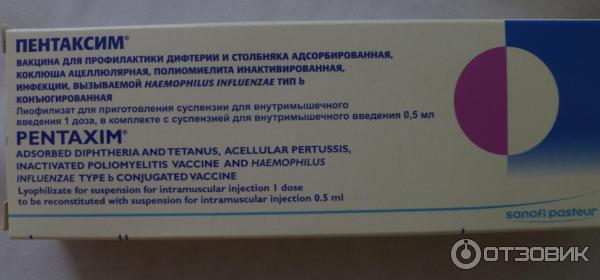 02.2020-31.01.2024
02.2020-31.01.2024
Главный врач
Национальный центр иммунизации и респираторных заболеваний
Центры по контролю и профилактике заболеваний
Atlanta, GA 30333
Холли Джейнс, доктор философии.
Специализация: биостатистика
Срок: 01.06.2019-31.01.2023
Ассоциированный член
Центр онкологических исследований Фреда Хатчинсона
Отдел вакцин и инфекционных заболеваний
Отдел наук общественного здравоохранения
Сиэтл, Вашингтон 98109
5 7 Дэвид Ким, М.Д., М.С., М.Х.А.
Специализация: педиатрия, вакцины
Срок: 01.02.2022-31.01.2025
CAPT, Служба общественного здравоохранения США
Директор отдела вакцин
Управление по инфекционным заболеваниям и политике в отношении ВИЧ/СПИДа Health
Министерство здравоохранения США и
Human Services
Washington, DC 20024
Arnold Monto, MD
Специализация: эпидемиология
Срок: 01.02. 2022-31.01.2026 Public Professor Franciser J Collegiate
2022-31.01.2026 Public Professor Franciser J Collegiate
Здоровье
Профессор эпидемиологии
Мичиганский университет
Анн-Арбор, Мичиган 48109
Пол Оффит, доктор медицинских наук
Специализация: инфекционные заболевания
Срок: 01.02.2022-01.01.2022 Профессор педиатрии 6 инфекционных отделений 9016 9025 Болезни
Abramson Research Building
The Children’s Hospital of Philadelphia
Philadelphia, PA 19104
Steven Pergam, M.D.0016 Медицинский директор
Профилактика инфекций
Seattle Cancer Care Alliance
Seattle, WA 98109
Stanley Perlman, M.D., Ph.D.
Специализация: Детские инфекционные болезни
Срок: 23.08.2022-31.01.2026
Профессор кафедры микробиологии и иммунологии
Профессор педиатрии
Марк Стински Кафедра вирусологии
University of Iowa
Iowa City, IA
Джей Портной, доктор медицины
Экспертиза: Представитель по защите прав потребителей
Срок: 01. 02.2022-31.01.2025
02.2022-31.01.2025
Профессор педиатрии
Медицинский директор телемедицины
Отделение аллергии, астмы и иммунологии
Детская больница милосердия
Канзас-Сити, Миссури 64108
Специализация: Иммунология и инфекционные заболевания
Срок: 01.02.2022-31.01.2026
Главный редактор
Медицинский журнал Новой Англии
Адъюнкт-профессор
Кафедра иммунологии и Гарвардская школа общественного здравоохранения им. Т.Х. Чана
Младший врач
Brigham and Women’s Hospital
Boston, MA 02115
Andrea Shane, MD, MPH, M.Sc.
Специализация: детские и инфекционные заболевания
Срок: 01.02.2022–31.01.2026
Профессор педиатрии
Медицинский факультет Университета Эмори
Atlanta, GA 30322
Gregg Sylvester +
Квалификация: заместитель представителя отрасли
Срок полномочий: 01.02.2020-31. 01.2024
01.2024
Вице-президент
Медицинские вопросы
Seqirus Inc.
Summit, NJ 07901
**Представитель по работе с потребителями
***Представитель отрасли
+ заместитель представителя отрасли
НАЗНАЧЕННЫЙ ФЕДЕРАЛЬНЫЙ ДОЛЖНОСТНЫЙ ЛИЦ
Sussan Paydar, Ph.D.
Отдел научных советников и консультантов
Центр оценки и исследований биологических препаратов
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов
Silver Spring, MD 20993
Эл.0004
Lashawn Marks
Отдел научных консультантов и консультантов
Центр оценки и исследований биологии
Управление по контролю за продуктами и лекарствами
Silver Spring, MD 20993
E-mail: [email protected]
9003 Директор
6666666666666666666666666666666666666666666666666666666666666666666666666666666666666666666666669н. Атрейя, доктор философии.
Отдел научных советников и консультантов
Центр оценки и исследований биологических препаратов
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов
Silver Spring, MD 20993
Электронная почта: VRBPAC@fda.
 hhs.gov
hhs.gov
О вакцинации против дифтерии, столбняка и коклюша
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) лицензировало 12 вакцин для использования в США для защиты от дифтерии и столбняка. Девять из этих вакцин также помогают защитить от коклюша. Некоторые вакцины обеспечивают защиту и от других заболеваний, включая Haemophilus influenzae типа b, гепатит B и полиомиелит. Узнайте о составе, типах, иммуногенности и эффективности этих вакцин, а также ознакомьтесь с вкладышами в упаковке ниже.
Типы и состав вакцин против дифтерии, столбняка и коклюша
Только вакцины против дифтерии и столбняка (DT и Td)
В Соединенных Штатах Америки используется одна общая педиатрическая вакцина DT .
Каждая доза 0,5 миллилитра (мл) DT (Sanofi Pasteur) содержит 6,7 предела флокуляции (Lf) анатоксина дифтерии, 5 Lf анатоксина столбняка и не более 0,17 миллиграмма (мг) алюминия. Остаточное содержание формальдегида по данным анализа составляет менее 0,02%. Вакцина содержит следовые количества тимеросала (не в качестве консерванта) из производственного процесса [≤0,3 микрограмма (мкг) ртути/доза].
Остаточное содержание формальдегида по данным анализа составляет менее 0,02%. Вакцина содержит следовые количества тимеросала (не в качестве консерванта) из производственного процесса [≤0,3 микрограмма (мкг) ртути/доза].
В США используются две вакцины Td: TENIVAC® и TDVAX®.
Каждая доза 0,5 мл препарата Td (MassBiologics) содержит следующие активные ингредиенты: 2 ЛФ столбнячного анатоксина и 2 ЛФ дифтерийного анатоксина. Каждая доза объемом 0,5 мл также содержит алюминиевый адъювант (не более 0,53 мг алюминия по результатам анализа), < 100 мкг (0,02 %) остаточного формальдегида и следовые количества тимеросала (< 0,3 мкг ртути на дозу) (не в качестве консерванта). ) от производственного процесса.
Каждая доза 0,5 мл TENIVAC® (Sanofi Pasteur) содержит следующие активные ингредиенты: 5 Лф столбнячного анатоксина и 2 Лф дифтерийного анатоксина. Другие ингредиенты на дозу 0,5 мл включают 1,5 мг фосфата алюминия (0,33 мг алюминия) в качестве адъюванта и ≤5,0 мкг остаточного формальдегида.
Вакцины против дифтерии, столбняка и коклюша (АКДС)
В настоящее время в США лицензированы и используются 7 детских вакцин АКДС: Daptacel®, Infanrix®, Kinrix®, Pediarix®, Pentacel®, Quadracel® и Vaxelis™ .
Каждая доза 0,5 мл DAPTACEL® (Sanofi Pasteur) содержит 15 Lf дифтерийного анатоксина, 5 Lf столбнячного анатоксина и бесклеточного коклюшного антигена [10 мкг детоксицированного коклюшного токсина (PT), 5 мкг филаментозного гемагглютинина (FHA), 3 мкг пертактина и 5 мкг фимбрий типов 2 и 3 (FIM)]. Другие ингредиенты на дозу 0,5 мл включают 1,5 мг фосфата алюминия (0,33 мг алюминия) в качестве адъюванта, ≤5 мкг остаточного формальдегида, <50 нанограмм (нг) остаточного глутаральдегида и 3,3 мг [0,6% объема на объем (об./об.) ] 2-феноксиэтанол (не в качестве консерванта).
Каждая доза 0,5 мл Infanrix® (GlaxoSmithKline) содержит 25 Lf дифтерийного анатоксина, 10 Lf столбнячного анатоксина, 25 мкг инактивированного PT, 25 мкг FHA и 8 мкг пертактина (белок наружной мембраны 69 кДа). ). Каждая доза 0,5 мл содержит гидроксид алюминия в качестве адъюванта (не более 0,625 мг алюминия по анализу) и 4,5 мг хлорида натрия. Каждая доза также содержит ≤100 мкг остаточного формальдегида и ≤100 мкг полисорбата 80 (Tween 80).
). Каждая доза 0,5 мл содержит гидроксид алюминия в качестве адъюванта (не более 0,625 мг алюминия по анализу) и 4,5 мг хлорида натрия. Каждая доза также содержит ≤100 мкг остаточного формальдегида и ≤100 мкг полисорбата 80 (Tween 80).
Каждая доза 0,5 мл Kinrix® (GlaxoSmithKline) включает те же компоненты дифтерии, столбняка и коклюша, которые перечислены выше в Infanrix®, и включает 40 D-антигенных единиц (DU) полиовируса типа 1 (Mahoney), 8 DU полиовируса типа 2 (MEF- 1) и 32 DU полиовируса 3 типа (Saukett). Каждая доза 0,5 мл содержит гидроксид алюминия в качестве адъюванта (не более 0,6 мг алюминия по анализу) и 4,5 мг хлорида натрия. Каждая доза также содержит ≤100 мкг остаточного формальдегида и ≤100 мкг полисорбата 80 (Tween 80). В процессе производства вакцины против полиомиелита используются неомицин сульфат и полимиксин B. Эти ингредиенты могут присутствовать в готовой вакцине в количестве ≤0,05 нг неомицина и ≤0,01 нг полимиксина B на дозу.
Каждая доза 0,5 мл препарата Pediarix® (GlaxoSmithKline) включает те же компоненты дифтерии, столбняка и коклюша, которые перечислены выше в Infanrix®, компоненты полиовируса, перечисленные выше в Kinrix®, и 10 мкг поверхностного антигена вируса гепатита В ( HBsAg). Каждая доза 0,5 мл содержит соли алюминия в качестве адъюванта (не более 0,85 мг алюминия по анализу) и 4,5 мг хлорида натрия. Каждая доза также содержит ≤100 мкг остаточного формальдегида и ≤100 мкг полисорбата 80 (Tween 80). В процессе производства вакцины против полиомиелита используются неомицин сульфат и полимиксин B. Эти ингредиенты могут присутствовать в готовой вакцине в количестве ≤0,05 нг неомицина и ≤0,01 нг полимиксина B на дозу. Процедуры, используемые для производства антигена HBsAg, приводят к получению продукта, который содержит ≤5% дрожжевого белка.
Каждая доза 0,5 мл содержит соли алюминия в качестве адъюванта (не более 0,85 мг алюминия по анализу) и 4,5 мг хлорида натрия. Каждая доза также содержит ≤100 мкг остаточного формальдегида и ≤100 мкг полисорбата 80 (Tween 80). В процессе производства вакцины против полиомиелита используются неомицин сульфат и полимиксин B. Эти ингредиенты могут присутствовать в готовой вакцине в количестве ≤0,05 нг неомицина и ≤0,01 нг полимиксина B на дозу. Процедуры, используемые для производства антигена HBsAg, приводят к получению продукта, который содержит ≤5% дрожжевого белка.
Каждая доза 0,5 мл препарата Pentacel® (Sanofi Pasteur) содержит 15 Lf дифтерийного анатоксина, 5 Lf столбнячного анатоксина, бесклеточные коклюшные антигены (20 мкг детоксицированного PT, 20 мкг FHA, 3 мкг пертактина, 5 мкг FIM), инактивированные полиовирусы [40 DU типа 1 (Mahoney), 8 DU типа 2 (MEF-1), 32 DU типа 3 (Saukett)] и 10 мкг полирибозил-рибитол-фосфата (PRP) H. influenzae типа b, ковалентно связанных до 24 мкг столбнячного анатоксина (PRP-T). Другие ингредиенты на дозу 0,5 мл включают 1,5 мг фосфата алюминия (0,33 мг алюминия) в качестве адъюванта, полисорбат 80 (приблизительно 10 частей на миллион по расчетам), 42,5 мг сахарозы, ≤5 мкг остаточного формальдегида, <50 нг остаточного глутаральдегида, ≤ 50 нг остаточного бычьего сывороточного альбумина, 3,3 мг (0,6% об./об.) 2-феноксиэтанола (не в качестве консерванта), <4 пикограмма (пг) неомицина и <4 пг полимиксина В сульфата.
Другие ингредиенты на дозу 0,5 мл включают 1,5 мг фосфата алюминия (0,33 мг алюминия) в качестве адъюванта, полисорбат 80 (приблизительно 10 частей на миллион по расчетам), 42,5 мг сахарозы, ≤5 мкг остаточного формальдегида, <50 нг остаточного глутаральдегида, ≤ 50 нг остаточного бычьего сывороточного альбумина, 3,3 мг (0,6% об./об.) 2-феноксиэтанола (не в качестве консерванта), <4 пикограмма (пг) неомицина и <4 пг полимиксина В сульфата.
Каждая доза 0,5 мл препарата Quadracel® (Sanofi Pasteur) содержит 15 Lf дифтерийного анатоксина, 5 Lf столбнячного анатоксина, бесклеточные коклюшные антигены (20 мкг детоксицированного PT, 20 мкг FHA, 3 мкг пертактина, 5 мкг FIM) и инактивированные полиовирусы [40 DU типа 1 (Mahoney), 8 DU типа 2 (MEF-1), 32 DU типа 3 (Saukett)]. Другие ингредиенты на дозу 0,5 мл включают 1,5 мг фосфата алюминия (0,33 мг алюминия) в качестве адъюванта, полисорбат 80 (примерно 10 частей на миллион по расчетам), ≤5 мкг остаточного формальдегида, <50 нг остаточного глутаральдегида, ≤50 нг остаточного бычьего альдегида. сывороточный альбумин, 3,3 мг (0,6% об./об.) 2-феноксиэтанола (не в качестве консерванта), <4 пг неомицина и <4 пг полимиксина В сульфата. Quadracel® не содержит консервантов.
сывороточный альбумин, 3,3 мг (0,6% об./об.) 2-феноксиэтанола (не в качестве консерванта), <4 пг неомицина и <4 пг полимиксина В сульфата. Quadracel® не содержит консервантов.
Каждая доза 0,5 мл Vaxelis ™ (MCM Vaccine Company) содержит 15 Lf дифтерийного анатоксина, 5 Lf столбнячного анатоксина, бесклеточные антигены коклюша (20 мкг детоксицированного PT, 20 мкг FHA, 3 мкг пертактина, 5 мкг FIM) , инактивированные полиовирусы [29 DU типа 1 (Mahoney), 7 DU типа 2 (MEF-1), 26 DU типа 3 (Saukett)], 3 мкг PRP H. influenzae типа b, ковалентно связанных с 50 мкг внешней мембранный белковый комплекс (OMPC) Neisseria meningitidis серогруппы B, и 10 мкг HBsAg. Каждая доза 0,5 мл также содержит 319 мкг алюминия из солей алюминия, используемых в качестве адъювантов. Другие ингредиенты на дозу 0,5 мл включают <0,0056% полисорбата 80 и следующие остатки производственного процесса: формальдегид ≤14 мкг, глутаральдегид ≤50 нг, альбумин бычьей сыворотки ≤50 нг, неомицин <5 нг, сульфат стрептомицина <200 нг, <25 нг сульфата полимиксина В, ≤0,125 мкг тиоцианата аммония и ≤0,1 мкг дрожжевого белка (максимум 1% по отношению к белку HBsAg).
Вакцины против столбняка, дифтерии и коклюша (Tdap)
В США используются две вакцины Tdap: Adacel® и Boostrix®.
Каждая доза 0,5 мл препарата Adacel® (Sanofi Pasteur) содержит 5 Lf столбнячного анатоксина, 2 Lf дифтерийного анатоксина и бесклеточного коклюшного антигена (2,5 мкг детоксицированного PT, 5 мкг FHA, 3 мкг пертактина, 5 мкг FIM). Другие ингредиенты на дозу 0,5 мл включают 1,5 мг фосфата алюминия (0,33 мг алюминия) в качестве адъюванта, ≤5 мкг остаточного формальдегида, <50 нг остаточного глутаральдегида и 3,3 мг (0,6% об./об.) 2-феноксиэтанола (не в качестве вспомогательного вещества). консервант).
Каждая доза 0,5 мл Boostrix® (GlaxoSmithKline) содержит 5 Lf столбнячного анатоксина, 2,5 Lf дифтерийного анатоксина, 8 мкг инактивированного PT, 8 мкг FHA и 2,5 мкг пертактина (белок наружной мембраны 69 кДа). ). Каждая доза объемом 0,5 мл содержит гидроксид алюминия в качестве адъюванта (не более 0,39 мг алюминия по анализу), 4,5 мг хлорида натрия, ≤100 мкг остаточного формальдегида и ≤100 мкг полисорбата 80 (Tween 80).
Иммуногенность и эффективность вакцин
Дифтерия и столбняк
Сегодня заболеваемость дифтерией и столбняком в США находится на рекордно низком уровне. Никто никогда не изучал эффективность столбнячного анатоксина и дифтерийного анатоксина в испытаниях вакцин. Однако эксперты делают вывод об эффективности по защитным уровням антитоксина. Полная серия вакцин имеет клиническую эффективность практически 100% в отношении столбняка и 97% в отношении дифтерии. Полная серия включает 3 дозы для людей в возрасте 7 лет и старше и 4 дозы для детей младше 7 лет.80-х годов вплоть до пандемии COVID-19 в 2020 году. Несмотря на это, сегодня коклюш поражает гораздо меньше людей, чем до того, как вакцины, содержащие коклюш, стали широко доступны в 1940-х годах. Есть несколько причин, которые помогают объяснить, почему в последнее время мы наблюдаем больше случаев:
- Повышение осведомленности
- Усовершенствованные диагностические тесты
- Улучшенная отчетность
- Больше циркуляции бактерий
- Ослабевающий иммунитет
Бесклеточные коклюшные вакцины, используемые в настоящее время в Соединенных Штатах, не защищают так долго, как предыдущая цельноклеточная коклюшная вакцина.
