8 антибиотиков, которые можно использовать лишь в крайнем случае
Всемирная организация здравоохранения составила список антибиотиков, являющихся последней надеждой человечества.
Из-за роста количества устойчивых к антибиотикам бактерий эксперты ВОЗ предложили разделить лекарственные препараты на три группы. В первую группу попали наиболее безобидные для здоровья пациентов лекарства, которые предназначены для борьбы с воспалительными и инфекционными заболеваниями. В частности, в этой группе оказались ампициллин, амоксициллин и другие подобные препараты, которые можно применять достаточно широко – но, тем не менее, тоже только по назначению врача и при условии наблюдения за состоянием пациента.
Лекарства из второй группы вроде ципрофлоксацина, гликопептидов, макролидов (азитромицин, кларитромицин, эритромицин), гликопептидов (ванкомицин), пенициллинов, карбапенемов и пенемов врачам нужно выписывать с большей осторожностью, поскольку они предназначены лишь для небольшого числа болезней. Эти лекарства обладают высоким потенциалом к резистентности, их следует назначать в качестве препаратов второй очереди.
Эти лекарства обладают высоким потенциалом к резистентности, их следует назначать в качестве препаратов второй очереди.
Ну а в третьей группе осталось 8 препаратов, являющихся последней надеждой человечества, которые необходимо выписывать только в случаях самых тяжелых, угрожающих жизни болезней при множественной устойчивости к другим лекарствам. Это средства третьей очереди, назначающиеся исключительно для помощи особым пациентам, которым уже не помогают никакие другие лекарства. Данные антибиотики ни в коем случае нельзя применять необдуманно, поскольку если в организме пациента выработается резистентность и к ним, то никакой надежды у него не останется, а сам штамм бактерий станет неуязвимым.
1. Азтреонам. Моноциклический синтетический бактерицидный бета-лактамный антибиотик, который активен исключительно в отношении некоторых штаммов аэробных бактерий. Лекарство рекомендуется применять при лечении тяжелых инфекционных болезней вроде сепсиса, менингита, эндокардита и перитонита.
2. Цефипим. Это четвертое поколение цефалспоринов, предназначенное для лечения устойчивой ко всем прочим антибиотикам пневмонии (а как писал Sobesednik.ru, по последним данным, это почти 22% случаев этого заболевания), сопровождающейся бактериемией, фебрильной нейтропенией, осложненных инфекций мочевыводящих путей, включая пиелонефрит, а также инфекций кожи и мягких тканей.
3. Цефтаролин. Это уже пятое поколение цефалспоринов. Применяется для осложненных инфекций кожи и мягких тканей, внебольничной пневмонии, тяжелых разновидностей сепсиса, борьбы с бактериями Streptococcus pneumoniae, Staphylococcus aureus (только метициллинчувствительные), Haemophilus influenzae, Haemophilus parainfluenzae, Klebsiella pneumoniae и Escherichia coli.
4. Полимиксины. Эти антибиотики нарушают цитоплазматическую мембрану бактерий, у них очень узкий спектр активности против грамотрицательной флоры. Чаще всего данные антибиотики используют для борьбы с особо устойчивой синегнойной палочкой.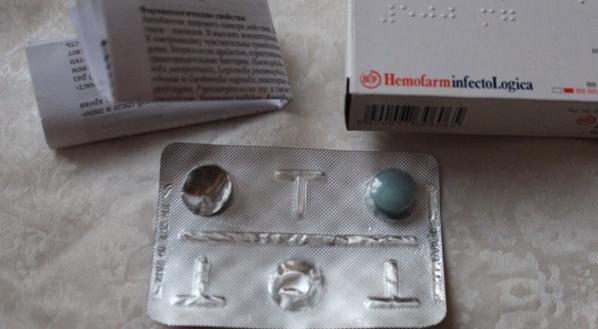
5. Фосфомицин. Это антибиотик широкого спектра действия, созданный на основе фосфоновой кислоты. С его помощью лечат бактериальный цистит, послеоперационные инфекции мочевыводящих путей, хронический бактериальный простатит, бактериальный уретрит и другие бактериальные урологические расстройства.
6. Оксазолидиноны. Еще один новый класс синтетических антибиотиков, имеющий узкий спектр активности. В основном они воздействуют на грамположительные кокки, включая MRSA, пенициллинорезистентные пневмококки и ванкомицинорезистентные энтерококки, которые показали устойчивость ко всем другим антибиотикам.
7. Тигециклин. Эффективное средство при особо устойчивой пневмонии, интраабдоминальных инфекциях, инфекциях кожи и мягких тканей.
8. Даптомицин. Антибиотик группы циклических липопептидов. Применяется для лечения инфекций, вызванных грамположительными бактериями. В частности, им можно лечить инфекции кожи и мягких тканей после ран, подкожные абсцессы, бактериальный эндокардит и расстройства, вызванные золотистым стафилококком.
[:wsame:][:wsame:]
крах антибиотика
КРАХ АНТИБИОТИКА
Антибиотики, ставшие когда – то открытием медицины, бесславно заканчивают свою историю. Их бесконтрольное применение привело к антибиотикорезистентности, проще говоря, к устойчивости бактерий к лекарственным препаратам. Всемирная организация здравоохранения (ВОЗ) добавляет пессимизма: практически все существующие патогенные бактерии приобретут устойчивость к антибиотикам уже в ближайшие десятилетия. Чем же тогда будет лечиться человечество?
Достойная альтернатива.
В результате устойчивости к антибиотикам в странах Европейского союза ежегодно умирают около 25 тысяч человек. Предотвратить бедствие могут только новые препараты, способные воздействовать на возбудителей опасных инфекций. В качестве альтернативы ученые предлагают бактериофаги (в переводе с греческого – «пожиратели бактерий») – специфические вирусы, которые способны точечно воздействовать на патогенную бактерию и разрушать ее.
Пять причин бессилия.
До 1929 года – когда английский ученый Александр Флеминг выделил антибиотик пенициллин – практически в 90% случаев пневмония заканчивалась летальным исходом. Новое лекарство позволило практически полностью одержать победу над тяжелым заболеванием. И врачи были уверены, что антибиотики навсегда избавят мир от опасных инфекций. Однако в настоящее время сил у антибиотиков поубавилось: 25% штаммов возбудителей пневмонии устойчивы к пенициллину, 480 штаммов, вызывающих сепсис (заражение крови), устойчивы более чем к шести антибактериальным препаратам (некоторые штаммы – к 20). Резистентность синегнойной палочки (может вызвать послеоперационные инфекции глаз, приводящие к слепоте, заболевания центральной нервной системы, желудочно-кишечного тракта, пневмонию) составляет 33%.
Почему же антибактериальные препараты, которые спасали людей столько лет, в настоящее время оказываются бездейственными?
- Основная причина – высокая популярность и доступность лекарств в свободной продаже.
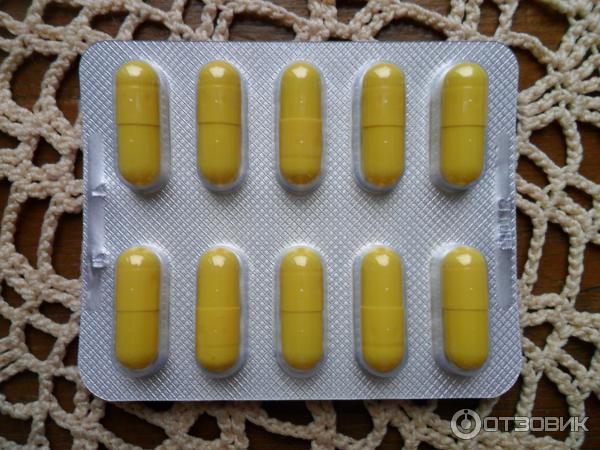 Антибиотик найдется в каждой домашней аптечке и чаще всего он попадает туда без рецепта врача. А ведь у каждого препарата свое определенное воздействие на организм: антибактериальное, противогрибковое, противовирусное и противоопухолевое. Антибиотики обладают избирательным действием на те или иные виды микробов и точно знают свой «путь назначения». Они проходят по кровотоку, собираются в области среднего уха и эффективно справляются с отитами, другие проникают в костную ткань и борются с остеомиелитом. Понятно, что при таком точном воздействии ошибка в выборе лекарства не проходит бесследно. Болезнетворные микроорганизмы вырабатывают штаммы, и антибиотик становится неэффективен.
Антибиотик найдется в каждой домашней аптечке и чаще всего он попадает туда без рецепта врача. А ведь у каждого препарата свое определенное воздействие на организм: антибактериальное, противогрибковое, противовирусное и противоопухолевое. Антибиотики обладают избирательным действием на те или иные виды микробов и точно знают свой «путь назначения». Они проходят по кровотоку, собираются в области среднего уха и эффективно справляются с отитами, другие проникают в костную ткань и борются с остеомиелитом. Понятно, что при таком точном воздействии ошибка в выборе лекарства не проходит бесследно. Болезнетворные микроорганизмы вырабатывают штаммы, и антибиотик становится неэффективен.  Регулярно попадая в небольших количествах в наш организм, те и другие «прививают» болезнетворные бактерии к лечебным препаратам.
Регулярно попадая в небольших количествах в наш организм, те и другие «прививают» болезнетворные бактерии к лечебным препаратам.- Третья причина
- Четверная причина – отсутствие на рынке эффективных фармацевтических препаратов. Дело в том, что разработка новых антибиотиков – чрезвычайно трудоемкое и дорогостоящее мероприятие. На создание одного средства требуется не менее десяти лет и не менее 1,5 миллиардов долларов.
- И наконец, пятая причина – сложность проведения лабораторной диагностики бактерий на чувствительность к антибиотикам.
Наш опыт.
В настоящее время медики пришли к выводу – в связи с высокой устойчивостью бактерий к антибиотикам необходимо сокращать количество необоснованных назначений данных препаратов и обратить внимание на альтернативные методы лечения.
В медицине бактериофаги стали использовать гораздо раньше, чем антибиотики. Русский ученый Николай Гамалея еще в 1898 году завершил исследование и успешно применил их для лечения различных инфекций и заживления ран. Нов сороковых годах прошлого века мировая медицина признала антибиотики лучшим средством от инфекционных заболеваний и отказалась от применения бактериофагов в качестве лечебных препаратов. Исследования в этой области продолжались только в СССР. И сегодня Россия, пожалуй, единственная страна, где фармацевтические производства выпускают бактериофаги с учетом контроля качества и эффективности препаратов.
Портрет с натуры.
Так что же собой представляют бактериофаги и как они борются с болезнетворными бактериями? Эти микроскопические представители семьи вирусов размером 0,1-0,2 миллимикрона встречаются в воде, земле, на плодах, ягодах и даже на коже человека. При большом увеличении внешне они напоминают космический корабль, готовый к запуску.
«Бактериофаги можно сравнить со снайперами: они обладают строгой специфичностью, направленностью, и, в отличие от антибиотиков, не подавляют нормальную микрофлору, иммунную защиту и не способствуют аллергизации. Кроме того, они безопасны и нетоксичны» говорит Ольга Дарбеева, главный эксперт управления экспертизы противобактериальных препаратов ЦЭКМИБП ФГБУ «НЦЭСМП» Минздравсоцразвития России.
Выбор – за доктором.
Лекарственные формы бактериофагов могут быть разными – инъекции, таблетки, аэрозоли, ректальные свечи. Выбор зависит от заболевания.
К примеру, при хронических воспалительных заболеваниях, а также при фурункулах, карбункулах, пиодермите делают инъекции, при цистите бактериофаг вводят в мочевой пузырь через катетер, гнойные раны лечат орошением и примочками жидким фагом. В некоторых случаях врачи сочетают препараты. Так, чтобы справиться с дисбактериозом, назначают таблетки (за час до еды) и клизмы с раствором бактериофага. Лечение инфекции проводится обычно тремя курсами по 7-20 дней с интервалом между ними в три дня.
Мощные антибиотики, обнаруженные с помощью AI
Бактерии Escherichia coli , окрашенные в зеленый цвет, на сканирующей электронной микрофотографии. Фото: Стефани Шуллер/SPL
Новаторский подход к машинному обучению выявил новые мощные типы антибиотиков из пула из более чем 100 миллионов молекул, в том числе один, который работает против широкого спектра бактерий, включая туберкулез и штаммы, считающиеся неизлечимыми.
Устойчивость к антибиотикам связана с языковой проблемой
Исследователи говорят, что антибиотик, названный галицином, является первым обнаруженным с помощью искусственного интеллекта (ИИ). Хотя ИИ и раньше использовался для помощи в некоторых частях процесса открытия антибиотиков, они говорят, что это первый случай, когда он идентифицировал совершенно новые виды антибиотиков с нуля, без использования каких-либо предыдущих человеческих предположений. Работа под руководством биолога-синтетика Джима Коллинза из Массачусетского технологического института в Кембридже опубликована в
Это замечательное исследование, говорит Джейкоб Даррант, специалист по вычислительной биологии из Университета Питтсбурга, штат Пенсильвания. По его словам, команда не только идентифицировала кандидатов, но и проверила перспективные молекулы в тестах на животных. Более того, этот подход можно применять и к другим типам лекарств, например, к тем, которые используются для лечения рака или нейродегенеративных заболеваний, говорит Даррант.
Резистентность бактерий к антибиотикам резко возрастает во всем мире, и исследователи прогнозируют, что, если не будут срочно разработаны новые лекарства, к 2050 году резистентные инфекции могут убивать десять миллионов человек в год. Но за последние несколько десятилетий открытие и одобрение регулирующими органами новых антибиотиков замедлился. «Люди снова и снова находят одни и те же молекулы, — говорит Коллинз. «Нам нужны новые химические вещества с новыми механизмами действия».
Забудьте о своих предположениях
Коллинз и его команда разработали нейронную сеть — алгоритм искусственного интеллекта, вдохновленный архитектурой мозга, — который изучает свойства молекул атом за атомом.
Исследователи обучили свою нейронную сеть обнаруживать молекулы, подавляющие рост бактерии Escherichia coli , используя набор из 2335 молекул, для которых была известна антибактериальная активность. Это включает в себя библиотеку из около 300 одобренных антибиотиков, а также 800 натуральных продуктов растительного, животного и микробного происхождения.
Алгоритм учится предсказывать молекулярную функцию без каких-либо предположений о том, как действуют лекарства, и без маркировки химических групп, говорит Регина Барзилай, исследователь ИИ в Массачусетском технологическом институте и соавтор исследования. «В результате модель может изучать новые закономерности, неизвестные экспертам-людям».
После того, как модель была обучена, исследователи использовали ее для проверки библиотеки под названием Центр перепрофилирования лекарственных средств, которая содержит около 6000 молекул, изучаемых в отношении болезней человека. Они попросили его предсказать, какой из них будет эффективен против E. coli и показать им только те молекулы, которые внешне отличаются от обычных антибиотиков.
Устойчивость к последним антибиотикам распространилась дальше, чем ожидалось
Из полученных совпадений исследователи отобрали около 100 кандидатов для физического тестирования. Один из них — молекула, которую исследуют для лечения диабета — оказался сильнодействующим антибиотиком, который они назвали галицином в честь HAL, интеллектуального компьютера в фильме 2001: Космическая одиссея 9. 0004 . В тестах на мышах эта молекула была активна против широкого спектра патогенов, включая штамм Clostridioides difficile и один из Acinetobacter baumannii , который является «панрезистентным» и против которого срочно требуются новые антибиотики.
0004 . В тестах на мышах эта молекула была активна против широкого спектра патогенов, включая штамм Clostridioides difficile и один из Acinetobacter baumannii , который является «панрезистентным» и против которого срочно требуются новые антибиотики.
Протонная блокада
Антибиотики действуют посредством ряда механизмов, таких как блокирование ферментов, участвующих в биосинтезе клеточной стенки, репарации ДНК или синтезе белка. Но механизм действия галицина нетрадиционный: он нарушает поток протонов через клеточную мембрану. В первоначальных испытаниях на животных он также показал низкую токсичность и устойчивость к резистентности. По словам Коллинза, в экспериментах устойчивость к другим антибиотикам обычно возникает в течение дня или двух. «Но даже после 30 дней таких испытаний мы не обнаружили никакой устойчивости к галицину».
Затем команда исследовала более 107 миллионов молекулярных структур в базе данных под названием ZINC15. Из короткого списка 23, физические тесты выявили 8 с антибактериальной активностью. Два из них обладали мощной активностью против широкого спектра патогенов и могли подавлять даже устойчивые к антибиотикам штаммы E. coli .
Два из них обладали мощной активностью против широкого спектра патогенов и могли подавлять даже устойчивые к антибиотикам штаммы E. coli .
Исследование является «прекрасным примером растущего объема работ с использованием вычислительных методов для обнаружения и предсказания свойств потенциальных лекарств», — говорит Боб Мерфи, специалист по вычислительной биологии из Университета Карнеги-Меллона в Питтсбурге. Он отмечает, что ранее были разработаны методы искусственного интеллекта для анализа огромных баз данных генов и метаболитов с целью определения типов молекул, которые могут включать новые антибиотики 9.0015 2 , 3 .
Но Коллинз и его команда говорят, что их подход отличается — вместо того, чтобы искать определенные структуры или молекулярные классы, они обучают свою сеть искать молекулы с определенной активностью. Теперь команда надеется наладить партнерские отношения с сторонней группой или компанией, чтобы провести клинические испытания галицина. Он также хочет расширить подход к поиску новых антибиотиков и созданию молекул с нуля. Барзилай говорит, что их последняя работа является доказательством концепции. «Это исследование собирает все воедино и демонстрирует, на что оно способно».
Он также хочет расширить подход к поиску новых антибиотиков и созданию молекул с нуля. Барзилай говорит, что их последняя работа является доказательством концепции. «Это исследование собирает все воедино и демонстрирует, на что оно способно».
Ссылки
Stokes, J. M. et al. Сотовый https://doi.org/10.1016/j.cell.2020.01.021 (2020).
Артикул Google ученый
Мохимани, Х. и др. ACS Chem. биол. 9 , 1545–1551 (2014).
Артикул пабмед Google ученый
Цао, Л. и др. Сотовая система 9 , 600–608 (2019).
Артикул пабмед Google ученый
Скачать ссылки
Антибиотики | Johns Hopkins Medicine
Что такое антибиотики?
Антибиотики — сильнодействующие лекарства, используемые для лечения определенных заболеваний. Однако антибиотики не лечат все, а ненужные антибиотики могут даже навредить.
Однако антибиотики не лечат все, а ненужные антибиотики могут даже навредить.
Существует два основных типа микробов, вызывающих большинство инфекций. Это вирусы и бактерии.
Вирусы вызывают:
Антибиотики не могут убить вирусы или помочь вам почувствовать себя лучше, когда у вас есть вирус.
Бактерии вызывают:
Антибиотики убивают определенные бактерии.
Некоторые вирусы вызывают симптомы, напоминающие бактериальные инфекции, а некоторые бактерии могут вызывать симптомы, напоминающие вирусные инфекции. Ваш лечащий врач может определить тип вашего заболевания и порекомендовать правильный тип лечения.
Что такое резистентные бактерии?
Каждый раз, когда вы принимаете антибиотик, бактерии погибают. Иногда бактерии, вызывающие инфекции, уже устойчивы к назначенным антибиотикам. Бактерии также могут стать устойчивыми во время лечения инфекции. Резистентные бактерии не реагируют на антибиотики и продолжают вызывать инфекцию. Распространенным заблуждением является то, что организм человека становится устойчивым к определенным лекарствам. Однако именно бактерии, а не люди, становятся устойчивыми к лекарствам.
Однако именно бактерии, а не люди, становятся устойчивыми к лекарствам.
Каждый раз, когда вы без необходимости или неправильно принимаете или даете ребенку антибиотик, вы увеличиваете вероятность развития устойчивых к лекарствам бактерий. Поэтому крайне важно принимать антибиотики только в случае необходимости. Из-за этих устойчивых бактерий некоторые заболевания, которые раньше легко поддавались лечению, теперь становятся практически неизлечимыми.
Бактерии могут развить устойчивость к определенным лекарствам:
Устойчивость к лекарствам возникает, когда бактерии вырабатывают способы выживания при использовании лекарств, предназначенных для их уничтожения или ослабления.
Если микроб становится устойчивым ко многим лекарствам, лечение инфекций может стать трудным или даже невозможным.
Кто-то с инфекцией, устойчивой к определенному лекарству, может передать эту устойчивую инфекцию другому человеку.
 Таким образом, трудноизлечимая болезнь может передаваться от человека к человеку.
Таким образом, трудноизлечимая болезнь может передаваться от человека к человеку.В некоторых случаях устойчивое к антибиотикам заболевание может привести к серьезной инвалидности или даже смерти.
Резистентность может возникнуть, если бактериальная инфекция вылечена лишь частично. Чтобы предотвратить это, важно закончить прием антибиотиков в соответствии с инструкциями, даже если ваш ребенок чувствует себя лучше.
Когда необходимы антибиотики?
Этот сложный вопрос, на который должен ответить лечащий врач, зависит от конкретного диагноза. Например, существует несколько типов ушных инфекций — большинству из них нужны антибиотики, а некоторым нет. В большинстве случаев боль в горле вызывается вирусами. Один вид, острый фарингит, диагностированный лабораторным тестом, нуждается в антибиотиках.
Обычные вирусные инфекции, такие как кашель или простуда, иногда могут осложниться и развиться бактериальная инфекция. Однако лечение вирусных инфекций антибиотиками для предотвращения бактериальных инфекций не рекомендуется из-за риска возникновения бактериальной резистентности:
Однако лечение вирусных инфекций антибиотиками для предотвращения бактериальных инфекций не рекомендуется из-за риска возникновения бактериальной резистентности:
Помните, что антибиотики не действуют при вирусной простуде и гриппе и что ненужные антибиотики могут быть вредными.
Поговорите со своим лечащим врачом об антибиотиках и узнайте о различиях между вирусами и бактериями, а также о том, когда следует и не следует использовать антибиотики.
Если ваш ребенок получает антибиотик, обязательно давайте его точно так, как это предписано, чтобы уменьшить развитие резистентных бактерий. Попросите ребенка закончить весь рецепт. Не останавливайтесь, когда симптомы инфекции исчезнут.
Никогда не оставляйте оставшиеся антибиотики на всякий случай. Эта практика также может привести к устойчивости бактерий.
Не делитесь своими антибиотиками с кем-то еще и не принимайте антибиотики, которые были прописаны кому-то другому.

