Дисбактериоз у грудного ребенка или гадание по содержимому подгузников
Наталия Гербеда-Вильсон
Лидер Ла Лече Лиги
Август 2008г.
Очень часто родители грудничков в России сталкиваются с необходимостью сдать анализы на дисбактериоз, а потом и лечить его. Ситуация обычно развивается по следующему сценарию: у ребенка наблюдается жидкий по сравнению с детьми на искусственных заменителях грудного молока и взрослыми стул, или зеленоватый стул, или пенистый стул, и врач рекомендует сдать анализы на дисбактериоз. Назначенное лечение, как правило, включает в себя прием препаратов, содержащих полезные бактерии-пробиотики и дрожжи. В худшем случае, грешат на грудное молоко и рекомендуют перевести ребенка на иные виды вскармливания.
Что же такое дисбактериоз? Бывает ли он у грудных детей? Что делать, если ребенку ставят такой диагноз? Нужно ли волноваться? (Прим. автора. Тут я немного забегу вперед, чтобы успокоить всех мам. Дисбактериоз у грудных детей – неслыханная вещь!) Давайте шаг за шагом разберемся с вопросом, который поглощает умы всех мам во всех уголках планеты – содержимое подгузников ребенка и что это значит.
Содержимое кишечника и подгузников здорового грудничка
В период внутриутробного развития желудочно-кишечный тракт (ЖКТ) плода стерилен. Там нет никаких бактерий и других микроорганизмов. Когда ребенок рождается, ЖКТ заселяется, или колонизируется, бактериями, которые попадают ему в рот во время прохождения через родовые пути матери. Бактерии могут также попасть ребенку из материнского стула во время родов. Именно так создается нормальная и здоровая микрофлора кишечника. После рождения ЖКТ ребенка заселяется бактериями, которые находятся в окружающей среде, во рту и на коже матери. Это происходит во время кормления грудью, при поцелуях и прикосновениях к ребенку.
В грудном молоке содержится бифидус-фактор, вещество, которое способствует росту бифидобактерий. Неудивительно, что бифидобактерии составляют 95-99% флоры кишечника детей на грудном вскармливании. Бифидобактерии, которые иногда называют еще пробиотиками, являются частью здоровой флоры кишечника. Да-да, это те самые пробиотики, которые обычно прописывают как лечение от дисбактериоза. Эти добрые «рыцари» способствуют пищеварению, нормальной работе иммунной системы, а также не дают разростаться потенциально патогенным бактериям, которые приводят к заболеваниям. Бифидобактерии преобладают в кишечнике у грудного ребенка до тех пор, пока грудное молоко составляет бо́льшую часть питания ребенка. Помимо этого, в кишечнике грудничка в небольших количествах могут обитать стрептококки, бактероиды, клостридии, микрококки, энтерококки и кишечная палочка (
Да-да, это те самые пробиотики, которые обычно прописывают как лечение от дисбактериоза. Эти добрые «рыцари» способствуют пищеварению, нормальной работе иммунной системы, а также не дают разростаться потенциально патогенным бактериям, которые приводят к заболеваниям. Бифидобактерии преобладают в кишечнике у грудного ребенка до тех пор, пока грудное молоко составляет бо́льшую часть питания ребенка. Помимо этого, в кишечнике грудничка в небольших количествах могут обитать стрептококки, бактероиды, клостридии, микрококки, энтерококки и кишечная палочка (
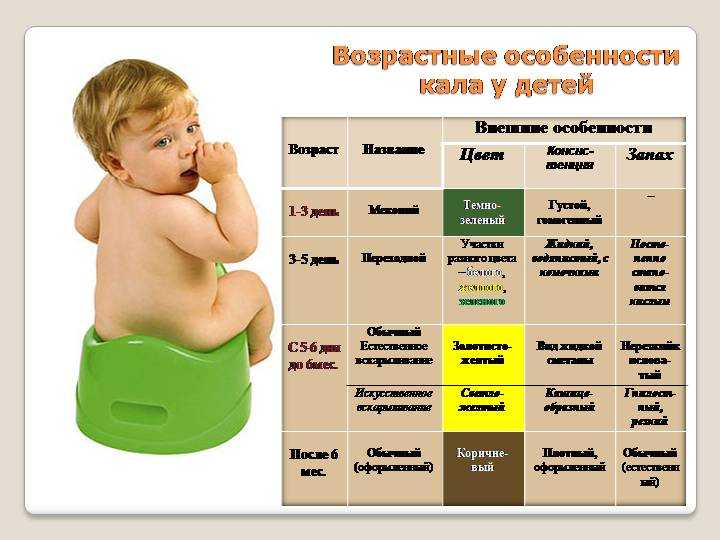
Сразу же после рождения ребенок начинает сосать грудь и получает молозиво, которое обладает слабительным эффектом. Это помогает быстро избавиться от первого стула новорожденного – мекония. Меконий – черный, липкий, похожий на смолу стул, без запаха. При частых прикладываниях в первые сутки, меконий выходит за первые 48 часов.
По мере прихода молока, стул новорожденного меняется с темного на более светлый. Переходный стул обычно зеленоватого цвета и жиже, чем меконий. К пятому дню жизни ребенка его стул становится желтым, похожим на горчицу или густой гороховый суп, часто зернистым, с вкраплениями, похожими на кусочки творога. Цвет стула грудного ребенка может варьироваться от желтого до желто-зеленого или желто-коричневого. Изредка стул может быть зеленым или пенистым. У стула грудных детей нет запаха или же запах неотталкивающий и слабый сладковатый или творожистый запах (что невероятно помогает менять грязные подгузники!)
В первые три дня после рождения число опорожнений кишечника должно соответствовать возрасту ребенка – в первые сутки ребенок должен опорожнить кишечник один раз, на вторые сутки – два, на третьи – три. После прихода молока грудной ребенок опорожняет кишечник минимум 3-4 раза в сутки, и количество стула довольно значительное. Большинство грудных детей опорожняют кишечник намного чаще, нередко после каждого кормления.
По мере взросления, в районе 6 недель от рождения или чуть раньше, многие грудные дети переходят на более редкий режим дефекации – от раза в несколько дней до раза в неделю или даже реже. При этом отсутствуют признаки запора (сухой, твердый стул) – стул ребенка попрежнему неоформленный, пюреобразный.
Введение любой другой пищи помимо грудного молока приведет к изменению консистенции, цвета и запаха стула у грудного ребенка. Если вы начали вводить прикорм, в стуле можно будет заметить кусочки пищи, которую вы даете ребенку.
Как мы видим, нормы дефекации и стула грудных детей значительно отличаются от нормы взрослых. То, что стало бы признаком беспокойства и поводом обратиться к врачу у взрослых, является нормой у грудничков. Для сравнения, нормы детей на грудном вскармливании значительно отличаются от показателей и детей на смешанном и искусственном вскармливании.
Содержимое подгузника грудничка, на которое следует обратить внимание
Отклонения от нормы частоты и внешнего вида стула не всегда означает, что ребенок обязательно чем-то болен. Однако, стул ребенка может быть полезным признаком достаточности питания или симптомом аллергии. В таких случаях изменение способа кормления или устранения аллергена – все что требуется для решения проблемы.
Частый, водянистый, зеленый и/или пенистый стул может быть признаком недоедания. Нередко такой стул бывает в сочетании с медленным набором веса. Иногда такое состояние называют дисбаланс переднего и заднего молока. Ребенок высасывает много переднего молока с низким содержанием жира, которое проходит через пищеварительную систему слишком быстро и вызывает вышеуказанные симптомы.
Если у малыша постоянно зеленый и водянистый стул, это может быть признаком аллергии. Помимо этого у ребенка может быть рвота, слизь или кровь в стуле, а также раздражительность, высыпания на коже. В этом случае особенно важно продолжать кормить грудью, т.к. отлучение от груди сопряжено с повышением риска аллергий. О том как справляться с аллергией у грудного ребенка можно узнать в статье Аллергии и семья грудного ребенка
Если ваш малыш пачкает более 12-16 подгузников в сутки, и стул плохо пахнет и водянистый – это понос. Обычно понос у грудных детей быстро проходит сам по себе и без всяких осложнений. Причной поноса может стать инфекция, лечение антибиотиками, введение прикорма, чрезмерное потребление фруктовых соков.
Что такое дисбактериоз
Дисбактериоз (от гр. dys- «нарушение, расстройство», bacterio- «бактерии» и –sis «состояние») или дисбиоз – нарушение качественного или количественного баланса микроорганизмов в организме, в данном случае, в кишечнике. Это значит, что изменилась пропорция бактерий в кишечнике или там появились необычные для нормальной флоры микроорганизмы. Дисбактериоз часто связывают с кишечными инфекциями и лечением антибиотиками.
Это значит, что изменилась пропорция бактерий в кишечнике или там появились необычные для нормальной флоры микроорганизмы. Дисбактериоз часто связывают с кишечными инфекциями и лечением антибиотиками.
Диагностирование дисбактериоза проводится по симптомам или же анализом кала на дисбактериоз. Обозначить симптомы дисбактериоза трудно, так как это состояние не является заболеванием согласно «Международной статистической классификации болезней и проблем, связанных со здоровьем» Десятого пересмотра (МКБ-10) – документу Всемирной организации здравоохранения, который является общепринятой международной диагностической классификацией в здравоохранении.
Обычно, показанием к анализу на дисбактериоз является непроходящий в течение двух или трех суток понос. У взрослых людей и детей на искусственном вскармливании понос определяется как частый и жидкий стул. Как уже было сказано выше, для грудных детей частый, неоформленный жидкий стул является нормой, поэтому не может являться показанием для анализов. Среди других симптомов, которые служат поводом для лабораторных исследований на дисбактериоз могут быть зеленоватый стул, стул со слизью, запор (редкий стул у грудных детей часто ошибочно принимают за запор), пенистый стул, частички непереваренной пищи. Все эти симптомы не у грудных детей действительно сопровождают поносы, которые часто вызваны патогенными бактериями и требуют лечения антибиотиками. У грудных детей каждый из перечисленных признаков может являться разновидностью нормы.
Среди других симптомов, которые служат поводом для лабораторных исследований на дисбактериоз могут быть зеленоватый стул, стул со слизью, запор (редкий стул у грудных детей часто ошибочно принимают за запор), пенистый стул, частички непереваренной пищи. Все эти симптомы не у грудных детей действительно сопровождают поносы, которые часто вызваны патогенными бактериями и требуют лечения антибиотиками. У грудных детей каждый из перечисленных признаков может являться разновидностью нормы.
Насколько показательны анализы на дисбактериоз у здоровых грудных детей?
Изучение состава кишечной флоры у здорового грудного ребенка, то есть ребенка без видимых симптомов заболевания, в данном случае поноса, представляет интерес для ученых, но не для родителей или практикующих врачей. Многочисленные исследования показали, что грудное молоко защищает детей от заболеваний, даже если кишечник колонизирован патогенными микроорганизмами. Например, в грудном молоке содержатся антитела и факторы против кишечной палочки, холерного вибриона, сальмонеллы, шигеллы, ротавируса и лямблии.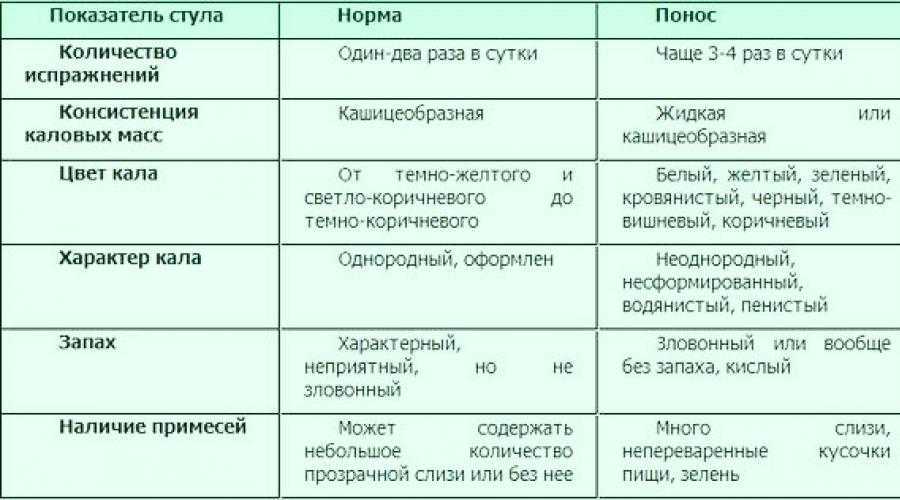 Это значит, что в стуле может высеваться патологический микроорганизм, но ребенок при этом не проявляет никаких симптомов заболевания.
Это значит, что в стуле может высеваться патологический микроорганизм, но ребенок при этом не проявляет никаких симптомов заболевания.
Когда нужно обратится к врачу?
В крайне редких случаях грудному ребенку может понадобиться медицинская помощь.
Обратитесь к врачу, если у ребенка в первые недели жизни наблюдается
- понос (более 12 дефекаций в сутки, водянистый стул)
- рвота
- темпаратура
- летаргия
- низкий набор веса
- потеря в весе
Обратитесь к врачу с грудным ребенком любого возраста, если у ребенка появились признаки обезвоживания
- слабость
- сонливость или летаргия
- слабый плач
- кожа не разглаживается быстро, если ее ущипнуть
- отсутствие слез
- сухой рот, во рту мало или отсуствует слюна
- менее двух мокрых подгузников в сутки
- моча темная, с сильным запахом
- запавший родничок
- температура
Что нужно знать и помнить кормящей маме?
Кормление грудью является самой настоящей страховкой здоровья желудочно-кишечного тракта ребенка в течение первых лет жизни. Грудное молоко способствует росту бифидобактерий, которые препятствуют колонизации кишечника болезнетворными бактериями, а также содержит антитела и факторы, которые защищают ребенка от болезни, даже если патогенным бактериям удалось прижиться в кишечнике. Кормление грудью помогает восстановить баланс микрофлоры кишечника ребенка после лечения антибиотиками. Попросту говоря, грудным детям дисбактериоз не страшен.
Грудное молоко способствует росту бифидобактерий, которые препятствуют колонизации кишечника болезнетворными бактериями, а также содержит антитела и факторы, которые защищают ребенка от болезни, даже если патогенным бактериям удалось прижиться в кишечнике. Кормление грудью помогает восстановить баланс микрофлоры кишечника ребенка после лечения антибиотиками. Попросту говоря, грудным детям дисбактериоз не страшен.
Библиография
Lawrence, R. A. and Lawrence R.M. Breastfeeding: A Guide for the Medical Profession, 6th ed. St. Louis: Mosby, 2005.
Mohrbacher N., Stock J. Breastfeeding Answer Book, Third Revised Edition, January 2003, La Leche League International.
Mosby’s Dictionary of Medicine, Nursing & Health Professions. 7th ed. St. Louis: Mosby, 2005.
Riordan, J. and Auerbach, K. Breastfeeding and Human Lactation, 3rd ed. Boston: Jones and Barlett, 2005.
World Health Organization. International Statistical Classification of Diseases and Related Health Problems. 10th revision, version 2007. Доступ 6 августа 2008, http://www.who.int/classifications/icd/en/
10th revision, version 2007. Доступ 6 августа 2008, http://www.who.int/classifications/icd/en/
Смагин А.Ю. «Пробиотики и пребиотики у новорожденных и детей грудного возраста (обзор литературы)». Журнал интенсивная терапия 2007. Доступ 6 августа 2008, http://www.icj.ru/2007-02-03.html
Симптомы дисбактериоза кишечника у детей — описание болезни, причины появления, способы профилактики и лечение заболевания
Дисбактериоз — это нарушение нормального соотношения микроорганизмов в кишечнике человека. Дисбактериоз обнаруживается только при микробиологическом исследовании. Клиническим его эквивалентом является дисбиоз кишечника. Заболевания под названием «дисбактериоз» не существует.
Дисбиоз кишечника часто встречается у детей младшего возраста.
- Позднее прикладывание к груди.
- Искусственное вскармливание.
- Неполноценное питание.
Изменения состава микрофлоры — это лишь следствие каких-то неблагоприятных событий в организме, т. е. дисбактериоз всегда является вторичным состоянием.
е. дисбактериоз всегда является вторичным состоянием.
К дисбактериозу могут привести:
- Нарушения моторики кишечника — запоры, поносы, возникающие по различным причинам.
- Заболевания, вызывающие нарушения всасывания в кишечнике.
- Хронические заболевания желудка и кишечника (гастродуодениты, язвенная болезнь, неспецифический язвенный колит и др.).
- Аллергические заболевания (пищевая аллергия, атопический дерматит).
- Острые инфекционные заболевания (кишечные инфекции, грипп и др.).
- Воздействие радиации.
- Различные хирургические вмешательства.
- Применение антибиотиков и других лекарств.
Симптомы
- Неустойчивый стул.
- Кишечные колики, боли в животе.
- Метеоризм.
- Неприятный запах изо рта.
- Снижение аппетита. Диагностика дисбактериоза основывается на данных лабораторных исследований: исследование кала на дисбактериоз.
Профилактика
- Грудное вскармливание.
- Искусственное вскармливание только адаптированными смесями.
- Корректное введение прикорма.
- Прием пробиотиков и пребиотиков после длительного лечения антибиотиками и после перенесенных кишечных инфекций.
- Изменение рациона питания детей до года только согласно рекомендациям педиатра.
- Увеличение в рационе ребенка доли кисломолочных продуктов, овощей и фруктов.
- Исключение продуктов, содержащих консерванты.
- Перерыв в приемах пищи не более 5 часов.
Подробнее о детской гастроэнтерологии в клинике «ЮгМед»
Оставляя свои персональные данные, Вы даете добровольное согласие на обработку своих персональных данных. Под персональными данными понимается любая информация, относящаяся к Вам, как субъекту персональных данных (ФИО, дата рождения, город проживания, адрес, контактный номер телефона, адрес электронной почты, род занятости и пр). Ваше согласие распространяется на осуществление Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед» любых действий в отношении ваших персональных данных, которые могут понадобиться для сбора, систематизации, хранения, уточнения (обновление, изменение), обработки (например, отправки писем или совершения звонков) и т.п. с учетом действующего законодательства. Согласие на обработку персональных данных даётся без ограничения срока, но может быть отозвано Вами (достаточно сообщить об этом в Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед»). Пересылая в Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед» свои персональные данные, Вы подтверждаете, что с правами и обязанностями в соответствии с Федеральным законом «О персональных данных» ознакомлены.
Ваше согласие распространяется на осуществление Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед» любых действий в отношении ваших персональных данных, которые могут понадобиться для сбора, систематизации, хранения, уточнения (обновление, изменение), обработки (например, отправки писем или совершения звонков) и т.п. с учетом действующего законодательства. Согласие на обработку персональных данных даётся без ограничения срока, но может быть отозвано Вами (достаточно сообщить об этом в Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед»). Пересылая в Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед» свои персональные данные, Вы подтверждаете, что с правами и обязанностями в соответствии с Федеральным законом «О персональных данных» ознакомлены.
Вмешательство при дисбактериозе у детей, рожденных путем кесарева сечения — Полный текст — Анналы питания и метаболизма 2018, Vol.
 73, Доп. 3
73, Доп. 3Симбиотические отношения между микробами и человеком имеют основополагающее значение для физиологического развития и здоровья. Микробиом новорожденного претерпевает кардинальные изменения в процессе рождения и в первую тысячу дней жизни. Мать-природа предоставила нам наилучший возможный старт для достижения эубиоза: вагинальные роды, чтобы получить микробиом нашей матери и грудное молоко, которое способствует установлению полезных бактерий. Младенцы, лишенные одного или обоих этих эволюционных даров, подвергаются важной модификации микробных сообществ, что приводит к состоянию дисбактериоза, повышающему вероятность возникновения различных иммунных, воспалительных и метаболических нарушений. Можем ли мы подражать природе? Существуют ли вмешательства при дисбактериозе у детей, рожденных путем кесарева сечения? В этом обзоре мы попытаемся ответить на этот интригующий вопрос на основе самых последних научных данных.
Введение
Люди эволюционировали, чтобы жить и процветать в среде, густо населенной микробами. В последнее время стало очевидным, что наше существование в микробном мире можно определить не просто как сожительство, а как взаимовыгодный симбиоз [1].
В последнее время стало очевидным, что наше существование в микробном мире можно определить не просто как сожительство, а как взаимовыгодный симбиоз [1].
Состоящая из 10 11 –10 12 микроорганизмов на грамм фекалий и насчитывающая более 500 видов, кишечная микробиота является важным посредником в норме и болезни и взаимодействует с различными органами и системами в организме, включая мозг, печень, кости и сердечно-сосудистую систему. Это сложная экосистема, сформированная эволюцией, с ассоциациями бактерий-хозяев, которые способствуют тонкому равновесию, эволюционировавшему для модуляции иммунных реакций и укрепления здоровья [2].
Микробная колонизация желудочно-кишечного тракта является важным процессом, определяющим физиологию и иммунитет хозяина, который начинается на раннем этапе развития и претерпевает глубокие изменения в течение жизни.
Этот деликатный процесс, развившийся в ходе эволюции и характеризующийся высокой численностью различных видов бактерий, может подвергнуться нескольким модификациям, вторичным по отношению к различным условиям окружающей среды, что в конечном итоге может привести к невыгодному для хозяина. Эти факторы могут включать способ родоразрешения, гестационный возраст при рождении, использование антибиотиков в раннем возрасте, вскармливание младенцев, чрезмерную гигиену и воздействие окружающей среды, а также другие медицинские вмешательства.
Эти факторы могут включать способ родоразрешения, гестационный возраст при рождении, использование антибиотиков в раннем возрасте, вскармливание младенцев, чрезмерную гигиену и воздействие окружающей среды, а также другие медицинские вмешательства.
На протяжении десятилетий считалось, что в паре плод-мать отсутствуют микробы до момента родов и первого контакта с вагинальным и фекальным микробным сообществом матери. Однако недавние данные свидетельствуют о том, что колонизация начинается внутриутробно; действительно, микробы были идентифицированы в амниотической жидкости, пуповинной крови, плодных оболочках, меконии и плаценте [3]. Недавние исследования с использованием комбинации культуральных и некультуральных методов предполагают, что новорожденные могут подвергаться воздействию микробов, попадающих в амниотическую жидкость, даже при наличии интактных плодных оболочек или культурально-позитивного хориоамнионита [4]. Следует помнить, что в течение последнего триместра беременности плод проглатывает большое количество амниотической жидкости, которая достигает кишечника плода с высокой иммунореактивностью и подвергается воздействию большого количества микробов и микробных компонентов/продуктов.
Однако возрождение к жизни является первым и наиболее важным окном микробного воздействия: это критически важная и уникальная возможность начать формирование стабильной основной кишечной микробиоты. Процесс вагинальных родов позволяет микробиому матери служить «стартовой культурой» для микробиома младенца: во время родов и вскоре после этого бактерии матери и окружающей среды колонизируют кишечник младенца.
Вагинальное рождение — это способ, которым природа устроила рождение млекопитающих, и эволюция диады мать-плод развивалась вокруг этой особенности, и это продолжалось миллионы лет. Однако природа не могла предвидеть, что появятся другие способы рождения. Кесарево сечение (кесарево сечение) спасло чрезвычайно большое количество жизней; однако в последние десятилетия это стало стандартной, а иногда и ненужной или, что еще хуже, удобной практикой. За последние 2 десятилетия частота кесарева сечения в некоторых странах приблизилась к 50%, что свидетельствует о малом интересе к тому, как «способ родоразрешения» может повлиять на здоровье в долгосрочной перспективе.
За последние несколько столетий, особенно в промышленно развитых странах, увеличение числа рождений с помощью кесарева сечения, показателей недоношенности и использования антибиотиков во время беременности, в дополнение к изменениям в питании младенцев, условиях жизни, диете, образе жизни и общей гигиене могут изменили способы приобретения кишечных микробных сообществ. Модификация микробных сообществ может привести к состоянию дисбактериоза, повышая вероятность возникновения различных иммунных (например, астма), воспалительных (воспалительное заболевание кишечника) и метаболических (например, детское ожирение) нарушений.
В настоящее время известно, что микробная колонизация после вагинальных родов отличается от таковой после кесарева сечения [5]; во время вагинальных родов контакт с вагинальной и кишечной флорой матери является наиболее важным источником микробной колонизации младенцев, способствующей колонизации в основном Lactobacilli, Prevotella и Bifidobacteria [6]. Напротив, во время кесарева сечения колонизация новорожденного осуществляется бактериями из окружающей среды, не происходящими от матери, что приводит к менее разнообразной флоре и бактериальному сообществу, напоминающему микробиоту поверхности кожи (стафилококки), и задерживает колонизацию кишечника лактобациллами, бифидобактериями и бактероидами. [7]. Недавние данные показывают, что дети, рожденные с помощью планового кесарева сечения, имеют особенно низкое бактериальное богатство и разнообразие, отсроченную колонизацию типа Bacteroidetes и сниженный Th2-ответ в течение первых 2 лет жизни [8, 9].]. Имеющиеся эпидемиологические данные показывают, что атопические заболевания, астма, диабет 1 типа и пищевая аллергия чаще встречаются у детей после кесарева сечения, чем после естественных родов [10].
Напротив, во время кесарева сечения колонизация новорожденного осуществляется бактериями из окружающей среды, не происходящими от матери, что приводит к менее разнообразной флоре и бактериальному сообществу, напоминающему микробиоту поверхности кожи (стафилококки), и задерживает колонизацию кишечника лактобациллами, бифидобактериями и бактероидами. [7]. Недавние данные показывают, что дети, рожденные с помощью планового кесарева сечения, имеют особенно низкое бактериальное богатство и разнообразие, отсроченную колонизацию типа Bacteroidetes и сниженный Th2-ответ в течение первых 2 лет жизни [8, 9].]. Имеющиеся эпидемиологические данные показывают, что атопические заболевания, астма, диабет 1 типа и пищевая аллергия чаще встречаются у детей после кесарева сечения, чем после естественных родов [10].
Хотя все данные, по-видимому, указывают на одно и то же, недавнее многоцентровое исследование в Европе, в котором анализировались 606 младенцев, показало, что способ родоразрешения не влиял на относительную долю бифидобактерий у 6-недельных младенцев. Тем не менее, вагинальные роды были связаны с более высокими средними пропорциями Bacteroides и членов кластера Atopobium и более низкими пропорциями членов группы Coccoides и группы Streptococcus. Дети, родившиеся естественным путем, имели более разнообразную и богатую микробиоту с большей долей в сумме выявленных групп по сравнению с другими детьми [11].
Тем не менее, вагинальные роды были связаны с более высокими средними пропорциями Bacteroides и членов кластера Atopobium и более низкими пропорциями членов группы Coccoides и группы Streptococcus. Дети, родившиеся естественным путем, имели более разнообразную и богатую микробиоту с большей долей в сумме выявленных групп по сравнению с другими детьми [11].
В недавнем исследовании Sakwinska et al. [12] исследовали влияние способа родоразрешения и кормления на вклад матери в микробиоту кишечника и носа младенцев. Используя секвенирование 16S рРНК и специфическую количественную полимеразную цепную реакцию, авторы смогли составить профиль микробиоты 42 матерей и младенцев на участках тела (материнское влагалище, прямая кишка и кожа, стул и нос младенца) и продемонстрировать совпадение между материнским влагалищем и младенцем. фекальная микробиота (минимальная) и ректальная микробиота матери и младенца (высокая).
Montoya-Williams et al. недавно опубликовали систематический обзор влияния способа родов на развитие микробиома младенцев с учетом доступной литературы, опубликованной с 2010 по 2015 год, с единственным ограничением на английском языке. Они сообщили, что микробиом кишечника младенцев, родившихся естественным путем, больше напоминает микробиом влагалища их матерей и, таким образом, чаще состоит из потенциально полезной микробиоты, такой как Lactobacillus, Bifidobacterium и Bacteroides. И наоборот, микробиом младенцев, рожденных с помощью кесарева сечения, показывает повышенную распространенность либо кожной флоры, либо потенциально патогенных микробных сообществ, таких как клебсиеллы, энтерококки и клостридии [13].
Они сообщили, что микробиом кишечника младенцев, родившихся естественным путем, больше напоминает микробиом влагалища их матерей и, таким образом, чаще состоит из потенциально полезной микробиоты, такой как Lactobacillus, Bifidobacterium и Bacteroides. И наоборот, микробиом младенцев, рожденных с помощью кесарева сечения, показывает повышенную распространенность либо кожной флоры, либо потенциально патогенных микробных сообществ, таких как клебсиеллы, энтерококки и клостридии [13].
Вмешивающиеся факторы
Данные по этой теме имеют серьезный недостаток, связанный с несколькими погрешностями. Первоначальная медицинская причина для кесарева сечения, независимо от того, проводится ли процедура по выбору или в экстренном порядке, получали ли матери дородовые или сразу послеродовые антибиотики, а также время грудного вскармливания или искусственного вскармливания — все это факторы, которые еще предстоит полностью понять и изучить. в будущих исследованиях. Наконец, немедицинские переменные, такие как социально-экономический статус матери и семьи, также могут играть важную роль в выборе между кесаревым сечением и вагинальными родами.
Формирование микробиоты кишечника после кесарева сечения
Зная важность «здорового» состава микробиома желудочно-кишечного тракта, становится очевидным, что микробиологические вмешательства во время беременности и в течение первых 1000 дней жизни могут представлять собой эффективные стратегии и окно возможностей для адресных вмешательств, направленных на улучшение здоровья детей в будущем.
Эти стратегии могут быть сосредоточены на матери, на новорожденном или на обоих. Улучшение состояния окружающей среды с помощью различных «гигиенических» привычек и методов охраны здоровья может оказать влияние на формирование микробиоты. В качестве альтернативы вмешательство может быть направлено на мать путем использования пробиотиков, и/или пребиотиков, и/или полиненасыщенных жирных кислот во время беременности. Наконец, вмешательство может быть сосредоточено на новорожденных с различными подходами: микробным «посевом», грудным вскармливанием в отличие от искусственного вскармливания или использованием пробиотиков/пребиотиков. В этом обзоре мы обобщаем возможное биологическое объяснение текущих возможных стратегий, направленных на предотвращение/коррекцию дисбиоза «Когда аист приходит со скальпелем» [14].
В этом обзоре мы обобщаем возможное биологическое объяснение текущих возможных стратегий, направленных на предотвращение/коррекцию дисбиоза «Когда аист приходит со скальпелем» [14].
Окружающая среда
Эпидемиологические исследования показывают, что проживание вблизи естественной сельской или прибрежной среды, часто называемой «зеленой зоной» или «голубой зоной» соответственно, может быть полезным для здоровья человека, поскольку снижает распространенность болезней и увеличивает выживаемость. «Дарвиновский» синтез гипотезы гигиены (или «старых друзей») предполагает, что рост хронических воспалительных заболеваний, начавшийся в Европе в середине 19 века и продолжающийся до сих пор, может быть, по крайней мере, частично связан с нарушением регуляции иммунитета. Ограниченное или неадекватное воздействие специфических микроорганизмов, с которыми мы были совместно эволюционно вовлечены в процессы созревания, ведущие к установлению физиологической иммунной регуляции, может быть источником нынешней эпидемии «современных болезней». Биоразнообразие окружающей среды ребенка, включая членов семьи, контактирующих с младенцами, разный образ жизни и гигиенические практики могут напрямую влиять на разнообразие микробов, которые передаются младенцу.
Биоразнообразие окружающей среды ребенка, включая членов семьи, контактирующих с младенцами, разный образ жизни и гигиенические практики могут напрямую влиять на разнообразие микробов, которые передаются младенцу.
Например, в 2013 г. Azad et al. оценили различные микробы, присутствующие в 24 образцах фекалий, собранных в период с 2008 по 2009 год у 4-месячных младенцев; из 24 младенцев 15 жили в домах как минимум с 1 собакой или кошкой. Исследователи обнаружили, что жизнь с домашними животными приводит к более высокому разнообразию микробов в кишечнике младенцев (по измерению в их фекалиях) [15].
Вмешательства во время беременности
Рацион матери до и во время беременности может влиять на развитие микробиоты кишечника ребенка [16]. Было показано, что избыточное потребление трансжирных кислот (ТЖК) матерями у крыс вызывает слабовыраженное воспаление у младенцев, в то время как добавки Jussara (Euterpe edulis Mart.) во время беременности и лактации обращают вспять эффекты трансжирных кислот и увеличивают количество Lactobacillus spp. у потомства [17].
у потомства [17].
Исследования на мышах показывают, что безглютеновая диета матери увеличивает количество Akkermansia, Proteobacteria, в кишечной микробиоте потомства и снижает заболеваемость диабетом и вялотекущим воспалением [18]. На людях также было показано, что «нездоровая» диета матери во время беременности или плохое питание в раннем детстве может привести к созданию дефектной кишечной микробиоты [19].
Введение пробиотиков будущим матерям, особенно на поздних сроках беременности, может представлять собой эффективную стратегию поддержания здорового микробного состава у детей. Было продемонстрировано, что лечение будущих матерей L. rhamnosus GG способно передавать и сохранять этот штамм новорожденному в течение как минимум 6 и до 24 месяцев. Кроме того, дети, чьи матери получали L. rhamnosus GG на поздних сроках беременности, демонстрируют более высокие показатели колонизации Bifidobacterium по сравнению с детьми, рожденными от матерей, получавших плацебо [20]. Однако во втором исследовании L. rhamnosus GG не удалось положительно модулировать микробное разнообразие, несмотря на то, что он способствовал благоприятному профилю бифидобактерий [21].
rhamnosus GG не удалось положительно модулировать микробное разнообразие, несмотря на то, что он способствовал благоприятному профилю бифидобактерий [21].
Различные рандомизированные контролируемые исследования продемонстрировали, что применение пробиотиков у матери во время беременности и грудного вскармливания может эффективно снизить заболеваемость атопическим дерматитом у ребенка [22]; этот эффект был недавно подтвержден в метаанализе, подтверждающем, что назначение пробиотиков во время беременности предотвращает развитие атопического дерматита у детей [23]. Возможное объяснение этого вывода состоит в том, что введение пробиотиков матерям во время беременности и/или грудного вскармливания может положительно влиять на цитокиновый профиль материнского молока и повышать уровень sIgA в фекалиях младенцев, тем самым способствуя ответу Th2 [24].
В дополнение к пробиотикам, пребиотики также продемонстрировали многообещающие эффекты в улучшении здоровья иммунной системы и микробиоты. Пребиотики — это «неперевариваемые вещества, оказывающие благотворное физиологическое воздействие на хозяина путем избирательной стимуляции роста или активности ограниченного числа местных бактерий». Пребиотики естественным образом встречаются в таких продуктах, как овощи, пшеница и соевые бобы, и обычно представляют собой олигосахариды или более сложные сахариды. На сегодняшний день наиболее часто изучаемыми соединениями являются инулин, фруктоолигосахариды и галактоолигосахариды. Исследования на животных показали, что добавки с пребиотиками во время беременности и кормления грудью приносят пользу потомству, включая модуляцию прибавки веса независимо от приема, увеличение длины толстой кишки, мышечной массы, массы костей и снижение частоты симптомов аллергии / астмы [25]. Исследования на людях ограничены, но добавление неперевариваемых олигосахаридных пребиотиков (в частности, фруктоолигосахаридов и/или галактоолигосахаридов) значительно увеличивает количество материнских фекалий Bifidobacterium spp.
Пребиотики — это «неперевариваемые вещества, оказывающие благотворное физиологическое воздействие на хозяина путем избирательной стимуляции роста или активности ограниченного числа местных бактерий». Пребиотики естественным образом встречаются в таких продуктах, как овощи, пшеница и соевые бобы, и обычно представляют собой олигосахариды или более сложные сахариды. На сегодняшний день наиболее часто изучаемыми соединениями являются инулин, фруктоолигосахариды и галактоолигосахариды. Исследования на животных показали, что добавки с пребиотиками во время беременности и кормления грудью приносят пользу потомству, включая модуляцию прибавки веса независимо от приема, увеличение длины толстой кишки, мышечной массы, массы костей и снижение частоты симптомов аллергии / астмы [25]. Исследования на людях ограничены, но добавление неперевариваемых олигосахаридных пребиотиков (в частности, фруктоолигосахаридов и/или галактоолигосахаридов) значительно увеличивает количество материнских фекалий Bifidobacterium spp. и, что наиболее важно, Bifidobacterium longum; однако этот бифидогенный эффект может не передаваться потомству [26].
и, что наиболее важно, Bifidobacterium longum; однако этот бифидогенный эффект может не передаваться потомству [26].
Вагинальный посев
Прививка новорожденному вагинальной микробиоты матери сразу после кесарева сечения называется вагинальным посевом. Это представляет собой потенциальный способ колонизации младенцев после кесарева сечения микробами, которые они получили бы при вагинальных родах. Вагинальный посев не является технически сложной процедурой. В первой опубликованной статье стерильная марля, смоченная физиологическим раствором, вводилась во влагалище за 1 час до кесарева сечения. Его удаляли перед операцией и хранили в стерильном контейнере до рождения ребенка, после чего марлевым тампоном протирали ребенка, начиная со рта и лица, а затем по всему телу [27]. Это пионерское исследование имеет некоторые существенные ограничения: во-первых, было изучено только 4 ребенка, а анализ микробиома проводился только в течение 30 дней после рождения. Однако этот экспериментальный эксперимент необходимо подтвердить в большей когорте с более длительным наблюдением.
Вагинальный посев постоянно вызывает интерес в научном мире как в средствах массовой информации, так и среди беременных женщин. Под растущим давлением со стороны акушеров и будущих матерей в ноябре 2016 года Американский колледж акушеров и гинекологов выпустил практические рекомендации по процедуре вагинального посева. Их вывод заключался в том, что, хотя преимущества вагинального посева биологически правдоподобны, до сих пор нет подтверждающих доказательств его использования из-за отсутствия данных о безопасности, связанных с рисками и потенциальным вредом для ребенка. Теоретически передача некоторых возбудителей, бессимптомных у матери («стрептококк группы В, вирус простого герпеса, Chlamydia trachomatis и Neisseria gonorrhoea») может быть причиной тяжелых неблагоприятных последствий для младенцев. О подобных предупреждениях сообщили педиатры в Соединенном Королевстве в редакционной статье BMJ в феврале 2016 г. [28].
Грудное вскармливание
Грудное вскармливание является идеальным питанием для новорожденных, и примерно десять лет назад оно считалось бесплодным; в 2003 г. молочнокислые бактерии впервые были описаны в человеческом молоке, взятом у здоровых женщин [29].
молочнокислые бактерии впервые были описаны в человеческом молоке, взятом у здоровых женщин [29].
В настоящее время в грудном молоке описано более 200 различных видов (принадлежащих к 50 разным родам) с большими индивидуальными вариациями [30]. Грудное молоко здоровой матери содержит 10 9 микроорганизмов на литр, и здоровое материнское питание имеет решающее значение для достижения «нормального» состава молока и правильной микробиоты кишечника у младенца [31].
В настоящее время грудное молоко признано источником комменсальных и потенциально пробиотических бактерий, выступающих в качестве пионеров на критической стадии начальной колонизации кишечника новорожденных и играющих ключевую роль в здоровье младенцев, способствуя созреванию иммунной системы и конкурентному исключению патогенов. . В период грудного вскармливания начинается колонизация актинобактериями и фирмикутами [32]; актинобактерии представлены в основном Bifidobacterium (В.), B. breve, B. longum, B. dentium, B. infantis, B. Pseudocatenulatum и Firmicutes — Lactobacillus, Enterococcus и Clostridia [33].
dentium, B. infantis, B. Pseudocatenulatum и Firmicutes — Lactobacillus, Enterococcus и Clostridia [33].
Помимо бактерий, грудное молоко характеризуется уникальным присутствием олигосахаридов грудного молока (HMO), которые представляют собой гетерогенную смесь неконъюгированных гликанов, не перевариваемых хозяином, и являются основным источником углерода для кишечных бактерий: а, изменение профиля олигосахаридов в молоке влияет на формирование микробов в кишечнике младенцев [34]. Грудное молоко также содержит много антимикробных факторов, таких как лизоцим, лактоферрин и секреторный иммуноглобулин А (IgA), которые вызывают дополнительный отбор в микробном сообществе кишечника [35].
Было обнаружено, что ранний контакт кожа к коже способствует грудному вскармливанию, косвенно способствуя созданию здоровой микробиоты кишечника.
Пребиотики/добавки с пробиотиками
Пробиотики — это живые микроорганизмы, которые при введении в адекватных количествах приносят пользу здоровью хозяина [36]. Как можно более раннее введение пробиотиков может дать потомству большее преимущество в формировании эубиотической кишечной микробиоты. Механизмы, с помощью которых пробиотики оказывают положительное влияние на хозяина, находятся в центре внимания ряда доклинических и клинических исследований и включают в себя все следующее: (а) улучшение микробного состава кишечника, (б) сохранение его стабильности, (в) конкуренция с патогенов для питательных веществ, роста и адгезии, (d) укрепления барьера слизистой оболочки кишечника, (e) противовоспалительного эффекта и (f) модуляции иммунной системы. Установлено, что определенные штаммы пробиотиков обладают способностью изменять состав микробиоты кишечника: у здоровых детей раннего возраста, получавших смесь с добавлением Lactobacillus rhamnosus GG, было повышенное количество лактобацилл по сравнению с теми, кто получал обычную смесь [37]. Добавление пробиотиков с Bifidobacterium breve Bb12 у младенцев с очень низкой массой тела при рождении приводило к колонизации кишечника, а также к быстрому росту Lactobacillus по сравнению с плацебо.
Как можно более раннее введение пробиотиков может дать потомству большее преимущество в формировании эубиотической кишечной микробиоты. Механизмы, с помощью которых пробиотики оказывают положительное влияние на хозяина, находятся в центре внимания ряда доклинических и клинических исследований и включают в себя все следующее: (а) улучшение микробного состава кишечника, (б) сохранение его стабильности, (в) конкуренция с патогенов для питательных веществ, роста и адгезии, (d) укрепления барьера слизистой оболочки кишечника, (e) противовоспалительного эффекта и (f) модуляции иммунной системы. Установлено, что определенные штаммы пробиотиков обладают способностью изменять состав микробиоты кишечника: у здоровых детей раннего возраста, получавших смесь с добавлением Lactobacillus rhamnosus GG, было повышенное количество лактобацилл по сравнению с теми, кто получал обычную смесь [37]. Добавление пробиотиков с Bifidobacterium breve Bb12 у младенцев с очень низкой массой тела при рождении приводило к колонизации кишечника, а также к быстрому росту Lactobacillus по сравнению с плацебо.
Гарсия Роденас и др. [38] была направлена на оценку реакции микробиоты детей, родившихся после кесарева сечения, на смесь, содержащую Lactobacillus reuteri DSM 17938. Младенцы, рожденные путем кесарева сечения и вагинально, были рандомизированы для получения либо контрольной смеси, либо той же смеси, содержащей Lactobacillus reuteri, в течение 72 часов после образцы при рождении и стула были собраны в возрасте 2 недель и 4 месяцев. Авторы смогли продемонстрировать, что L reuteri DSM 17938 у младенцев, рожденных с помощью кесарева сечения, играет ключевую роль в модулировании раннего развития микробиоты по отношению к составу, обнаруженному после вагинальных родов.
Однако продолжительность приема добавок для обеспечения устойчивого положительного эффекта неизвестна.
Пребиотики — это «субстрат, избирательно используемый микроорганизмами-хозяевами, приносящий пользу для здоровья». Это определение расширяет понятие пребиотиков и, возможно, включает (а) неуглеводные вещества (например, полиненасыщенные жирные кислоты), (б) применение на других участках тела, кроме желудочно-кишечного тракта, и (в) различные категории, кроме продуктов питания [39].
Есть многообещающие результаты исследований, в которых оценивалось влияние смесей с добавками пребиотиков на кишечную флору младенцев. В целом, смесь с добавками пребиотиков по сравнению с смесью без добавок увеличивает мягкость стула и может снизить частоту кишечных инфекций и диареи, уменьшить экзему, уменьшить потребность в лечении антибиотиками и увеличить количество бифидобактерий [40]. К результатам следует относиться с осторожностью, поскольку эти исходы не сообщались и не демонстрировались во всех испытаниях, включенных в обзор, а другие авторы в предыдущих систематических исследованиях не смогли продемонстрировать увеличение количества бифидобактерий или лактобактерий или снижение уровня патогенов (9).0093 Bacteriodes , Escherichia coli ) у младенцев, получающих смесь с пребиотиками [41].
Новые исследования показали важность ОПЗ для улучшения развития кишечной микробиоты и поддержки иммунной защиты. Пуччо и др. [42] оценили влияние детских смесей, дополненных ОПЗ, на рост, переносимость и заболеваемость у здоровых детей. Здоровых младенцев рандомизировали на стандартную детскую смесь или ту же смесь с 1,0 г/л 2’фукозиллактозы (2’FL) и 0,5 г/л лакто-N-неотетраозы (LNnT) в течение 6 месяцев. Они пришли к выводу, что детская смесь с 2’FL и LNnT безопасна, хорошо переносится и поддерживает рост в соответствии с возрастом; добавление ОПЗ было связано с более низким уровнем заболеваемости (в частности, бронхита) по сообщениям родителей и использованием лекарств, что позволяет предположить, что ОПЗ могут оказывать воздействие за пределами желудочно-кишечного тракта.
Здоровых младенцев рандомизировали на стандартную детскую смесь или ту же смесь с 1,0 г/л 2’фукозиллактозы (2’FL) и 0,5 г/л лакто-N-неотетраозы (LNnT) в течение 6 месяцев. Они пришли к выводу, что детская смесь с 2’FL и LNnT безопасна, хорошо переносится и поддерживает рост в соответствии с возрастом; добавление ОПЗ было связано с более низким уровнем заболеваемости (в частности, бронхита) по сообщениям родителей и использованием лекарств, что позволяет предположить, что ОПЗ могут оказывать воздействие за пределами желудочно-кишечного тракта.
Наконец, еще предстоит продемонстрировать, могут ли младенцы, рожденные с помощью кесарева сечения, по сравнению с младенцами, рожденными вагинальными родами, получить больше преимуществ от смеси, дополненной пребиотиками.
Выводы
Первая тысяча дней формирует здоровье будущего человека. Мать-природа предоставила нам наилучшее начало двумя различными способами: вагинальные роды, чтобы получить микробиом нашей матери, сформированный вокруг нашего генома, и грудное молоко, которое способствует установлению полезных бактерий для защиты ребенка от колонизации патогенными бактериями и предотвращения диареи у новорожденных. и инфекции дыхательных путей. Иногда младенцы лишены одного или обоих этих эволюционных даров, что приводит к резким изменениям состава и формы микробиоты с возможным негативным влиянием на здоровье взрослых в будущем. «Новые микробы», приобретенные сразу после рождения в результате кесарева сечения, могут способствовать дисбалансу иммунной системы, играя роль как в раннем постнатальном периоде, так и в течение всей жизни человека. Можем ли мы подражать природе? Конечно, нет, но разработка стратегий достижения золотого стандарта должна основываться на результатах хорошо спланированных и проведенных клинических испытаний, которые мы надеемся провести в ближайшем будущем. Надеясь на лучшее, мы «никогда не думаем о будущем — оно наступает достаточно скоро» (Альберт Эйнштейн).
и инфекции дыхательных путей. Иногда младенцы лишены одного или обоих этих эволюционных даров, что приводит к резким изменениям состава и формы микробиоты с возможным негативным влиянием на здоровье взрослых в будущем. «Новые микробы», приобретенные сразу после рождения в результате кесарева сечения, могут способствовать дисбалансу иммунной системы, играя роль как в раннем постнатальном периоде, так и в течение всей жизни человека. Можем ли мы подражать природе? Конечно, нет, но разработка стратегий достижения золотого стандарта должна основываться на результатах хорошо спланированных и проведенных клинических испытаний, которые мы надеемся провести в ближайшем будущем. Надеясь на лучшее, мы «никогда не думаем о будущем — оно наступает достаточно скоро» (Альберт Эйнштейн).
Заявление о раскрытии информации
У всех авторов нет финансовых отношений, имеющих отношение к этой статье, о раскрытии которой говорится. Все авторы не имеют конфликтов интересов, которые необходимо раскрыть.
Источник финансирования
Нет для объявления.
Авторское право: Все права защищены. Никакая часть данной публикации не может быть переведена на другие языки, воспроизведена или использована в любой форме и любыми средствами, электронными или механическими, включая фотокопирование, запись, микрокопирование или любую систему хранения и поиска информации, без письменного разрешения издателя. .
Дозировка препарата: авторы и издатель приложили все усилия, чтобы гарантировать, что выбор препарата и дозировка, указанные в этом тексте, соответствуют текущим рекомендациям и практике на момент публикации. Тем не менее, в связи с продолжающимися исследованиями, изменениями в правительственных постановлениях и постоянным потоком информации, касающейся лекарственной терапии и реакций на лекарства, читателю настоятельно рекомендуется проверять вкладыш в упаковке для каждого лекарства на предмет любых изменений в показаниях и дозировке, а также для дополнительных предупреждений. и меры предосторожности. Это особенно важно, когда рекомендуемый агент является новым и/или редко используемым лекарственным средством.
и меры предосторожности. Это особенно важно, когда рекомендуемый агент является новым и/или редко используемым лекарственным средством.
Отказ от ответственности: заявления, мнения и данные, содержащиеся в этой публикации, принадлежат исключительно отдельным авторам и участникам, а не издателям и редакторам. Появление рекламы и/или ссылок на продукты в публикации не является гарантией, одобрением или одобрением рекламируемых продуктов или услуг или их эффективности, качества или безопасности. Издатель и редактор(ы) отказываются от ответственности за любой ущерб, нанесенный людям или имуществу в результате любых идей, методов, инструкций или продуктов, упомянутых в содержании или рекламе.
ваш путеводитель по здоровому кишечнику – Новорожденный ребенок
Микробиом кишечника и грудное вскармливание? Действительно?
Хотите верьте, хотите нет, но кишечный микробиом оказывает БОЛЬШОЕ влияние на результаты грудного вскармливания . Как так? Позволь мне объяснить;
Микробиом не просто так является популярной темой. Триллионы микробов, которые живут в нас и на нас, влияют на наше здоровье и функции на многих уровнях. Микробиом обычно обсуждается в контексте ЖКТ (поскольку именно там живет наибольшая концентрация микробов), но БОЛЬШИНСТВО участков тела имеет свой собственный микробиом, и есть несколько других, которые также влияют на грудное вскармливание.
Триллионы микробов, которые живут в нас и на нас, влияют на наше здоровье и функции на многих уровнях. Микробиом обычно обсуждается в контексте ЖКТ (поскольку именно там живет наибольшая концентрация микробов), но БОЛЬШИНСТВО участков тела имеет свой собственный микробиом, и есть несколько других, которые также влияют на грудное вскармливание.
В третьем триместре микробиомы меняются при подготовке к родам и грудному вскармливанию.
- Микробиом влагалища повышает уровень лактобацилл (полезных микробов) для «воздействия» во время вагинальных родов
- Микробиом кишечника изменяется, увеличивая поглощение и накопление жира и сахара (чтобы увеличить запасы энергии для родов и грудного вскармливания)
- Изменяется микробиом полости рта (мы все еще выясняем, почему!)
- В ткани молочной железы начинают накапливаться микробы в рамках подготовки к грудному вскармливанию
Организм использует лимфатическую систему для «транспортировки» микробов (из других основных резервуаров по всему телу) в ткани молочной железы. Это не только заботится о здоровье и функции ткани молочной железы и грудного молока, но также является одним из основных путей «колонизации» микробов от мамы к ребенку.
Это не только заботится о здоровье и функции ткани молочной железы и грудного молока, но также является одним из основных путей «колонизации» микробов от мамы к ребенку.
Грудное молоко содержит не только «живые бактерии-ПРОбиотики», которые помогают поддерживать и развивать незрелую пищеварительную и иммунную системы младенцев, но также «ПРЕбиотики — олигосахариды грудного молока (HMO)», которые питают определенный тип микробиома в кишечнике развивающегося младенца.
ОПЗ довольно удивительны, они, наверное, моя ЛЮБИМАЯ часть человеческой физиологии!
Мало того, что они регулируют «тип» бактерий, которые растут в кишечнике детенышей, они невероятно индивидуальны (в соответствии с потребностями каждого ребенка), противовоспалительны И могут действовать как «приманки» для патогенов (плохих микробов) чтобы они могли защитить маленький нежный животик малыша, пока он привыкает к миру вне мамы…
Как это удивительно!
Производители детских смесей пытались «имитировать» функции ОПЗ, но они не могут заставить их делать то, что делает грудное молоко, особенно то, как грудное молоко изменяется в ответ на потребности ребенка посредством «рефлекса обратной промывки»
Это не так. меняется не только профиль HMO, но и другие компоненты грудного молока, которые имеют решающее значение для оптимального роста и развития: иммунные клетки, антитела, факторы роста, стволовые клетки, гормоны и т. д.
меняется не только профиль HMO, но и другие компоненты грудного молока, которые имеют решающее значение для оптимального роста и развития: иммунные клетки, антитела, факторы роста, стволовые клетки, гормоны и т. д.
Снова – как это прекрасно!!
Микробиом и результаты грудного вскармливанияДисбактериоз — это термин, описывающий «дисбаланс» в нашем микробиоме, и это может произойти в любом участке тела.
Обычно это выглядит как потеря «хороших жуков» и/или разрастание «плохих жуков».
К сожалению, дисбактериоз очень распространен, так как многие из наших повседневных действий и компонентов нашей «современной жизни» влияют на наши микробы;
- Диета – продукты с высоким содержанием сахара и полуфабрикатов, низким содержанием питательных веществ и клетчатки
- Экологические токсины, гербициды, пестициды, хлор и т. д.
- Стресс
- Общие лекарства — лекарства от кислотного рефлюкса, стероиды, противовоспалительные средства, антидепрессанты — даже парацетамол!
- Антибиотики
Если у вас есть дисбактериоз в какой-либо момент от зачатия до рождения (в любом участке тела), скорее всего, вы перенесете его во время грудного вскармливания.
И если вы в конечном итоге получите ИМП, положительный результат на СГБ или кесарево сечение, это означает, что вам нужно больше антибиотиков (и больше дисбактериоза!).
Очень часто мы входим в эту стадию с нарушенным микробиомом, и это может СИЛЬНО ПОВЛИЯТЬ на результаты грудного вскармливания.
Исследования показывают, что дибиоз может способствовать повышенному риску осложнений при грудном вскармливании, таких как;
- Боль в груди
- Боль в сосках, молочница на сосках, кандидоз полости рта (у детей)
- Воспаление и/или инфекция – мастит
- Закупорка протоков
- Колики/рефлюкс 9014 90148 Дети с неустроенностью0121 Как мне убедиться, что мой микробиом будет способствовать улучшению результатов грудного вскармливания?
Как уже упоминалось, микробиом грудного молока формируется другими участками тела, поэтому лучше всего начинать заботиться о своем микробиоме как можно раньше (даже до зачатия) и во всех частях тела, но это определенно начинается с ЖКТ.
 .
.Диета — это единственное наиболее эффективное вмешательство в наш микробиом, поэтому крайне важно сделать это правильно;
- Много растительных красок , богатые полифенолами (растительные химикаты) цельные продукты – мы должны стремиться к преимущественно РАСТИТЕЛЬНОЙ диете с хорошим разнообразием и разнообразием. Стремитесь к 30-40 порциям РАЗНЫХ растительных продуктов в неделю.
- Овощи, фрукты, орехи, семена, травы, специи, бобовые, бобовые, цельнозерновые – множество вариантов!
- Пищевые продукты с низким содержанием/отсутствием сахара или обработанные продукты (они кормят плохих насекомых)
- Пребиотические продукты – неперевариваемые волокна растительной пищи, КОРМЯЩИЕ живых насекомых
- Пробиотические продукты – продукты, которые на самом деле содержат ЖИВЫХ микробов – йогурт, кефир, чайный гриб, кимчи, квашеная капуста и т. д.
Образ жизни также важен – снижает стресс, снижает воздействие токсинов в окружающей среде, хорошо спит, ведет активный образ жизни, принимает минимум лекарств, практикует осознанность и т.
Пищевые добавки с пре- и пробиотиками д.
д.Даже когда вы хорошо питаетесь, ведете здоровый образ жизни и избегаете лекарств, ДЕЙСТВИТЕЛЬНО трудно избегать продуктов, вызывающих дисбактериоз.
Я применяю подход «оптимизация и защита» при уходе за здоровьем кишечника и микробиомом моего клиента.
Наряду с диетой и изменением образа жизни я использую высококачественные добавки с пребиотиками и полифенолами, а также специальные штаммы пробиотиков, которые оказывают прямое положительное влияние на микробиом определенных участков тела, важных во время беременности и грудного вскармливания — кишечника, влагалища и грудного молока.
Самым сложным для мам здесь является выбор правильных пищевых добавок, поэтому я ВСЕГДА рекомендую проконсультироваться с квалифицированным специалистом в области здравоохранения.
Еще один хороший способ ориентироваться в том, «какие продукты» — это исследования, но опять же, это может быть чем-то вроде минного поля из-за перегрузки информацией от благонамеренных блоггеров о здоровье (подождите, это я прямо сейчас!?!) и Доктор Google, а также молодые мамы могут быть очень ограничены во времени.

