Все, что нужно знать про вирус Коксаки
Что такое вирус Коксаки?
Вирус Коксаки относится к энтеровирусам, которые размножаются в желудочно-кишечном тракте. Энтеровирусы хорошо переносят низкие температуры, сохраняются в воде. Источником инфекции является только человек — больной или здоровый носитель.
Кто находится в зоне риска заражения вирусом Коксаки
Эти вирусы считаются «детскими», поскольку заболевают преимущественно дети от 3 до 10 лет. У взрослых заболевание встречается редко. Считается, что дети до 3-месячного возраста защищены от этого энтеровируса, а после 10-12 лет практически все уже имеют за плечами опыт заражения, после которого вырабатывается устойчивый иммунитет. Таким образом, в группу риска заражения вирусом Коксаки попадают дети старше 3 месяцев и до 12 лет, однако пик заболевания выпадает на период от 3 до 10 лет.
Как происходит заражение вирусом Коксаки
Любые энтеровирусные инфекции считаются болезнями грязных рук, и вирус Коксаки не исключение.
Также возможно заражение воздушно-капельным путем, через зараженные продукты, которые не прошли термическую обработку, и даже воду.
Симптомы и признаки заражения вирусом Коксаки
Инкубационный период длится от 2 до 10 дней, чаще всего заболевание проявляется на 3-4-й день.
Первым симптомом вируса Коксаки может стать появление язвочек и водянистых прыщиков. Как правило, они становятся следствием развивающейся инфекции. Местом их локализации обычно выступают ноги и руки, однако врачи обнаруживают их и в ротовой полости. Со временем и развитием вируса язвы могут появиться по всему телу, но преимущественно они будут располагаться вокруг рта. Также часто наблюдается синдром рука-нога-рот — сыпь появляется одновременно на слизистой рта, ладонях и ступнях.
Вторым симптомом вируса Коксаки может стать плохое самочувствие. возможны сильная головная боль, рвота и диарея. Также поражается слизистая глотки, из-за чего больному трудно принимать пищу.
Третьим признаком вируса Коксаки может стать высокая температура. Она поднимается буквально за несколько часов и может не снижаться около трех дней. Так как этот вирус — инфекционное заболевание, которое не напрямую связано с данным показателем, жаропонижающие медикаментозные препараты окажутся бессильными в борьбе против высокой температуры.
Как правило, врачи рекомендуют уже при обнаружении первых язвочек обращаться в медицинское учреждение, чтобы появления дальнейших симптомов можно было избежать. Для того чтобы выявить вирус, нужно проводить лабораторное исследование.
Профилактика вируса Коксаки
На сегодняшний день вакцины от вируса Коксаки, впрочем, как и от других энтеровирусов, не получено. Единственная профилактика — соблюдение личной гигиены. Но поскольку один из путей передачи вируса — воздушно-капельный, то и этот способ не панацея. Желательно, чтобы ребенок меньше бывал в людных местах, особенно в эпидемический период. Не стоит глотать воду из бассейна, рекомендуется пить только специальную питьевую воду из чистой посуды.
Но поскольку один из путей передачи вируса — воздушно-капельный, то и этот способ не панацея. Желательно, чтобы ребенок меньше бывал в людных местах, особенно в эпидемический период. Не стоит глотать воду из бассейна, рекомендуется пить только специальную питьевую воду из чистой посуды.
В большинстве случаев болезнь постепенно проходит в течение 7-10 дней при симптоматическом лечении. В редких случаях могут развиваться осложнения в виде обезвоживания, менингита или энцефалита (воспаление головного мозга).
В целях профилактики возникновения заболеваний вирусом Коксаки и другими энтеровирусными инфекциями необходимо придерживаться следующих правил:
- соблюдать правила личной гигиены, тщательно мыть руки с мылом перед едой, после посещения туалета, после возвращения с прогулок;
- использовать для питья только бутилированную или кипяченую воду;
- соблюдать температурные условия хранения пищи, употреблять в пищу продукты с известными сроками хранения;
- тщательно мыть фрукты, ягоды, овощи;
-
при ухудшении эпидемиологической ситуации ограничивать допуск детей в бассейны.

При первых признаках ухудшения самочувствия следует обращаться за медицинской помощью. При стандартном течении болезни симптомы исчезают за одну-две недели. В таких случаях помощь больному сводится к облегчению состояния: снижению температуры, предупреждению обезвоживания и созданию необходимых гигиенических условий.
Эпидемия вируса Коксаки на турецких курортах
Что за вирус такой?
Начнем с того, что вирус Коксаки – не название болезни, а название группы вирусов, которые могут вызвать разные заболевания (порядка 30 заболеваний). Относится к семейству энтеровирусов.
Проявляться может поражением дыхательных путей, органов желудочно-кишечного тракта. В редких случаях может вызывать менингиты и энцефалиты.
Это не новое и достаточно распространенное заболевание, которым часто страдают дети не только в жарких странах. Группа вирусов впервые была диагностирована в маленьком городке США Коксаки, именно поэтому название города закрепилось за вирусом. Второе название заболевания – «рука-нога-рот», так как характерная сыпь покрывает именно эти части тела. Заболевание чаще всего встречается у детей до 5 лет и крайне редко у взрослых.
Второе название заболевания – «рука-нога-рот», так как характерная сыпь покрывает именно эти части тела. Заболевание чаще всего встречается у детей до 5 лет и крайне редко у взрослых.
Инкубационный период вируса Коксаки составляет от 4 до 6 дней, опасен в осеннее и летнее время, когда воздух обогащен влагой. Повышенная влажность – это необходимое условие для жизнеспособности данного микроорганизма. Именно поэтому чаще всего вирусом заражаются дети в жаркое время. Например, в прошлом году, когда на Урале было прекрасное, жаркое лето, и у нас было зарегистрировано достаточное количество заболевших вирусом Коксаки.
Как им можно заразиться?
Болезни, вызываемые вирусом Коксаки, передаются воздушно-капельным путем: через немытые руки, общую посуду, немытые овощи или фрукты, сырую воду. Еще вариант: через чихание или кашель.
Специфической профилактики вируса не существует. Необходимо тщательно мыть руки и овощи, следить за чистотой посуды, пить только кипяченую воду, предпочитать бассейну море и, естественно, исключить любые контакты с уже заболевшими людьми.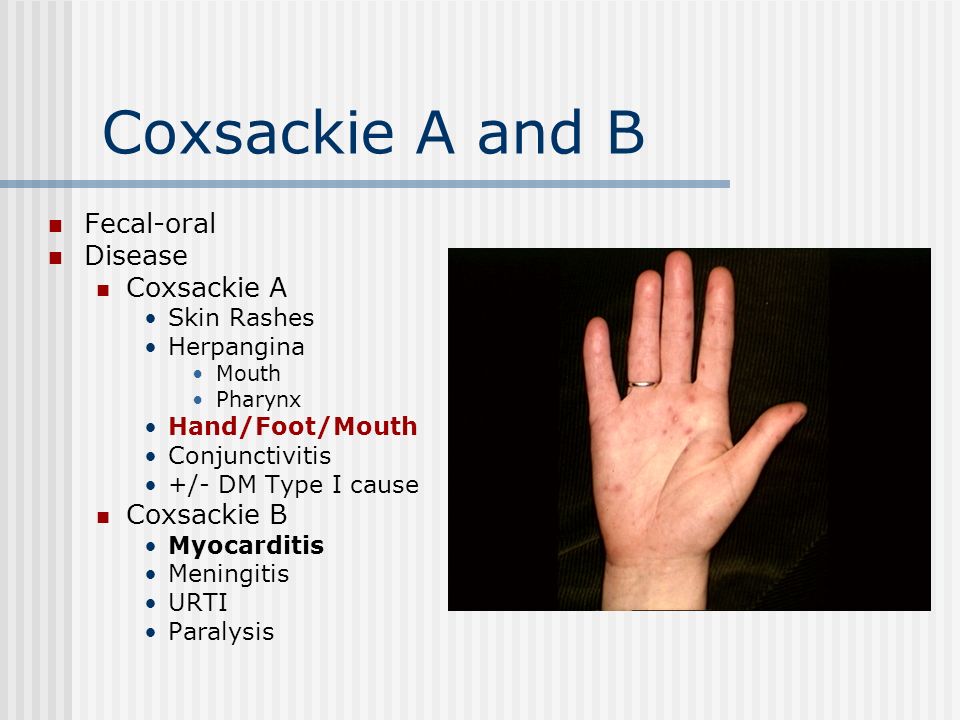
Какие у него симптомы?
Преимущественно вирус Коксаки проявляется нарушением работы кишечника, диареей, общей интоксикацией и характерной сыпью на руках, ногах и в горле, поднимается высокая температура, может болеть горло.
Когда нужно обращаться к врачу?
Если инфекция протекает легко, то есть ребенок относительно хорошо себя чувствует, температура не очень высокая или легко сбивается, нет рвоты и вялости, то к врачу обращаться не обязательно (если вам, конечно, не нужен больничный).
Внимание! Вирусы не лечатся антибиотиками, поэтому при вирусе Коксаки самостоятельное назначение и лечение антибиотиками не приведет к выздоровлению, а только даст побочные эффекты.
К врачу необходимо обратиться при появлении ЛЮБЫХ осложнений: температура держится более трех дней, если сыпь (язвы) в полости рта очень болезненны и мешают открывать рот, есть и пить.
НЕМЕДЛЕННО обратиться к врачу: если температура не сбивается, организм ребенка обезвожен (ребенок не мочится, плачет без слез, губы высохли и потрескались), сильно болит голова на фоне высокой температуры, ребенок не может наклонить голову и достать подбородком груди.
Профилактика
Если в семье заболел один ребенок, то все другие члены семьи под угрозой, особенно дети до 10 лет. Вирус не летает по воздуху, передается только контактно. Поэтому заболевший ребенок должен иметь свои ложки-игрушки (мамы, не доедайте за больным ребенком еду, особенно его ложкой!), и всем членам семьи рекомендуется почаще обрабатывать руки спиртовыми антисептиками.
Оценка инкубационного периода ящура у детей разных возрастных групп
- Список журналов
- Научные отчеты
науч. респ. 2017; 7: 16464.
Опубликовано в сети 28 ноября 2017 г. doi: 10.1038/s41598-017-16705-7
, , , и
Информация об авторе Примечания к статье Информация об авторских правах и лицензии Отказ от ответственности
- заболевание, часто вызывающее крупные вспышки в Азии и иногда в Европе и США.
 Инкубационный период HFMD обычно описывается как около 3–7 дней, но эмпирических данных нет. В этом исследовании мы оценили инкубационный период HFMD после школьных вспышек в Гонконге, используя информацию о появлении симптомов и датах отсутствия по болезни у учащихся с диагнозом HFMD. Всего 9Для анализа были отобраны 9 случаев HFMD из 12 школ. Мы подогнали параметрические модели с учетом интервальной цензуры. На основе наиболее подходящих распределений расчетные средние инкубационные периоды составили 4,4 (95% ДИ 3,8–5,1) дней, 4,7 (95% ДИ 4,5–5,1) дней и 5,7 (95% ДИ 4,6–7,0) дней для детей в детских садах. , начальные школы и средние школы соответственно. Исходя из подобранного распределения, предполагаемые инкубационные периоды могут быть длиннее 10 дней для 8,8% и 23,2% случаев HFMD в детских садах и средних школах соответственно. Наши результаты показывают, что инкубационный период HFMD для учащихся средних школ может быть длиннее, чем обычно описываемые диапазоны. Для борьбы со вспышками может потребоваться длительный период усиленной личной гигиены и дезинфекции окружающей среды.
Инкубационный период HFMD обычно описывается как около 3–7 дней, но эмпирических данных нет. В этом исследовании мы оценили инкубационный период HFMD после школьных вспышек в Гонконге, используя информацию о появлении симптомов и датах отсутствия по болезни у учащихся с диагнозом HFMD. Всего 9Для анализа были отобраны 9 случаев HFMD из 12 школ. Мы подогнали параметрические модели с учетом интервальной цензуры. На основе наиболее подходящих распределений расчетные средние инкубационные периоды составили 4,4 (95% ДИ 3,8–5,1) дней, 4,7 (95% ДИ 4,5–5,1) дней и 5,7 (95% ДИ 4,6–7,0) дней для детей в детских садах. , начальные школы и средние школы соответственно. Исходя из подобранного распределения, предполагаемые инкубационные периоды могут быть длиннее 10 дней для 8,8% и 23,2% случаев HFMD в детских садах и средних школах соответственно. Наши результаты показывают, что инкубационный период HFMD для учащихся средних школ может быть длиннее, чем обычно описываемые диапазоны. Для борьбы со вспышками может потребоваться длительный период усиленной личной гигиены и дезинфекции окружающей среды.
Болезнь рук, ящур — детское заболевание, вызываемое различными вирусами, принадлежащими к роду энтеровирусов, включая вирусы Коксаки, эховирусы и энтеровирусы 1
Инкубационный период HFMD обычно составляет около 3–7 дней 9 .
 Однако недавний и более ранний систематические обзоры выявили отсутствие эмпирических данных об инкубационном периоде HFMD 10 , 11 . Например, в одном исследовании сообщалось, что инкубационный период HFMD «обычно составляет 3–4 дня, но может достигать 10 дней и более» 12 , в то время как в другом исследовании инкубационный период описывался как «начиная от от 5 до 7 дней 13 . Однако доказательств, подтверждающих эти диапазоны инкубационного периода, предоставлено не было, и по этим описаниям трудно определить долю пациентов с HFMD с инкубационными периодами, попадающими в эти диапазоны. Кроме того, инкубационный период может варьироваться к 9 годам.0018
Однако недавний и более ранний систематические обзоры выявили отсутствие эмпирических данных об инкубационном периоде HFMD 10 , 11 . Например, в одном исследовании сообщалось, что инкубационный период HFMD «обычно составляет 3–4 дня, но может достигать 10 дней и более» 12 , в то время как в другом исследовании инкубационный период описывался как «начиная от от 5 до 7 дней 13 . Однако доказательств, подтверждающих эти диапазоны инкубационного периода, предоставлено не было, и по этим описаниям трудно определить долю пациентов с HFMD с инкубационными периодами, попадающими в эти диапазоны. Кроме того, инкубационный период может варьироваться к 9 годам.0018 В 2015–2016 гг. в средних школах Гонконга произошли неожиданные вспышки HFMD. Это обеспечивает данные из более широкого возрастного диапазона случаев HFMD. В нашем исследовании мы оценили инкубационный период HFMD у детей разных возрастных групп от школьных вспышек в Гонконге.

Всего было набрано 1458 участников из 97 классов 35 школ (24 детских сада, 3 начальных и 8 средних школ), в том числе 309клинически диагностированные случаи HFMD. После выбора классов с ≥2 случаями для дальнейшего анализа было выявлено в общей сложности 65 классов с 286 случаями HFMD. Далее мы удалили 147 случаев с отсутствующими датами начала или отсутствия и последующие случаи в том же классе и 40 изолированных случаев. Всего для анализа было доступно 99 случаев HFMD из 12 школ (4 детских сада, 1 начальная и 7 средних школ). Мы выявили 1 случай с предшествующим бытовым заражением и считали, что он не инфицирован в классе, но может заразить других одноклассников.
В таблице показаны основные характеристики случаев HFMD в нашем исследовании. Среди 99 случаев HFMD 64,5% составляют мужчины. Средний возраст составил 12,1 года (стандартное отклонение 4,7 года). Среднее время от появления симптомов до отсутствия болезни составляло 2 дня (межквартильный размах (IQR) 0–2 дня), а среднее число случаев HFMD на класс составляло 2 (IQR 2–4 случая).
 Среднее количество дней от даты начала первого до последнего случая в каждом классе составляло 7,5 (межквартильный интервал 5–14 дней). В среднем было 1,3 инфицированных (диапазон: 1–5), связанных с появлением каждого симптома, чтобы определить период воздействия.
Среднее количество дней от даты начала первого до последнего случая в каждом классе составляло 7,5 (межквартильный интервал 5–14 дней). В среднем было 1,3 инфицированных (диапазон: 1–5), связанных с появлением каждого симптома, чтобы определить период воздействия.Таблица 1
Характеристики 99 диагностированных случаев заболевания рук, ящура в результате школьных вспышек в Гонконге, 2015–2016 гг.
Характеристики n = 99 (%) Мужчина 64 64,6% 64 64,6% 64 64,6% 64 64,6% 9. 
Тип школы Детский сад 17 17,2% Начальная школа 9,1% Вторичная школа 73 73,7% 73,7% . 0–2 Открыть в отдельном окне
На основе дат появления симптомов и дат отсутствия болезни у включенных в анализ случаев HFMD мы подогнали логарифмически нормальное, гамма-распределение и распределение Вейбулла к наблюдаемым диапазонам инкубационных периодов (таблица). Гамма была наиболее подходящей моделью с самым низким AIC для средних и всех школ, а логарифмически-нормальное распределение было наиболее подходящим распределением для детских садов и начальных школ.
 Другие распределения также хорошо соответствовали различиям AIC <3 по сравнению с наиболее подходящим распределением. Большинство распределений удовлетворительно соответствуют наблюдаемым данным, за исключением начальной школы, где у нас был небольшой размер выборки (см. Дополнительный рисунок 9).0018 С2 ). Расчетный средний инкубационный период для всех детей из гамма-распределения составил 5,4 (95% ДИ 4,4–6,5) дней с расчетными 5% и 95% процентилями 1,0 и 16,0 дней соответственно (рис. ). Инкубационный период у учащихся детских садов был самым коротким со средним значением 4,4 (95% ДИ 3,8–5,1), а у учащихся средних школ был самым продолжительным со средним значением 5,7 (95% ДИ 4,6–7,0). Однако различия не были статистически значимыми (тесты начальной загрузки, все значения p>0,07).
Другие распределения также хорошо соответствовали различиям AIC <3 по сравнению с наиболее подходящим распределением. Большинство распределений удовлетворительно соответствуют наблюдаемым данным, за исключением начальной школы, где у нас был небольшой размер выборки (см. Дополнительный рисунок 9).0018 С2 ). Расчетный средний инкубационный период для всех детей из гамма-распределения составил 5,4 (95% ДИ 4,4–6,5) дней с расчетными 5% и 95% процентилями 1,0 и 16,0 дней соответственно (рис. ). Инкубационный период у учащихся детских садов был самым коротким со средним значением 4,4 (95% ДИ 3,8–5,1), а у учащихся средних школ был самым продолжительным со средним значением 5,7 (95% ДИ 4,6–7,0). Однако различия не были статистически значимыми (тесты начальной загрузки, все значения p>0,07).Таблица 2
Расчетный инкубационный период для HFMD в разных возрастных группах.
School type (age range) Median (95% CI)/AIC Weibull Gamma Log-normal Overall (2–18 y) 5,5 (4,5–6,7) 5,4 (4,4–6,5) 4,9 (4,0–5,9) 243,9 242,4 242,5 242,5 242,5 242,5 242,5 Kindergarten (2–5 y) 4.  6 (3.9–5.5)
6 (3.9–5.5)4.7 (4.0–5.5) 4.4 (3.8–5.1) 31.1 29.9 28.3 Primary school ( 6–12 y) 4.7 (4.4–5.1) 4.8 (4.4–5.1) 4.7 (4.5–5.1) 23.9 23.2 23.0 Secondary school (12–18 у) 5,9 (4,8–7,2) 5,7 (4,6–7,0) 5,1 (4,2–6,3) 192.1 191.7 193.6 Открыто в отдельном окне
Открыто в отдельном окне
.
 Оценка была основана на 17, 9 и 73 отобранных случаях HFMD в результате вспышек в детских садах, начальных и средних школах соответственно в Гонконге, 2015–2016 гг. Наиболее подходящими распределениями были логнормальные распределения для детских садов и начальных школ и гамма-распределения для средних школ.
Оценка была основана на 17, 9 и 73 отобранных случаях HFMD в результате вспышек в детских садах, начальных и средних школах соответственно в Гонконге, 2015–2016 гг. Наиболее подходящими распределениями были логнормальные распределения для детских садов и начальных школ и гамма-распределения для средних школ.В качестве анализа чувствительности мы включили первый и не более трех последующих случаев в каждом классе, из которых для анализа было включено 42 случая HFMD. Предполагаемый средний инкубационный период для всех детей тогда составлял 5,7 (95% ДИ: 4,7–6,8) дней с 5% и 95% процентилями 1,3 и 15,2 дня соответственно. Для анализа чувствительности, который ограничивался вспышками одного класса в каждом классе, в анализ были включены 34 случая HFMD. Предполагаемый инкубационный период составил 4,8 (95% ДИ 3,8–5,8) дней, с 5% и 95% процентили 0,9 и 14,0 дней соответственно.
Мы оценили средний инкубационный период HFMD в 4,4 дня (95% ДИ 3,8–5,1) для учащихся детских садов в возрасте около 2–5 лет, что согласуется с диапазоном около 3–7 дней, который обычно указывается различными агентствами здравоохранения 10 .
 Предполагаемый средний инкубационный период HFMD составлял 5,7 (95% ДИ 4,6–7,0) для учащихся средней школы в возрасте около 12–18 лет и, по-видимому, был дольше, хотя разница не достигла статистической значимости при небольшом размере выборки в исследовании. Расчетные инкубационные периоды могут быть длиннее 10 дней для 8,8% и 23,2% учащихся детских садов и средних школ соответственно, исходя из подобранного распределения. Расчетный инкубационный период для детей младшего школьного возраста (n = 9) имели относительно низкую вариабельность по сравнению с другими группами, вероятно, потому, что данные были получены из одной школы и, следовательно, вероятно, были вызваны одним возбудителем. Напротив, относительно высокая вариабельность предполагаемого инкубационного периода у учащихся средних школ (n = 73) может быть объяснена более высокой гетерогенностью иммунных ответов хозяина из-за более раннего воздействия различных патогенов.
Предполагаемый средний инкубационный период HFMD составлял 5,7 (95% ДИ 4,6–7,0) для учащихся средней школы в возрасте около 12–18 лет и, по-видимому, был дольше, хотя разница не достигла статистической значимости при небольшом размере выборки в исследовании. Расчетные инкубационные периоды могут быть длиннее 10 дней для 8,8% и 23,2% учащихся детских садов и средних школ соответственно, исходя из подобранного распределения. Расчетный инкубационный период для детей младшего школьного возраста (n = 9) имели относительно низкую вариабельность по сравнению с другими группами, вероятно, потому, что данные были получены из одной школы и, следовательно, вероятно, были вызваны одним возбудителем. Напротив, относительно высокая вариабельность предполагаемого инкубационного периода у учащихся средних школ (n = 73) может быть объяснена более высокой гетерогенностью иммунных ответов хозяина из-за более раннего воздействия различных патогенов.Насколько нам известно, это первое исследование по оценке распределения инкубационного периода HFMD для разных возрастных групп на основе эмпирических данных.
 В то время как время заражения обычно было ненаблюдаемым, относительно короткий период между началом болезни и отсутствием болезни в школе помог уменьшить неопределенность в периоде воздействия. Предполагаемый инкубационный период не чувствителен к неопределенности из-за ненаблюдаемой цепочки передачи во время вспышек, которые могут включать несколько поколений. Наш вывод может иметь значение для вмешательства или лечения вспышек в школьных условиях, таких как определение основанного на фактических данных периода наблюдения за вспышками HFMD и поддержание более длительного периода усиленной практики личной гигиены и дезинфекции окружающей среды 11 .
В то время как время заражения обычно было ненаблюдаемым, относительно короткий период между началом болезни и отсутствием болезни в школе помог уменьшить неопределенность в периоде воздействия. Предполагаемый инкубационный период не чувствителен к неопределенности из-за ненаблюдаемой цепочки передачи во время вспышек, которые могут включать несколько поколений. Наш вывод может иметь значение для вмешательства или лечения вспышек в школьных условиях, таких как определение основанного на фактических данных периода наблюдения за вспышками HFMD и поддержание более длительного периода усиленной практики личной гигиены и дезинфекции окружающей среды 11 .В нашем исследовании есть некоторые оговорки. Возможна систематическая ошибка припоминания дат появления симптомов и отсутствия болезни. В анкету были включены отдельные вопросы о датах появления основных симптомов HFMD, а также о датах начала и окончания отсутствия по болезни. Когда участников просили сообщить последовательность событий, связанных с эпизодом HFMD, ответы, как правило, были более связными.
 Мы не могли исключить потенциальные инфекции от сообщества. Однако в нашем исследовании мы наблюдали ограниченную передачу от домохозяйства, и вероятность передачи от сообщества должна быть еще меньше в течение ограниченного периода школьных вспышек. Наконец, мы не собирали образцы для лабораторных испытаний, и поэтому нам не хватало информации о штамме вируса, вызывающем заболевание, а также, возможно, неправильно классифицировали случаи HFMD из-за различий в симптомах. В течение периода исследования основным штаммом, циркулирующим в сообществе, был вирус Коксаки А6, с которым было связано 58% вспышек, за которым следовал энтеровирус 71 15 . Необходимы дальнейшие исследования для оценки потенциальной гетерогенности инкубационного периода для различных штаммов вируса. За исключением вакцинации против энтеровируса 71, другие профилактические меры общественного здравоохранения против HFMD обычно не учитывают различия в серотипах. Наши результаты могут улучшить доказательную базу для контроля HFMD.
Мы не могли исключить потенциальные инфекции от сообщества. Однако в нашем исследовании мы наблюдали ограниченную передачу от домохозяйства, и вероятность передачи от сообщества должна быть еще меньше в течение ограниченного периода школьных вспышек. Наконец, мы не собирали образцы для лабораторных испытаний, и поэтому нам не хватало информации о штамме вируса, вызывающем заболевание, а также, возможно, неправильно классифицировали случаи HFMD из-за различий в симптомах. В течение периода исследования основным штаммом, циркулирующим в сообществе, был вирус Коксаки А6, с которым было связано 58% вспышек, за которым следовал энтеровирус 71 15 . Необходимы дальнейшие исследования для оценки потенциальной гетерогенности инкубационного периода для различных штаммов вируса. За исключением вакцинации против энтеровируса 71, другие профилактические меры общественного здравоохранения против HFMD обычно не учитывают различия в серотипах. Наши результаты могут улучшить доказательную базу для контроля HFMD.
Источники данных
Мы набрали детей из детских садов, начальных и средних школ в период с февраля по май 2015 г. и с сентября 2015 г. по январь 2016 г., охватывающих основные пиковые сезоны HFMD в Гонконге. Мы набрали всех учеников из классов, которые сообщили о случаях HFMD. Для настоящего анализа инкубационных периодов были отобраны классы с ≥2 случаями HFMD.
Мы разослали анкеты родителям или законным опекунам учащихся, принявших участие в опросе, для сбора демографической и эпидемиологической информации. Мы также собрали ключевую информацию, касающуюся передачи болезни и прогрессирования HFMD, такую как даты появления симптомов (особенно лихорадки, язвы в полости рта и сыпи), даты отсутствия по болезни и потенциальную эпидемиологическую связь с другими случаями HFMD в домашнем хозяйстве. Поощрения были предусмотрены для случаев HFMD, которые предоставили более подробную информацию. Мы также собрали записи о посещаемости в школах, стратифицированные по случаям HFMD и случаям отсутствия, чтобы оценить полноту данных.

Одобрение этики
Письменное информированное согласие было предоставлено всеми участвующими школами. Для студентов было получено доверенное письменное согласие от родителей или законных опекунов. Протокол исследования был одобрен Институциональным наблюдательным советом Университета Гонконга/управления больниц Западного кластера Гонконга и проводился в соответствии с применимыми рекомендациями.
Статистический анализ
Мы подобрали параметрические распределения к времени от заражения до появления самых ранних симптомов лихорадки, язвы в ротовой полости или сыпи 16 . Точное время заражения не наблюдалось, но окна экспозиции были определены с момента появления симптомов до дня перед отсутствием болезни, при условии, что случаи HFMD были заразны только после появления симптомов 17 . Все потенциальные инфекционные агенты одного и того же класса были включены для построения окон экспозиции, предполагая ограниченную передачу между разными классами.
 Случаи с отсутствующей датой начала или отсутствия заболевания, а также последующие случаи в том же классе были исключены из анализа. Другими словами, в анализ были включены только передачи с полным соблюдением окон экспозиции. Предполагалось, что учащиеся с более ранними случаями HFMD в своих домохозяйствах были инфицированы за пределами школы и были включены в анализ только для контакта с последующими случаями. Мы также учитывали выходные и школьные каникулы, когда в школах не было облучения. Мы использовали максимальную вероятность, чтобы подобрать гамма, распределение Вейбулла и логарифмически нормальное распределение к потенциальным инкубационным интервалам, и выбрали лучшие модели, используя информационный критерий Акаике (AIC). Мы оценили средний инкубационный период для детей в детских садах (в возрасте около 2-5 лет), начальной (в возрасте около 6-11 лет) и средней школе (в возрасте около 12-18 лет) соответственно и вычислили соответствующие 95% доверительный интервал (ДИ) с помощью параметрического бутстрап-подхода с использованием 1000 повторов.
Случаи с отсутствующей датой начала или отсутствия заболевания, а также последующие случаи в том же классе были исключены из анализа. Другими словами, в анализ были включены только передачи с полным соблюдением окон экспозиции. Предполагалось, что учащиеся с более ранними случаями HFMD в своих домохозяйствах были инфицированы за пределами школы и были включены в анализ только для контакта с последующими случаями. Мы также учитывали выходные и школьные каникулы, когда в школах не было облучения. Мы использовали максимальную вероятность, чтобы подобрать гамма, распределение Вейбулла и логарифмически нормальное распределение к потенциальным инкубационным интервалам, и выбрали лучшие модели, используя информационный критерий Акаике (AIC). Мы оценили средний инкубационный период для детей в детских садах (в возрасте около 2-5 лет), начальной (в возрасте около 6-11 лет) и средней школе (в возрасте около 12-18 лет) соответственно и вычислили соответствующие 95% доверительный интервал (ДИ) с помощью параметрического бутстрап-подхода с использованием 1000 повторов. Затем из подобранного распределения 16 был рассчитан 95%-й процентиль инкубационного периода. Более подробная информация о статистическом анализе описана в дополнительной информации.
Затем из подобранного распределения 16 был рассчитан 95%-й процентиль инкубационного периода. Более подробная информация о статистическом анализе описана в дополнительной информации.Анализ чувствительности
Чтобы изучить потенциальное влияние использования данных о вспышках для оценки распределения инкубационного периода, мы проанализировали подмножество случаев, которое консервативно включало первичные случаи и не более трех последующих случаев HFMD в каждом классе. Учитывая репродуктивное число 2,5–5,5 для передачи HFMD в Гонконге 18 , это должно включать большинство случаев первого поколения. Чтобы оценить чувствительность результата к предположению об ограниченной межклассовой передаче, мы определили школьные классы с зарегистрированными случаями HFMD только в одном классе и оценили распределение инкубационного периода в этом подмножестве. Все анализы проводились с помощью R версии 3.3.2. (R Foundation for Statistical Computing, Вена, Австрия).

Дополнительное приложение (244K, pdf)
Благодарим всех участвующих учащихся, родителей, детские сады и школы. Мы также благодарим Венди Чиу за координацию набора в школу. Этот проект был поддержан Программой ранней карьеры Совета по исследовательским грантам Специального административного района Гонконг (грант № 27100814) и Гарвардским центром динамики инфекционных заболеваний Национального института общих медицинских наук (грант № U54 GM088558). . Содержание является исключительной ответственностью авторов и не обязательно отражает официальную точку зрения Национального института общих медицинских наук или Национального института здоровья.
З.Ю. участвовал в разработке дизайна исследования, провел анализ и написал рукопись. Q.Z. собрал и критически рассмотрел рукопись. Би Джей Си участвовал в разработке исследования, анализе и критически рецензировал рукопись. Э.Х.И.Л. участвовал в разработке исследования, анализе, интерпретации данных, написании и критическом обзоре рукописи.
 Все авторы внесли свой вклад в интерпретацию данных, составление статьи и окончательное утверждение версии для публикации.
Все авторы внесли свой вклад в интерпретацию данных, составление статьи и окончательное утверждение версии для публикации.Конкурирующие интересы
B.J.C. получает финансирование исследований от MedImmune Inc. и Sanofi Pasteur и консультирует Crucell N.V. Авторы не сообщают о других потенциальных конфликтах интересов.
Дополнительный электронный материал
Дополнительная информация прилагается к этому документу по адресу 10.1038/s41598-017-16705-7.
Примечание издателя: Springer Nature остается нейтральной в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
1. Pallansch, M.A., Oberste, M.S. & Whitton, JL. In Fields virology (eds David, M. Knipe & Peter, M. Howley) 490–530 (Wolters Kluwer/Lippincott Williams & Wilkins Health, 2013).
2. Chang LY, et al. Клинические особенности и факторы риска отека легких после энтеровируса-71, связанного с болезнью рук, ящура и рта.
 Ланцет. 1999; 354: 1682–1686. doi: 10.1016/S0140-6736(99)04434-7. [PubMed] [CrossRef] [Google Scholar]
Ланцет. 1999; 354: 1682–1686. doi: 10.1016/S0140-6736(99)04434-7. [PubMed] [CrossRef] [Google Scholar]3. Xing W, et al. Болезни рук, ящура и рта в Китае, 2008–2012 годы: эпидемиологическое исследование. Ланцет Инфекционные заболевания. 2014; 14:308–318. дои: 10.1016/S1473-3099(13)70342-6. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
4. Hassel C, et al. Схемы передачи энтеровируса человека 71 в европейские страны, из них и между ними, с 2003 по 2013 год. Евронадзор. 2015;20:2–12. doi: 10.2807/1560-7917.ES.2015.20.34.30005. [PubMed] [CrossRef] [Google Scholar]
5. Центры по контролю и профилактике заболеваний. Заметки с мест: тяжелое заболевание рук, ящура и рта, связанное с вирусом Коксаки A6 — Алабама, Коннектикут, Калифорния и Невада, ноябрь 2011 г. — Февраль 2012 г. MMWR Morb Mortal Wkly Rep. 2012; 61: 213–214. [PubMed] [Академия Google]
6. Wu JT, et al. Плановая детская вакцинация против энтеровируса 71 в Китае: анализ эффективности затрат.
 Плос Мед. 2016;13:e1001975. doi: 10.1371/journal.pmed.1001975. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Плос Мед. 2016;13:e1001975. doi: 10.1371/journal.pmed.1001975. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]7. Отдел эпиднадзора за новыми заболеваниями и реагирования на них Управления безопасности и чрезвычайных ситуаций в области здравоохранения Западно-Тихоокеанского регионального управления. Информационный бюллетень по заболеваниям рук, ящура и рта , http://www.wpro.who.int/emerging_diseases/hfmd.information.sheet/en/ (2012).
8. Мелкий ПЭМ. Интервал между последовательными случаями инфекционного заболевания. Am J Эпидемиол. 2003; 158:1039–1047. doi: 10.1093/aje/kwg251. [PubMed] [CrossRef] [Google Scholar]
9. Всемирная организация здравоохранения. Болезни рук, ящура , http://www.wpro.who.int/mediacentre/factsheets/fs_10072012_HFMD/en/ (2012).
10. Koh WM, et al. Эпидемиология заболеваний рук, ящура и рта в Азии: систематический обзор и анализ. Pediatr Infect Dis J. 2016; 35:e285–300. дои: 10.1097/INF.0000000000001242.
 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]11. Ричардсон М., Эллиман Д., Магуайр Х., Симпсон Дж., Николл А. инфекционные заболевания в школах и дошкольных учреждениях. Pediatr Infect Dis J. 2001; 20:380–391. doi: 10.1097/00006454-200104000-00004. [PubMed] [CrossRef] [Google Scholar]
12. Чанг Л.И. Энтеровирус 71 на Тайване. Педиатр Неонатол. 2008;49: 103–112. doi: 10.1016/S1875-9572(08)60023-6. [PubMed] [CrossRef] [Google Scholar]
13. Qiaoyun F, Xiongfei J, Lihuan L, Angao X. Эпидемиология и этиологические характеристики заболеваний рук, ящура в городе Хуэйчжоу в период с 2008 по 2011 год. Arch Virol. 2013; 158: 895–899. doi: 10.1007/s00705-012-1566-6. [PubMed] [CrossRef] [Google Scholar]
14. Virlogeux, V. et al . Связь между тяжестью инфекций, вызванных вирусом гриппа A(H7N9), и продолжительностью инкубационного периода. Plos One 11 (2016). [Бесплатная статья PMC] [PubMed]
15. Chuang, S.
 Центр охраны здоровья, правительство Специального административного района Гонконг. Инфекционные заболевания Watc h, http://www.chp.gov.hk/files/pdf/cdw_compendium_2016.pdf (2016).
Центр охраны здоровья, правительство Специального административного района Гонконг. Инфекционные заболевания Watc h, http://www.chp.gov.hk/files/pdf/cdw_compendium_2016.pdf (2016).16. Коулинг Б.Дж. и др. Альтернативные методы оценки инкубационного распределения — Примеры тяжелого острого респираторного синдрома. Эпидемиология. 2007; 18: 253–259. doi: 10.1097/01.ede.0000254660.07942.фб. [PubMed] [CrossRef] [Google Scholar]
17. Heymann, D.L. Руководство по борьбе с инфекционными заболеваниями . (Американская ассоциация общественного здравоохранения, 2014 г.).
18. Ma E, et al. Оценка основного репродукционного числа энтеровируса 71 и вируса Коксаки А16 при вспышках ящура и кистей рук. Pediatr Infect Dis J. 2011; 30: 675–679. doi: 10.1097/INF.0b013e3182116e95. [PubMed] [CrossRef] [Google Scholar]
Статьи из научных отчетов предоставлены здесь с разрешения Издательская группа Nature
Болезни рук, ящура и рта — Глава 4 — Желтая книга 2020 г.
 | Travelers’ Health
| Travelers’ HealthHolly M.Biggs
ИНФЕКЦИОННЫЙ АГЕНТ
В Соединенных Штатах вирус Коксаки A16 является важной причиной заболевания рук, ящура и рта (HFMD). Совсем недавно вирус Коксаки А6 был признан причиной вспышек и спорадических случаев заболевания в Соединенных Штатах и во всем мире. В Азиатско-Тихоокеанском регионе энтеровирус 71 является распространенным этиологическим агентом.
ПЕРЕДАЧА ТРАНСМИССИИ
Прямой контакт от человека к человеку со слюной, выделениями из носа и горла, везикулярной жидкостью или стулом инфицированного человека.
ЭПИДЕМИОЛОГИЯ
HFMD, распространенное заболевание у детей раннего возраста, распространено по всему миру. Вспышки часто происходят летом и ранней осенью в Соединенных Штатах. За последние два десятилетия были зарегистрированы крупные вспышки в Камбодже, Китае, Японии, Корее, Малайзии, Сингапуре, Таиланде, Тайване и Вьетнаме. Сезонные модели в Азии варьируются в зависимости от климатических зон.
 В Азии с умеренным климатом, включая материковый Китай, пик заболеваемости приходится на начало лета.
В Азии с умеренным климатом, включая материковый Китай, пик заболеваемости приходится на начало лета.КЛИНИЧЕСКАЯ КАРТИНА
Инкубационный период 3–6 дней. Пациенты обычно обращаются с лихорадкой и недомоганием, сопровождаемыми болью в горле и появлением везикул во рту (обычно спереди, с вовлечением слизистой оболочки щек, языка или твердого неба) и периферической сыпью, часто папуловезикулярной, на руках (ладони) и стопы (подошвы). В некоторых случаях, особенно при инфекции вирусом Коксаки А6, сыпь может быть более распространенной, очаги увеличиваются и сливаются, образуя буллы. Поражения обычно исчезают в течение примерно недели. Онихомадез (выпадение ногтей) и шелушение ладоней или подошв могут возникать во время выздоровления. Редкие осложнения включают асептический менингит и энцефалит. У небольшой части детей с инфекцией энтеровирусом 71 в Азии имели место тяжелые проявления, включая поражение центральной нервной системы и смерть.
ДИАГНОЗ
Диагноз обычно ставится клинически.
 Подтверждающее лабораторное тестирование с использованием ОТ-ПЦР доступно и проводится в атипичных или тяжелых случаях. Предпочтительные образцы для тестирования включают везикулярную жидкость, мазки из горла или ротовой полости или кал. Анализы ОТ-ПЦР для обнаружения РНК энтеровируса доступны во многих коммерческих или справочных лабораториях. Лаборатория пикорнавирусов CDC проводит тестирование и типирование энтеровирусов в отделениях: www.cdc.gov/non-polio-enterovirus/lab-testing/index.html.
Подтверждающее лабораторное тестирование с использованием ОТ-ПЦР доступно и проводится в атипичных или тяжелых случаях. Предпочтительные образцы для тестирования включают везикулярную жидкость, мазки из горла или ротовой полости или кал. Анализы ОТ-ПЦР для обнаружения РНК энтеровируса доступны во многих коммерческих или справочных лабораториях. Лаборатория пикорнавирусов CDC проводит тестирование и типирование энтеровирусов в отделениях: www.cdc.gov/non-polio-enterovirus/lab-testing/index.html.ЛЕЧЕНИЕ
Поддерживающая терапия.
ПРОФИЛАКТИКА
Избегание тесного контакта с инфицированными людьми, поддержание надлежащей гигиены рук и дезинфекция потенциально зараженных поверхностей, включая игрушки.
Веб-сайт CDC: www.cdc.gov/hand-foot-mouth
БИБЛИОГРАФИЯ
- Американская академия педиатрии. Энтеровирус (неполиовирус). В: Кимберлин Д.В., Брэди М.Т., Джексон М.А., Лонг С.С., редакторы. Красная книга: Отчет Комитета по инфекционным заболеваниям за 2015 г.

- Американская академия педиатрии. Энтеровирус (неполиовирус). В: Кимберлин Д.В., Брэди М.Т., Джексон М.А., Лонг С.С., редакторы. Красная книга: Отчет Комитета по инфекционным заболеваниям за 2015 г.
