Гипотрофия у детей раннего возраста — причины гипотрофии, диагностика и лечение, степени
Гипотрофия у детей – дефицит массы, связанный с недостатком либо нарушением усвоения в организме питательных веществ. Ежегодно диагностируется от 2 до 30 % случаев патологии.
Классификация и клинические симптомы
По времени развития гипотрофию классифицируют на внутриутробную и внеутробную. По выраженности различают три степени патологии:
-
гипотрофия 1 степени у детей – недостаток веса до 10-20 % от нормы. Малыши развиваются по возрасту, снижение аппетита незначительное. Кожа бледная, жировой слой истончен;
-
гипотрофия 2 степени у детей – снижение веса на 20-30 % и отставание роста на 2-3 см. Нарушена активность, аппетит плохой. Тургор кожи и тонус мышц резко снижены, жировой слой отсутствует на теле и конечностях;
-
3 степень гипотрофии у детей — недобор веса на 30 % и более, резко выраженное отставание в развитии и росте.

Причины гипотрофии у детей
Гипотрофия у детей раннего возраста возникает под действием внешних и внутренних причин.
Внутренние причины – это различные заболевания: ферментопатии, пороки развития, иммунодефициты.
Внешние причины связаны с тремя факторами:
-
алиментарный: при несбалансированном/недостаточном питании -дефиците грудного молока, частом срыгивании, болезнях (родовые травмы, заячья губа, ДЦП и др.), голодании;
-
инфекционный, связанный с ОРВИ и другими инфекциями;
-
социальный — плохие условия проживания.

Диагностика и лечение гипотрофии у детей
Врожденная патология обнаруживается при УЗИ-диагностике. Приобретенная гипоторофия у детей до года и старше диагностируется при осмотре, изменении антропометрических показателей, подтверждается при углубленном обследовании.
Подход к лечению зависит от причин. Алиментарный фактор корректируется диетой: оптимизацией питания по качеству, нутриентному и витаминно-минеральному составу, калорийности. Медикаментозное лечение – только по рекомендации врача.
Обязателен контроль динамики роста и массы тела. Лучший помощник для мамы — высокоточные смарт-весы AGU Wally с мониторингом веса и роста ребенка в мобильном приложении, помогающие избежать и гипотрофии, и паратрофии.
Профилактика гипотрофии у детей включает качественное питание и лечение сопутствующих болезней.
Гипотрофия — ПроМедицина Уфа
Гипотрофия у детей
– хроническое нарушение питания, сопровождающееся недостаточным приростом массы тела ребенка по отношению к его росту и возрасту. Гипотрофия у детей выражается отставанием ребенка в весе, задержкой в росте, отставанием в психомоторном развитии, недоразвитием подкожно-жирового слоя, снижением тургора кожных покровов.
Гипотрофия у детей выражается отставанием ребенка в весе, задержкой в росте, отставанием в психомоторном развитии, недоразвитием подкожно-жирового слоя, снижением тургора кожных покровов.Причины
Причинами, ведущими к возникновению гипотрофии, служат как внутренние факторы, так и внешние. Принято различать первичную патологию, при которой существует недостаток питания, и вторичную – когда на фоне различных болезней, или других вредных факторов, питательные вещества из принимаемой пищи просто не усваиваются организмом. К внутренним факторам относят заболевания различных внутренних органов, участвующих в пищеварении, то есть питательные вещества, под влиянием каких-либо причин, не могут усваиваться организмом. Здесь, к примеру, уместно сказать, что нарушение может быть как на уровне желудочно-кишечного тракта, так и на тканевом и клеточном уровне. При этом возникают различные нарушения обмена в самой клетке. Клеточные запасы энергии постепенно уменьшаются. В случае их полного истощения начинается естественный процесс отмирания клеток.
Симптомы
Признаки и симптомы внутриутробной гипотрофии у ребенка: масса тела ниже нормы от 15% и более, рост меньше на 2-4 см, ребенок вялый, тонус мышц понижен, врожденные рефлексы слабые, терморегуляция нарушена — ребенок мерзнет или перегревается быстрее и сильнее, чем нормальный.
В дальнейшем первоначальный вес медленно восстанавливается, пупочная ранка плохо заживает.
Для приобретенной гипотрофии характерна недостаточная упитанность: ребенок худой, но пропорции тела не нарушены. Также отмечаются трофические расстройства (нарушение питания тканей организма): подкожно-жировой слой истончен (вначале на животе, затем на конечностях, при тяжелом течении и на лице), масса недостаточна, пропорции тела нарушены, кожа сухая, упругость снижена.
Отмечаются изменения работы нервной системы: угнетенное настроение, снижение тонуса мышц, ослабление рефлексов, психомоторное развитие задерживается, а при тяжелом течении даже исчезают приобретенные навыки.
Снижается восприятия пищи: аппетит ухудшается вплоть до полного его отсутствия, появляются частые срыгивания, рвота, нарушения стула, выделение пищеварительных ферментов угнетается. Снижение иммунитета: ребенок начинает часто болеть, развиваются хронические инфекционно-воспалительные заболевания, возможно токсическое и бактериальное поражение крови, организм страдает от общего дисбактериоза.
Снижение иммунитета: ребенок начинает часто болеть, развиваются хронические инфекционно-воспалительные заболевания, возможно токсическое и бактериальное поражение крови, организм страдает от общего дисбактериоза.
Диагностика и лечение
Если не обнаружены причины в режиме питания и инфекционных болезнях, ищут более редкие обмена веществ, энзимопатии. Отеки почти всегда связаны с недостатком белка в пище, а иногда – с потерей белка организмом.
В комнате, где большую часть дня находится ребенок с гипотрофией, нужно поддерживать температуру 24-27°С. Следует контролировать одежду ребенка при прогулках, а также время нахождения вне квартиры.
Следует уделять большое внимание гигиене гипотрофиков, потому что у них очень снижен иммунитет. После стула ребенка моют и обрабатывают кожу детским увлажняющим кремом. Тщательно выбирают одежду, обращая внимания на ее состав. К телу не должны прилегать грубые швы. Предпочтение отдают натуральным тканям. В иных случаях у ребенка может быть аллергия и раздражения на коже.
Создавайте ребенку каждый день позитивные эмоции. Чаще играйте с ними. Ребенок должен правильно, сбалансировано и регулярно питаться. Используйте для питания новорожденных материнское молоко или специальные смеси, которые адаптированы для больных деток и малышей с недовесом. Добавьте в рацион витамины и полезные вещества, которые необходимы организму грудничка.
причины, симптомы, диагностика, лечение, профилактика
Паталогическое состояние, обусловленное хроническим нарушением питания, что сопровождается недостаточным приростом массы тела ребенка по отношению к его росту и возрасту.
Хроническое нарушение питания может возникать на фоне различных факторов, которые воздействуют в пренатальном или постнатальном периоде.
Внутриутробная гипотрофия у плода возникает в результате воздействия неблагоприятных условий, нарушающих нормальное развитие плода. В пренатальном периоде развитие гипотрофии плода и новорожденного могут вызывать патология беременности, соматические заболевания женщины, стрессы, вредные привычки, нарушение питания женщины, производственные и экологические вредности, внутриутробное инфицирование и гипоксия плода.
Развитие внеутробной гипотрофии у детей раннего возраста может возникать на фоне эндогенных и экзогенных факторов. К эндогенным причинам относят хромосомные аномалии и врожденные пороки развития, ферментопатии, снижение защитных сил организма, аномалии конституции.
Все экзогенные факторы, приводящие к гипотрофии у детей, делятся на алиментарные, инфекционные и социальные. Алиментарные факторы обусловлены развитием белково-энергетических дефицитов, возникающих на фоне недостаточного или несбалансированного питания. Возникновение гипотрофии у ребенка может возникать на фоне систематического недокармливания, связанного с затруднением сосания при неправильной форме сосков у матери, гипогалактией, недостаточным количеством молочной смеси, частыми и обильными срыгиваниями, несбалансированным питанием ребенка и кормящей женщины. К этой же группе причин также относятся заболевания самого новорожденного, не позволяющие ему активно сосать и получать необходимое количество пищи, такие как расщелина губы и неба, врожденные пороки сердца, родовые травмы, перинатальные энцефалопатии, пилоростеноз, детский церебральный паралич и алкогольный синдром плода.
Возникновение гипотрофии у ребенка может возникать на фоне систематического недокармливания, связанного с затруднением сосания при неправильной форме сосков у матери, гипогалактией, недостаточным количеством молочной смеси, частыми и обильными срыгиваниями, несбалансированным питанием ребенка и кормящей женщины. К этой же группе причин также относятся заболевания самого новорожденного, не позволяющие ему активно сосать и получать необходимое количество пищи, такие как расщелина губы и неба, врожденные пороки сердца, родовые травмы, перинатальные энцефалопатии, пилоростеноз, детский церебральный паралич и алкогольный синдром плода.
К развитию приобретенной гипотрофии предрасположены дети, часто болеющие острыми респираторными инфекциями, кишечными инфекциями, воспалительным поражение легочной ткани или туберкулезом. Развитию гипотрофии у детей также способствуют неблагоприятные санитарно-гигиенические условия, обусловленные некачественным уходом за ребенком.
СимптомыПри гипотрофии первой степени состояние детей практически не нарушено, нервно-психическое развитие находится в пределах нормы, иногда у ребенка может определяться незначительное снижение аппетита.
Для гипотрофии II степени характерно нарушение активности ребенка и выраженное снижение аппетита. У ребенка выявляется бледность кожных покровов, а также их усиленное шелушение и дряблость. Определяется снижение мышечного тонуса, эластичности и упругости тканей. Кожа у малыша легко собирается в складки, которые плохо расправляются. На животе, конечностях и туловище исчезает подкожно-жировой слой, но при этом он сохраняется на лице. У ребенка может обнаруживается одышка, артериальная гипотония и тахикардия.
При гипотрофии III степени у ребенка выявляется резкое истощение, отмечается атрофия подкожно-жирового слоя на всем туловище и на лице. Ребенок адинамичен и фактически не реагирует на раздражители. Такие малыши резко отстают в росте и нервно-психическом развитии. Кожные покровы у ребенка имеют бледно-серый окрас, слизистые оболочки сухие и бледные, отмечается атрофия и отсутствие тургора мышц.
Чаще всего выявление внутриутробной гипотрофии плода, происходит при проведении ультразвукового исследования беременной. В процессе акушерского ультразвукового обследования может определяться размеры головки, длина и предполагаемая масса плода. При задержке внутриутробного развития плода акушер-гинеколог направляет беременную в стационар для выявления причин нарушения.
У новорожденных детей гипотрофии может определяться сразу после рождения. Для выявления нарушения применяют антропометрию, основанную на определении параметров физического развития: длины, массы, окружности головы, груди, плеча, живота, бедра, толщины кожно-жировых складок.
Лечение постнатальной гипотрофии основано на мероприятиях, которые включают устранение причин нарушения питания, диетотерапию, организацию правильного ухода, устранение метаболических нарушений.
Медикаментозная терапия основана на назначении ферментов, витаминов, адаптогенов, анаболических гормонов. При тяжелой степени гипотрофии может потребоваться внутривенное введение белковых гидролизатов, глюкозы, солевых растворов, витаминов.
ПрофилактикаПрофилактика развития пренатальной гипотрофии плода включает соблюдение режима дня и питания беременной и исключении влияния на плод различных неблагоприятных факторов.
Гипотрофия — Медкор
Гипотрофия первой степени
Первоначально недостаток питательных элементов организм пытается компенсировать накопленным подкожно-жировым слоем. Жиры из депо мигрируют в кровь, проходят через печень и превращаются в энергию для поддержания нормальной физиологической активности органов и систем. Первоначально жировые запасы исчезают в области живота, затем в других местах. Оценка степени истощения подкожно-жирового слоя производится разными методиками. Наиболее практичным, и вместе с тем информативным методом, считается индекс Чулицкой. В основе данного метода лежит измерение окружности плеча в двух разных местах, затем бедра и голени, а от получившейся суммы отнимают рост ребенка. Норма для ребенка до года равна 20-25 см. Другой способ представляет собой измерение кожной складки в четырех разных местах: на животе слева от пупка, на плече, в области лопаток, и наконец, на бедре с внешней стороны. При нормальном росте и развитии ребенка кожная складка равна приблизительно 2-2.5 см. При первой степени гипотрофии индекс Чулицкой равен 10-15 сантиметрам, а кожная складка незначительно уменьшается.
Наиболее практичным, и вместе с тем информативным методом, считается индекс Чулицкой. В основе данного метода лежит измерение окружности плеча в двух разных местах, затем бедра и голени, а от получившейся суммы отнимают рост ребенка. Норма для ребенка до года равна 20-25 см. Другой способ представляет собой измерение кожной складки в четырех разных местах: на животе слева от пупка, на плече, в области лопаток, и наконец, на бедре с внешней стороны. При нормальном росте и развитии ребенка кожная складка равна приблизительно 2-2.5 см. При первой степени гипотрофии индекс Чулицкой равен 10-15 сантиметрам, а кожная складка незначительно уменьшается.
Симптомы гипотрофии первой степени:
•Жировые складки дряблые, тонус мышц снижен, теряется эластичность и упругость кожи.
•Рост ребенка первоначально соответствует возрастным нормам.
•Масса тела снижена приблизительно от 11% до 20% от первоначальной.
•Общее самочувствие нормальное. Отмечается быстрое утомление.
Отмечается быстрое утомление.
•Нарушений со стороны центральной нервной системы нет. Сон тревожный, прерывистый.
•Ребенок немного раздражителен, может срыгивать съеденную пищу.
Гипотрофия второй степени
Изменения те же что, при первой степени, но отличие состоит в том, что они немного углубляются, а также появляются другие характерные симптомы:
Признаки гипотрофии второй степени:
•Подкожный жировой слой сильно истончается на ногах, руках, и может отсутствовать на животе или груди.
•Индекс Чулицкой снижается, и варьирует в пределах от одного до десяти сантиметров.
•Кожные покровы бледные, сухие.
•Кожа дряблая, легко сдвигается в складки.
•Волосы и ногти становятся ломкими.
•Снижается мышечная масса на конечностях, масса тела убывает приблизительно на двадцать – тридцать процентов, также отмечается отставание в росте.
•Нарушается терморегуляция, такие дети быстро замерзают, или также быстро перегреваются.
•Высок риск обострения хронических инфекций (пиелонефрит, отит, пневмония).
•Нарушение устойчивости по отношению к принимаемой пище.
В связи с трофическими нарушениями ворсинок и слизистой оболочки кишечника нарушается пищеварение, в частности всасывание питательных веществ. Появляется дисбактериоз, то есть преобладает патогенная бактериальная флора. У детей появляются: усиленное газообразование, вздутие и дискомфорт в области живота. Нередки запоры или поносы, часто сменяющиеся друг за другом.
•Снижается мышечный тонус. Из-за значительно сниженного тонуса мышц живот выпячивается наружу, и создается впечатление лягушачьего живота.
•Недостаток витамина Д и кальция в организме приводит к дополнительному развитию слабости мышц, развитию симптомов остеопороза (вымывание кальция из костей). При этом кости черепа становятся мягкими, большой и малый роднички остаются открытыми довольно длительное время.
При этом кости черепа становятся мягкими, большой и малый роднички остаются открытыми довольно длительное время.
•Со стороны центральной нервной системы также выявляется ряд патологических нарушений, сходных с таковыми при первой степени гипотрофии. Дети беспокойны, не могут уснуть, часто капризничают. Затем характерные симптомы перевозбуждения центральной нервной системы постепенно сменяются вялостью и апатией к окружающему миру.
Гипотрофия третьей степени Отражает всю полноту клинической картины заболевания. При данной степени максимально выражены нарушения работы всех органов и систем. Первичная причина заболевания обуславливает наиболее тяжелое состояние ребенка, малоэффективность предпринимаемых мер по выведению ребёнка из данного состояния, и его дальнейшее выздоровление. Третья степень гипотрофии характеризуется сильным истощением организма, снижением всех видов обмена веществ.
Характерные признаки и симптомы гипотрофии третьей степени:
•По внешнему виду можно сразу определить, что существует хронический недостаток питания. Подкожно-жировой слой отсутствует практически во всех местах, включая лицо. Кожные покровы сухие, бледные и настолько истончены, что ребенок выглядит, будто мумия.
Подкожно-жировой слой отсутствует практически во всех местах, включая лицо. Кожные покровы сухие, бледные и настолько истончены, что ребенок выглядит, будто мумия.
•При попытке образовать пальцами кожную складку практически отсутствует сопротивление здоровой кожи. Эластичность кожи настолько снижена, что складка не расправляется в течение длительного времени после отпускания пальцев. По всему телу образуются глубокие морщины.
•Мышечная масса и масса тела в целом настолько малы, что индекс упитанности по Чулицкой не определяется, либо отрицательный. Общее снижение массы тела составляет 30% и более от нормальных показателей.
•На лице видно западение щек, скулы выпячиваются вперед, выражено заострение подбородка.
•Четко выражены проявления нехватки жизненно важных микроэлементов и витаминов.
•Нехватка железа сказывается на появлении трещин в углах рта (заеды), а также анемии.
•Недостаток витаминов А и С проявляется в виде появления на слизистых оболочках: кровоточивости и атрофии (отмирание, уменьшение в размерах) десен, стоматита в виде мелких белесоватых высыпаний.
•Живот сильно растянут за счет слабости мышц, поддерживающих его.
•Температура тела часто скачет вверх вниз за счет того, что не работает центр терморегуляции в головном мозге.
•Резко снижен иммунитет. Можно обнаружить признаки вялотекущих хронических инфекций. Воспаление среднего уха – отит, воспаление почек – пиелонефрит, воспаление легких – пневмония.
•У ребенка рост отстает от среднестатистических показателей.
Варианты течения гипотрофии
Отставание в росте и развитии ребенка может присутствовать на каждом этапе его развития, начиная преимущественно со второй половины беременности, и заканчивая периодом младшего школьного возраста. При этом проявления заболевания характеризуются своими особенностями. В зависимости от периода развития гипотрофических проявлений, различают четыре варианта течения гипотрофии:
При этом проявления заболевания характеризуются своими особенностями. В зависимости от периода развития гипотрофических проявлений, различают четыре варианта течения гипотрофии:
•внутриутробная гипотрофия;
•гипостатура;
•квашиоркор;
•алиментарный маразм.
Внутриутробная гипотрофия
Внутриутробная гипотрофия берет свое начало еще во внутриутробном периоде. Некоторые авторы называют данную патологию внутриутробной задержкой развития плода. Существует несколько вариантов развития внутриутробной гипотрофии:
1. Гипотрофический – когда нарушается питание всех органов и систем, плод развивается очень медленно, и не соответствует сроку беременности.
2. Гипопластический – этот вариант развития означает, что наряду с недостаточным общим развитием организма плода, существует и некоторое отставание в созревании и развитии всех органов. Здесь идет речь о том, что органы и ткани при рождении недостаточно сформированы, и не полностью выполняют свои функции.
Здесь идет речь о том, что органы и ткани при рождении недостаточно сформированы, и не полностью выполняют свои функции.
3. Диспластический вариант течения гипотрофии характеризуется неравномерным развитием отдельных органов. Одни, например сердце, печень – развиваются нормально, соответствуя сроку беременности, а другие – наоборот, отстают в своем развитии, или развиваются несимметрично.
Гипостатура Гипостатура – термин берет свое начало из греческого языка, и означает hypo – ниже, или под, statura – рост, или величина. При этом варианте развития гипотрофии существует равномерное отставание как в росте ребенка, так и в его массе тела. Единственное отличие от истинной гипотрофии заключается в том, что кожные покровы и подкожно-жировой слой не подвергаются сильным изменениям. Гипостатура, как один из вариантов течения гипотрофии, возникает вторично при хронических заболеваниях некоторых внутренних органов. Развитие гипостатуры обычно связано с переходными периодами роста и развития ребенка. Один из таких периодов приходится на первое полугодие жизни ребенка. При этом к материнскому молоку начинают понемногу добавлять продукты питания, молочные смеси – другими словами, докармливать ребенка. Появление данной патологии на втором году жизни связано, прежде всего, с врожденными хроническими заболеваниями. Вот часто встречающиеся из них:
Один из таких периодов приходится на первое полугодие жизни ребенка. При этом к материнскому молоку начинают понемногу добавлять продукты питания, молочные смеси – другими словами, докармливать ребенка. Появление данной патологии на втором году жизни связано, прежде всего, с врожденными хроническими заболеваниями. Вот часто встречающиеся из них:
•Врожденные пороки сердечнососудистой системы. Нарушение кровообращения ведет к недостаточному притоку кислорода и питательных веществ к органам и тканям.
•Энцефалопатии в сочетании с эндокринными расстройствами также крайне неблагоприятно влияют на обмен веществ в организме, задерживая развитие и рост.
•Бронхолегочная дисплазия – это нарушенное развитие легочной ткани еще в период внутриутробного развития плода. При этом возникают серьезные осложнения, связанные с дыханием и доставкой кислорода в кровь.
Как уже было сказано выше, дети с гипостатурой преимущественно отстают в росте. Было доказано, что устранение причины, вызвавшей данную патологию, постепенно приводит к нормализации роста таких детей. Квашиоркор Термином квашиоркор принято называть такой вариант течения гипотрофии, который встречается в странах с тропическим климатом, и где в питании преобладает растительная пища. Кроме того существуют специфические нарушения, при которых организм недополучает, не синтезирует или вовсе не усваивает белковую пищу. К нарушениям, способствующим развитию квашиоркора, относятся:
Было доказано, что устранение причины, вызвавшей данную патологию, постепенно приводит к нормализации роста таких детей. Квашиоркор Термином квашиоркор принято называть такой вариант течения гипотрофии, который встречается в странах с тропическим климатом, и где в питании преобладает растительная пища. Кроме того существуют специфические нарушения, при которых организм недополучает, не синтезирует или вовсе не усваивает белковую пищу. К нарушениям, способствующим развитию квашиоркора, относятся:
•Длительное нарушение пищеварения, проявляющееся постоянным неустойчивым стулом – другими словами, у ребенка хроническая диарея.
•При заболеваниях печени нарушается ее белковообразовательная функция.
•Заболевания почек, сопровождающиеся повышенной потерей белка вместе с мочой.
•Ожоги, чрезмерные кровопотери, инфекционные заболевания.
Недостаточное потребление белковых продуктов (мясо, яйца, молочные) приводит к своеобразному течению данной патологии, выражающемуся в четырех основных и постоянных симптомах:
1. Нервно-психические расстройства – ребенок апатичен, вял, у него наблюдается повышенная сонливость, отсутствие аппетита. При обследовании таких детей часто можно выявить отставание в психомоторном развитии (поздно начинает держать головку, сидеть, ходить, речь формируется с большим опозданием).
Нервно-психические расстройства – ребенок апатичен, вял, у него наблюдается повышенная сонливость, отсутствие аппетита. При обследовании таких детей часто можно выявить отставание в психомоторном развитии (поздно начинает держать головку, сидеть, ходить, речь формируется с большим опозданием).
2. Отёки обусловлены недостатком белковых молекул в крови (альбуминов, глобулинов и др.). Альбумины поддерживают онкотическое давление в крови, привязывая к себе молекулы воды. Как только возникает белковая недостаточность, вода сразу покидает сосудистое русло и проникает в межтканевое пространство – образуется местная отечность тканей. В начальных стадиях болезни отекают преимущественно внутренние органы, но этот факт ускользает от внимания родителей. В развернутых (манифестных) стадиях болезни отекают периферические ткани. Отеки появляются на лице, стопах, конечностях. Создается ошибочное представление, что ребенок здоров и упитан.
3. Cнижение мышечной массы. Мышечная масса, а вместе с ней сила, значительно уменьшаются. Белковое голодание приводит к тому, что организм заимствует собственные белки из мышц. Происходит так называемая атрофия мышечных волокон. Мышцы становятся дряблыми, вялыми. Вместе с мышцами нарушается питание подлежащих тканей и подкожно-жировой клетчатки.
Мышечная масса, а вместе с ней сила, значительно уменьшаются. Белковое голодание приводит к тому, что организм заимствует собственные белки из мышц. Происходит так называемая атрофия мышечных волокон. Мышцы становятся дряблыми, вялыми. Вместе с мышцами нарушается питание подлежащих тканей и подкожно-жировой клетчатки.
4. Опоздание в физическом развитии детей. Сопровождается недостаточностью ростового показателя, в то время как масса тела снижена намного меньше. Дети при квашиоркоре низкого роста, приземисты, двигательная активность находится ниже нормы. Кроме постоянных симптомов, у детей, страдающих квашиоркором, присутствуют другие признаки заболевания, встречающиеся с различной частотой. Частыми симптомами считаются:
1. Изменение цвета, смягчение истончение и, в конце концов, выпадение волос на голове. Волосы становятся светлее, а в более поздних проявлениях болезни, или у детей старшего возраста, обнаруживаются обесцвеченные, или вовсе седые пряди волос.
2. Дерматит – воспаление поверхностных слоев кожных покровов. На коже проявляются покраснение, зуд, трещины. В последующем кожа на пораженных участках отшелушивается, и на этом месте остаются следы в виде светлых пятен. К редким симптомам относят:
1. Дерматоз – красно-коричневые пятна округлой формы.
2. Гепатомегалия – патологическое увеличение печени. Печеночная ткань замещается жировой и соединительной тканью. Печень не способна образовывать ферменты и другие активные вещества, необходимые для нормальной функции всего организма.
3. Нарушения функции почек. Снижается фильтрационная способность. В крови накапливаются вредные продукты обмена веществ.
4. Нарушения стула носит постоянный характер. У ребенка присутствует постоянный понос. Каловые массы блестят и неприятно пахнут.
Подытоживая изложенный материал, с уверенностью можно сказать, что квашиоркор – это заболевание, исключительно редко встречающееся в странах с умеренным климатом. Страны, расположенные в данной географической широте, имеют развитый социальный статус и уровень жизни, поэтому практически исключается возможность недоедания и дефицита в питании белков и калорий.
Страны, расположенные в данной географической широте, имеют развитый социальный статус и уровень жизни, поэтому практически исключается возможность недоедания и дефицита в питании белков и калорий.
Алиментарный маразм
Алиментарный маразм (истощение) встречается у детей младшего и старшего школьного возраста. При маразме присутствует недостаток как белков, так и калорий. Чтобы установить причину и поставить точный диагноз, выясняют: •Из истории начала заболевания узнают, какова была масса тела ребенка еще до того, как появились первые признаки гипотрофии.
•Социально-экономическое положение, в котором находится семья ребенка.
•По возможности выяснить суточный рацион.
•Есть ли рвота или хроническая диарея, и насколько часто возникает.
•Принимает ли данный ребенок какие-либо лекарственные средства. Например, анорексигенные, которые подавляют аппетит, или мочегонные средства, выводящие из организма много полезных питательных веществ, в том числе белок.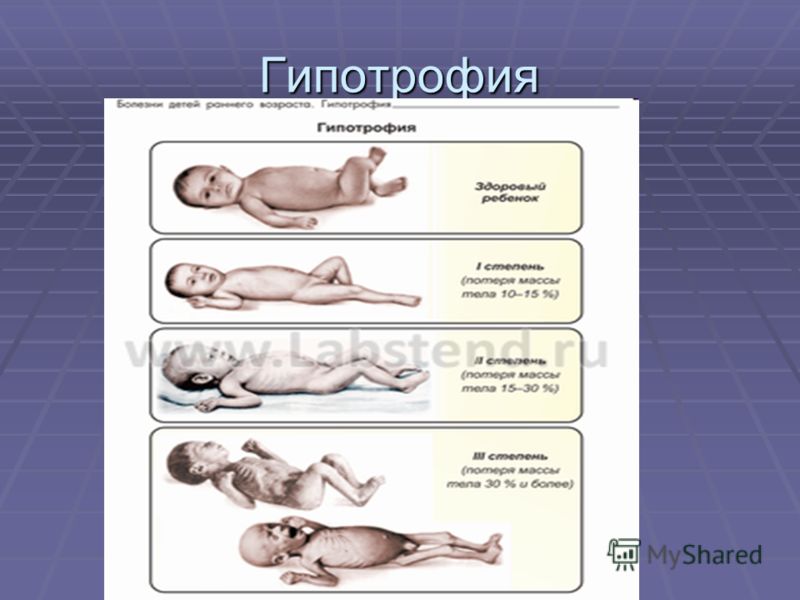 •Есть ли нарушения со стороны центральной нервной системы: стрессовые ситуации, алкогольная или наркотическая зависимость.
•Есть ли нарушения со стороны центральной нервной системы: стрессовые ситуации, алкогольная или наркотическая зависимость.
•В подростковом возрасте, в частности у девочек, начиная с 12 лет, выясняют наличие и оценивают регулярность, периодичность и длительность менструального цикла. Все вышеперечисленные факторы прямым или косвенным путем отражаются на состоянии организма, влияют на все органы и системы, угнетая их функциональную работоспособность. Тем самым предрасполагают к развитию алиментарного маразма. Среди всех симптомов, появляющихся при алиментарном маразме, выделяют постоянные и редкие симптомы.
К постоянным симптомам относят:
•потеря массы тела достигает до 60% от нормальной, соответствующей возрасту;
•уменьшение толщины подкожно-жирового слоя;
•уменьшение массы мышечных волокон;
•конечности больного становятся очень тонкими;
•на лице появляются множество морщин, кожа обтягивает все лицевые кости и, кажется, будто это лицо старика. Редкими симптомами считаются:
Редкими симптомами считаются:
•Диарея, носит хронический характер. Стул жидкий, блестит, с неприятным запахом.
•Истончение и просветление волос, которые со временем начинают выпадать.
•Обострение хронических инфекций – очень частый спутник ослабленного недоеданием организма.
•Молочница – грибковое заболевание, при котором поражаются слизистые оболочки полости рта, влагалища и мочеиспускательного канала. Проявляются выделениями белесоватого цвета, зудом и дискомфортом в указанных местах. •Симптомы поливитаминной недостаточности, в зависимости от нехватки определенных витаминов и минералов. При объективном обследовании у таких детей обнаруживается множество патологических изменений среди всех органов и систем:
•Глазные изменения проявляются воспалением век, образованием новых мелких сосудов на роговой оболочке. Во внутренних углах глаз появляются бляшки сероватого цвета (недостаток витамина А).
•В ротовой полости наблюдаются воспалительные изменения слизистой оболочки и десен. Язык увеличивается в размерах (из-за нехватки витамина В12).
•Сердце увеличивается в размерах. Недостаточная сила сердечных толчков приводит к застаиванию крови в венах, появляется отечность нижних конечностей.
•Слабость мышц передней брюшной стенки обуславливает отвислый, выступающий живот. Печень выступает за нижний край правого подреберья.
•Явные неврологические нарушения проявляются в нервозности, повышенной раздражительности, мышечной слабости, в снижении сухожильных рефлексов. Функциональные изменения отражают степень патологических нарушений, связанных с белково-калорийной недостаточностью:
•Ухудшается память, снижаются умственно-познавательные способности, в том числе работоспособность. •Падает острота зрения. Недостаток витамина А обуславливает снижение зрения в сумеречное время.
•Острота вкусовых ощущений также снижена.
•Недостаток витамина С приводит к повышенной ломкости капилляров. На коже можно заметить мелкоточечные кровоизлияния после легкого щипка. Нехватка незаменимых жирных кислот Если присутствует дефицит незаменимых жирных кислот (линолевая и линоленовая кислоты), незамедлительно появляются специфические симптомы, характерные при недостаточном их потреблении. Линоленовая и линолевые кислоты в большом количестве содержатся в растительных маслах (оливковое, подсолнечное, соевое). В большинстве случаев данный вариант гипотрофии появляется у детей грудного возраста, которым недостает в питании материнского молока. Коровье молоко и другие молочные смеси не содержат незаменимые жирные кислоты количестве, необходимом для энергетических и пластических затрат молодого организма. В зависимости от недостаточности той или иной жирной кислоты, симптомы заболевания будут немного отличаться друг от друга. При недостатке линолевой кислоты появляются следующие симптомы:
•Сухость кожных покровов с отшелушиванием поверхностного рогового слоя.
•Алопеция (облысение).
•Заживление ран продолжается длительный период.
•Тромбоцитопения – пониженное количество тромбоцитов (клетки крови, отвечающие за ее свертываемость) в крови. Недостаток тромбоцитов приводит к повышенной ломкости мелких сосудов, при случайных мелких бытовых повреждениях кожных покровов кровотечение удлиняется. Незначительные щипки вызывают появление множества мелкоточечных кровоизлияний.
•Длительный неустойчивый стул (диарея).
•Периодические обострения инфекционных заболеваний (к примеру, кожи или легких).
Недостаток линоленовой кислоты приводит к: •онемению и парестезии (чувство покалывания) нижних и верхних конечностей;
•общей мышечной слабости;
•нарушению четкости зрения.
В целом, тяжесть патологических изменений и отставание массы тела от роста зависят от множества причин, в том числе от длительности белкового и калорийного голодания юношей и девушек. Поэтому своевременное выяснение причин приводящих к развитию алиментарного маразма может предотвратить все патологические последствия. Диагностика гипотрофии Основные положения Подходя к этапу диагностирования гипотрофии, вариантов течения, возможных осложнений со стороны других органов – необходимо учитывать несколько моментов. Обнаружение важных клинических признаков по всем основным системам, вовлеченным в патологический процесс. Сюда включают следующие нарушения: •нарушения упитанности – проявляются в виде истончения подкожно-жирового слоя и трофических изменений; •нарушения пищеварительной функции – включают изменение устойчивости к пище;
Поэтому своевременное выяснение причин приводящих к развитию алиментарного маразма может предотвратить все патологические последствия. Диагностика гипотрофии Основные положения Подходя к этапу диагностирования гипотрофии, вариантов течения, возможных осложнений со стороны других органов – необходимо учитывать несколько моментов. Обнаружение важных клинических признаков по всем основным системам, вовлеченным в патологический процесс. Сюда включают следующие нарушения: •нарушения упитанности – проявляются в виде истончения подкожно-жирового слоя и трофических изменений; •нарушения пищеварительной функции – включают изменение устойчивости к пище;
•нарушения обмена веществ: белкового, жирового, углеводного, минерального, витаминного;
•функциональные нарушения со стороны центральной нервной системы.
Важным, и основным критерием для диагностирования данной патологии, является размер подкожного жирового слоя. Чем тоньше этот слой, тем более выражено нарушение общего состояния организма.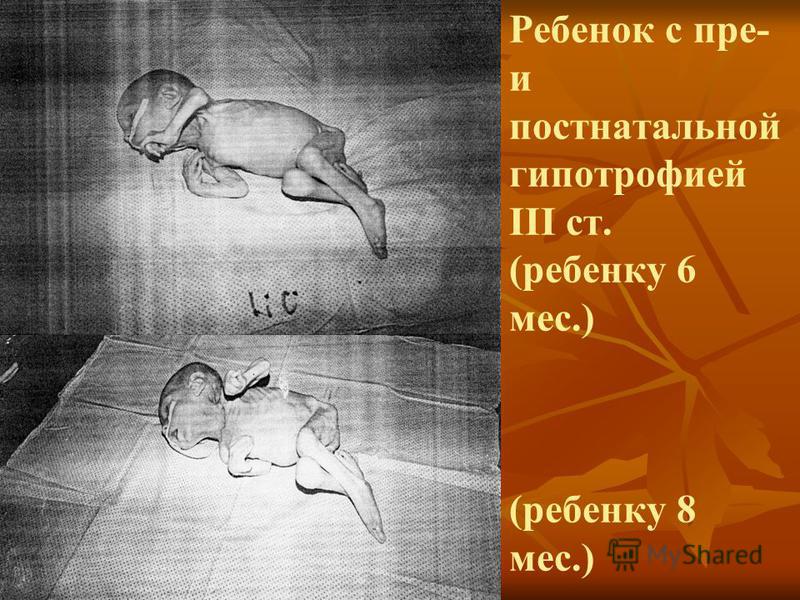 Вторым моментом, который не должен ускользать от внимания врачей, является дифференцировка патологических изменений, происходящих при гипотрофии, с другими похожими заболеваниями, со снижением роста, массы тела, и общего физического развития детей. Симптомы детей с гипостатурой очень схожи с таким заболеванием, как нанизм. Это патология центральных эндокринных органов (гипоталамуса и гипофиза), при которой не вырабатывается гормон роста – соматотропин. При данном заболевании, в отличие от гипостатуры, нет патологических изменений в виде истончения подкожного жирового слоя и других трофических нарушений. Все органы развиваются равномерно, хотя и уменьшены в размере. Оценка состояния ребенка и определение степени патологических изменений определяется также по характеру каловых масс. Первоначально при гипотрофии стул скудный, без цвета, с характерным зловонным запахом. В дальнейшем нарушения функциональной способности перерабатывать пищу желудочно-кишечным трактом приводят к тому, что стул становится обильным, блестит, в нем присутствуют остатки непереваренной пищи, мышечных волокон.
Вторым моментом, который не должен ускользать от внимания врачей, является дифференцировка патологических изменений, происходящих при гипотрофии, с другими похожими заболеваниями, со снижением роста, массы тела, и общего физического развития детей. Симптомы детей с гипостатурой очень схожи с таким заболеванием, как нанизм. Это патология центральных эндокринных органов (гипоталамуса и гипофиза), при которой не вырабатывается гормон роста – соматотропин. При данном заболевании, в отличие от гипостатуры, нет патологических изменений в виде истончения подкожного жирового слоя и других трофических нарушений. Все органы развиваются равномерно, хотя и уменьшены в размере. Оценка состояния ребенка и определение степени патологических изменений определяется также по характеру каловых масс. Первоначально при гипотрофии стул скудный, без цвета, с характерным зловонным запахом. В дальнейшем нарушения функциональной способности перерабатывать пищу желудочно-кишечным трактом приводят к тому, что стул становится обильным, блестит, в нем присутствуют остатки непереваренной пищи, мышечных волокон. Инфицирование патогенными бактериями слизистой оболочки кишечника влечет за собой явления дисбактериоза (диарея, вздутие и дискомфорт в области живота). Вследствие недостаточного поступления белка, организм использует внутренние резервы (из мышц, жировой ткани), продукты обмена которых в виде аммиака выводятся почками. Моча таких больных имеет запах аммиака. Лабораторные исследования Ввиду того, что при гипотрофии присутствует многообразие патологических изменений, лабораторные анализы будут вариабельны, в зависимости от преимущественного поражения того или иного органа. К примеру, при анемии будет снижение числа эритроцитов и гемоглобина в кровяном русле. В биохимических анализах можно обнаружить признаки нарушения работы печени, недостаток витаминов и микроэлементов.
Инфицирование патогенными бактериями слизистой оболочки кишечника влечет за собой явления дисбактериоза (диарея, вздутие и дискомфорт в области живота). Вследствие недостаточного поступления белка, организм использует внутренние резервы (из мышц, жировой ткани), продукты обмена которых в виде аммиака выводятся почками. Моча таких больных имеет запах аммиака. Лабораторные исследования Ввиду того, что при гипотрофии присутствует многообразие патологических изменений, лабораторные анализы будут вариабельны, в зависимости от преимущественного поражения того или иного органа. К примеру, при анемии будет снижение числа эритроцитов и гемоглобина в кровяном русле. В биохимических анализах можно обнаружить признаки нарушения работы печени, недостаток витаминов и микроэлементов.
запускать нельзя! » Кузбасс главное
Нередко у малышей отмечается недостаточная для их возраста и роста прибавка веса. Хроническое недостающее до нормы на 10 процентов и более прибавление массы тела у ребенка называют гипотрофией. Это патологически нарушенное питание является самостоятельным заболеванием – разновидностью дистрофии. Чаще оно наблюдается у детей первых трех лет жизни, вызывает серьезные изменения в организме, поэтому так важно вовремя выявить его и лечить.
Это патологически нарушенное питание является самостоятельным заболеванием – разновидностью дистрофии. Чаще оно наблюдается у детей первых трех лет жизни, вызывает серьезные изменения в организме, поэтому так важно вовремя выявить его и лечить.
Разобраться в этом вопросе нам поможет Наталья Жданова, врач-детский эндокринолог детской поликлиники Областной клинической больницы.
– Наталья Александровна, какую опасность таит в себе недостаточная прибавка веса у ребенка?
– Это не просто отставание в весе тела. Гипотрофия приводит к отставанию в психическом развитии, речевом. А прогрессирующая гипотрофия приводит к истощению и представляет угрозу для жизни малыша.
Вот как бывает. Родителей маленьких детей гораздо чаще, чем ожирение, тревожат недостаточные прибавки массы тела. В подростковом же возрасте поводом для обращения к врачу, как правило, становится избыточный вес, поэтому на снижение массы тела чаще обращает внимание врач.
Для взрослых патологическим считается снижение массы тела на 5% и более в течение шести месяцев, если это снижение не было умышленным. У детей низкой массой тела по росту является ее величина меньше 3-го перцентиля (по спецтаблицам массы тела).
– Есть какие-то градации у болезни?
– Конечно. Различают три степени гипотрофии.
Первая степень характеризуется истончением подкожно-жирового слоя на всех участках тела, в первую очередь на животе. Дефицит массы тела по росту составляет 11-20 процентов, жировая складка дряблая, тургор тканей, тонус мышц и эластичность кожи снижены. У детей отмечается повышенная раздражительность, легкая утомляемость, нарушение сна. У этих ребятишек может снижаться скорость роста, может быть задержка пубертата. У девочек пубертатного возраста возможна первичная аменорея, или нарушение менструального цикла.
Вторая степень – это дефицит массы тела 20-30 процентов, подкожно-жировой слой отсутствует на животе и груди, истончен на конечностях, у маленьких детей сохранен на лице. Кожа бледная, сухая, дряблая, шелушащаяся. Волосы и ногти – сухие и ломкие, слизистые яркие, а в углах рта – заеды. Живот нередко увеличен, обычно бывают запоры. Характерны слабость и раздражительность, зябкость, снижение внимания, работоспособности, плаксивость. Скорость роста снижена. В подростковом периоде половое созревание не наступает.
Кожа бледная, сухая, дряблая, шелушащаяся. Волосы и ногти – сухие и ломкие, слизистые яркие, а в углах рта – заеды. Живот нередко увеличен, обычно бывают запоры. Характерны слабость и раздражительность, зябкость, снижение внимания, работоспособности, плаксивость. Скорость роста снижена. В подростковом периоде половое созревание не наступает.
А третья степень уже характеризуется крайней степенью истощения с дефицитом массы тела более 30 процентов, отсутствием подкожной клетчатки, прекращением роста. Кожа сухая, грубая, бледно-серого цвета, пигментированная, холодная. Бывает стоматит, выпадение волос, ломкость ногтей, запоры.
– Почему ребенок может терять вес?
– Похудание возникает или в результате недостаточного потребления (усвоения) пищи, или в результате чрезвычайных энергетических потерь. Аппетит больного может быть повышенным, нормальным или сниженным. При диагностике заболеваний, которые сопровождаются снижением массы тела, врач учитывает не только степень ее снижения, но и период времени, за который это произошло.
Причинами низкого веса у детей могут быть многочисленные заболевания, в том числе эндокринные, такие как сахарный диабет, гипертиреоз, феохромацитома, недостаточность надпочечников. В раннем детском возрасте (на первом году жизни) к низким прибавкам веса ребенка приводит гипогалактия у матери, затруднение вскармливания со стороны ребенка или матери, не соответствующее возрасту питание. Такие проблемы легко решаются с врачом-педиатром. Поэтому после рождения ребенка очень важны ежемесячные консультации педиатра для контроля веса и роста ребенка. А недоношенные дети или дети, рожденные с внутриутробной задержкой развития, должны наблюдаться еще чаще. Лучше всего иметь дома весы и взвешивать младенца ежедневно.
А еще снижение массы тела может быть одним из симптомов таких заболеваний, как муковисцидоз, целиакия, хронический гастрит, энтерит, язвенная болезнь, хронический гепатит, цирроз печени. Поэтому при жалобах на снижение веса необходима консультация врача-гастроэнтеролога.
К снижению аппетита (и как следствие – к снижению веса) ведут такие заболевания, как злокачественные опухоли, хронические инфекционные заболевания (например, туберкулез), невроз, депрессия, наркомания, алкоголизм.
– А нервная анорексия имеет отношение к этому заболеванию?
– Да. Нервная анорексия – это расстройство приема пищи, характеризующееся значительно сниженным весом тела, преднамеренно вызываемым самим пациентом в целях похудения или для профилактики набора лишнего веса. И она развивается чаще у девочек – подростков и молодых женщин. В начальном периоде заболевания формируется недовольство своей внешностью и стремление к коррекции фигуры. Второй период характеризуется сознательным отказом от еды, но аппетит сохранен. Многие используют повышенные физические нагрузки, вызывают рвоту, принимают мочегонные и слабительные средства. В результате происходит потеря 25-50 процентов массы тела. И развиваются эндокринные и соматические нарушения. Первым признаком нарушения эндокринной системы обычно становится аменорея, гирсутизм, снижение сахара крови.
– Какие еще заболевания могут возникать на фоне потери веса?
– Со снижения массы тела может начинаться даже сахарный диабет. Помимо потери веса на фоне повышенного аппетита у ребенка разовьется выраженная жажда, полиурия (частые мочеиспускания), появится слабость. При данных симптомах следует помнить о необходимости незамедлительного измерения сахара в крови! Только в этом случае вы сможете избежать такого грозного и смертельно опасного состояния как кетоацидоз.
Еще одно эндокринное заболевание – диффузно-токсический зоб (или Базедова болезнь) протекает с потерей массы тела. Для этой болезни также характерно повышенное сердцебиение, потливость, дрожь в теле, чувство жара. Потеря массы тела обусловлена усилением распада жировой ткани при повышенном уровне тиреоидных гормонов.
В общем, самое главное – при снижении веса ребенка необходимо незамедлительно обратиться к врачу с целью выяснения причины потери веса!
К слову, в Кемеровском областном клиническом перинатальном центре ведут прием врачи разных специальностей: педиатр, гастроэнтеролог, эндокринолог, кардиолог, пульмонолог, невролог, окулист, иммунолог, хирург, уролог, психолог. Записаться на прием можно по телефону 39-00-25. Направление не требуется. С собой нужно иметь полис и амбулаторную карту.
Записаться на прием можно по телефону 39-00-25. Направление не требуется. С собой нужно иметь полис и амбулаторную карту.
Дальнозоркость у детей: причины, симптомы, степени
Дальнозоркость или по-научному гиперметропия – это дефект зрительного восприятия, во время которого снижается видимость предметов, расположенных и вблизи, и вдали. Дальнозоркость присутствует у всех новорожденных детей, что обусловлено физиологическими особенностями оптической системы глаз и является вариантом нормы.
Но в некоторых случаях патология сохраняется и в дальнейшем, возникают дополнительные симптомы в виде жжения и быстрого утомления глаз, головных болей, снижения зрения, косоглазия.
Гиперметропия достаточно опасное заболевание, ведь заметить скрытые симптомы могут только очень внимательные родители, а поставить окончательный диагноз исключительно врач-офтальмолог. Своевременно начатое лечение у детей позволяет в дальнейшем навсегда избавиться от патологии.
Своевременно начатое лечение у детей позволяет в дальнейшем навсегда избавиться от патологии.
Норма и патология при гиперметропии
Гиперметропия в норме присутствует у детей раннего возраста (1-3 года), не вызывает беспокойства и не требует лечения. В период развития между младенчеством и школьным возрастом (до 6-7 лет) идет активный рост, увеличивается масса тела ребенка, развиваются внутренние органы и системы. Особенно активное развитие происходит в зрительной системе – вырабатывается точное соотношение функциональности разных частей глазного яблока.
У детей к четырем годам данный дефект зрительного восприятия проходит. Специалисты считают, что обнаружить заболевание и отличить его от нормы можно уже с первых месяцев жизни. При выявлении дальнозоркости у детей больше возрастных нормальных значение требует проведения лечения.
Очень важно начать терапию сразу после постановки диагноза, так как дети школьного возраста подвергаются усиленной нагрузке на глаза. В дальнейшем, при отсутствии коррекции глаз, симптомы гиперметропии усиливаются.
В дальнейшем, при отсутствии коррекции глаз, симптомы гиперметропии усиливаются.
Особенности гиперметропии
При детской дальнозоркости расстройство зрительного анализатора характеризуется фокусировкой изображения не на зрительной части сетчатки, а за ее пределами. Симптомы проявляются невозможностью различать объекты, находящиеся вблизи, но которые ребенок отлично различает на далеком расстоянии. Так, малыши с данным дефектом не могут сосредоточиться на игрушке, которая находится рядом возле них.
Четкость зрения, видимость предметов вдали и вблизи обеспечивает аккомодационный аппарат. Фокусировка изображения на сетчатке происходит благодаря изменению кривизны хрусталика, за которую отвечает ресничная мышца (цилиарная). Чтобы хорошо видеть объекты на близком расстоянии цилиарная мышца напрягается, а хрусталик становится более выпуклым и преломление света происходит сильнее. Для дальнего зрения хрусталик становится плоским благодаря расслаблению цилиарной мышцы. Таким образом, для хорошего рассмотрения предметов на разном расстоянии кривизна хрусталика постоянно изменяется. Показатель преломления хрусталика измеряют в диоптриях.
Показатель преломления хрусталика измеряют в диоптриях.
У детей с рождения глаз характеризуется гиперметропией, которая постепенно уменьшается с ростом глаза и исчезает полностью к 7 годам. Данное состояние у младенцев считается нормой и характеризуется не полностью сформировавшимся зрительным анализатором.
Классификация дальнозоркости
Степени тяжести гиперметропии у детей:
- Слабая стадия дальнозоркости характеризуется показателями до 2 дптр включительно – у детей отсутствуют симптомы за счет компенсации аккомодационных способностей зрительного органа. Первая стадия болезни обнаруживается при профилактических осмотрах, хорошо поддается коррекции с помощью специальных упражнений для глаз.
- Средняя степень патологии (от 2.25 до 5 дптр) – ребенок плохо видит вблизи, но может хорошо различать дальние объекты.
- Высокая степень нарушений (5.25 дптр и выше) – зрение значительно снижается, как вблизи, так и вдали.
Этиологические факторы развития детской дальнозоркости
Причинами развития дальнозоркости в детском возрасте являются:
- генетические факторы;пороки развития зрительной системы, неправильная закладка структур глаза;
- нарушение внутриутробного роста плода;
- травматическое повреждение глаз химическими соединениями или физическими факторами;
- состояния после инфекционных процессов;
- операции на зрительном органе;
- повышенное перенапряжение, утомляемость глаз;
- неправильно подобранные очки или контактные линзы.

Клиническая картина гиперметропии
При слабой степени дальнозоркости симптомы со стороны нарушения зрительной функции отсутствуют. Поэтому в данном периоде важно наблюдение родителей за изменившимся поведением ребенка. Признаки гиперметропии на ранних стадиях болезни, проявляются:
- учащенным морганием;
- капризностью и раздражительностью;
- постоянно возникающими головными болями, головокружением;
- невозможностью сконцентрироваться на игрушках и любых других предметах, расположенных близко или находящихся в руках;
- повышенная усталость глаз без видимых причин;
- нарушение сна;
- воспаление глазного яблока, гиперемия, сухость;
- повышенное слезотечение.
Средняя стадия болезни чаще диагностируется у детей при профилактических осмотрах офтальмолога в школьном возрасте. Выше описанная картина может проявляться более яркими симптомами. Основными проявлениями средней степени дальнозоркости являются плохая видимость предметов на близком расстоянии, их расплывчатость. Ребенок испытывает затрудения при чтении, письме. Таким пациентам ошибочно ставят диагнозы дисграфия, дислексия, задержка развития.
Ребенок испытывает затрудения при чтении, письме. Таким пациентам ошибочно ставят диагнозы дисграфия, дислексия, задержка развития.
При высокой степени гиперметропии ребенок жалуется на плохую видимость ближних предметов и дальних объектов.
При гиперметропии часто развивается сходящееся косоглазие, имеются нарушения бинокулярного зрения.
Диагностические мероприятия
Пройдите полное обследование зрения
в глазной клинике «Леге Артис»
Пора исправить зрение!
Запись на прием по телефону:
Диагностика гиперметропии у детей проводится врачом-офтальмологом. Проверка остроты зрения проводится разными методами, в зависимости от возраста ребенка. Также перед началом исследования в глаз закапывают капли для расширения зрачка. Это приводит к расслаблению цилиарной мышцы и позволяет правильно измерить светопреломляющую способность глаза. Для своевременного выявления дальнозоркости рекомендуется посещать детского офтальмолога не реже 1 раз в год.
Диагностика состоит из сбора анамнеза, родители дают полную информацию о поведении ребенка и присутствующих жалобах: ребенок с проблемами зрительного восприятия быстро утомляется, становится замкнутым, у него преобладает плохое настроение, для детей школьного возраста характерно медленное чтение, но яркие картинки на расстоянии (билборды, плакаты) они рассматривают с высоким интересом.
Для выявления дальнозоркости используются разные методы диагностики:
- визометрия – для малышей применяют таблицы с картинками, для детей среднего школьного возраста таблицы с буквами;
- определение нарушений преломляющей способности глаза проводится с помощью авторефрактометрии, обязательно в условиях циклоплегии: медикаментозного расширения зрачка и выключения аккомодации;
- скиаскопия и ретиноскопия.
Методы лечения гиперметропии у детей
Лечение дальнозоркости проводится консервативным путем у детей до 18 лет. При отсутствии положительного эффекта после совершеннолетия применяется микрохирургическая операция или лазерная коррекция зрения.
Начиная с самого раннего возраста — с нескольких месяцев жизни, применяются оптические средства для коррекции зрения – очки или контактные линзы. Очковая коррекция наиболее распространенная, в связи с ее доступностью и дешевизной. Применяется плеоптическое аппаратное лечение для развития остроты зрения. Получить высокие положительные результаты и в будущем снять очки можно только при условии правильно подобранных линз. Для этого проводится диагностика, после чего врач выписывает рецепт на необходимые очки. Родители могут самостоятельно выбрать оправу, желательно отдавать предпочтение таким материалам, как карбон или пластмасса. Такие оправы обладают прочностью, надежностью и легкостью, не вызывают дискомфорта. Чтобы ребенок носил очки без капризов лучше выбирать оправу любимой цветовой гаммы малыша.
Некоторые родители подбирают с врачом для коррекции дальнозоркости контактные линзы, так как они имеют свои преимущества – в первую очередь, линзы не сползают и не пачкаются, не мешают ребенку заниматься активными видами спорта.
Аппаратное лечение гиперметропии
Методы аппаратного лечения применяются у детей с 3-х летнего возраста, такие методы весьма эффективны и нравятся малышам. Аппаратное лечение улучшает микроциркуляцию в тканевых структурах глаз, нормализует обменные процессы, улучшает трофику, стимулирует развитие зрительного анализатора, повышение остроты зрения, развитие бинокулярных функций.
Аппаратное лечение проводится в игровой форме по специальной программе, разработанной врачом.
Оперативное лечение
Лазерная коррекция остроты зрения проводится у пациентов с 18 лет. Применяются методы в ходе которых производится искусственное формирование роговичной поверхности с нужной преломляющей силой. Хирургическое вмешательство проводится и в тяжелых случаях и заключается в замене хрусталика.
Осложнения
Отсутствие лечения дальнозоркости может стать причиной развития амблиопии («ленивого глаза», не поддающегося коррекции с помощью оптики), косоглазия.
Белково-энергетическая недостаточность (БЭН) — Болезни нарушения питания
Симптомы умеренной БЭН могут быть общими (системными) или затрагивать определенные органы и системы. Характерны апатия и раздражительность. Пациент ослаблен, работоспособность снижена. Нарушены когнитивные способности, а иногда и сознание. Развиваются временный дефицит лактозы и ахлоргидрия. Часты поносы, которые могут усугубляться дефицитом кишечных дисахаридаз, особенно лактазы. Определяется атрофия ткани половых желез. БЭН может вызвать аменорею у женщин и потерю либидо у представителей обоих полов.
Потери жира и мышечной массы являются общим проявлением для всех форм БЭН. У взрослых добровольцев, которые голодали в течение 30–40 дней, потери веса были явными (25% от начального веса). Если голодание более длительное, то потери веса могут достигнуть 50% у взрослых и, возможно, больших значений у детей.
Кахексия у взрослых наиболее заметна в тех областях, где в норме обычно имеются видимые жировые отложения. Мышцы уменьшаются в объеме, а кости заметно выступают. Кожа становится тонкой, сухой, неэластичной, бледной и холодной. Волосы сухие и легко выпадают, становясь редкими. Замедлено заживление ран. У пожилых пациентов увеличивается риск переломов бедра, пролежней.
Мышцы уменьшаются в объеме, а кости заметно выступают. Кожа становится тонкой, сухой, неэластичной, бледной и холодной. Волосы сухие и легко выпадают, становясь редкими. Замедлено заживление ран. У пожилых пациентов увеличивается риск переломов бедра, пролежней.
При острой или хронической тяжелой БЭН размер сердца и сердечный выброс уменьшаются; пульс замедляется, снижается артериальное давление. Интенсивность дыхания и жизненная емкость легких снижаются. Падает температура тела, что иногда может способствовать смертельному исходу. Могут развиться отек, анемия, желтуха и петехиальная сыпь. Может наблюдаться печеночная, почечная или сердечная недостаточность.
У младенцев маразм вызывает чувство голода, потерю веса, задержку роста, потерю подкожной жировой клетчатки и мышечной массы. Выступают ребра и лицевые кости. Дряблая, тонкая кожа собирается в складки.
Квашиоркор характеризуется периферическими и периорбитальными отеками из-за снижения уровня альбумина. Живот выпячивается из-за ослабления брюшных мышц, растяжения петель кишечника, увеличения печени и асцита. Кожа сухая, тонкая и сморщенная; она становится гиперпигментированной, трескается, а потом развивается ее гипопигментация, рыхлость и атрофия. Кожа различных областей тела может поражаться в различное время. Волосы становятся тонкими, бурыми или седыми. Волосы на голове легко выпадают, в конечном счете становясь редкими, однако ресницы могут расти в значительной степени. Чередование недостаточности питания и адекватного питания приводит к тому, что волосы имеют вид «полосатого флага». Больные дети могут быть апатичными, но становятся раздражительными, если их пытаются расшевелить.
Живот выпячивается из-за ослабления брюшных мышц, растяжения петель кишечника, увеличения печени и асцита. Кожа сухая, тонкая и сморщенная; она становится гиперпигментированной, трескается, а потом развивается ее гипопигментация, рыхлость и атрофия. Кожа различных областей тела может поражаться в различное время. Волосы становятся тонкими, бурыми или седыми. Волосы на голове легко выпадают, в конечном счете становясь редкими, однако ресницы могут расти в значительной степени. Чередование недостаточности питания и адекватного питания приводит к тому, что волосы имеют вид «полосатого флага». Больные дети могут быть апатичными, но становятся раздражительными, если их пытаются расшевелить.
Абсолютное голодание завершается смертью, если длится более 8-12 недель. Таким образом, некоторые характерные для БЭН симптомы не успевают развиться.
Спинальная мышечная атрофия — состояния
Что такое спинальная мышечная атрофия (СМА)?
Спинальная мышечная атрофия — это генетическое заболевание, поражающее двигательные нервные клетки спинного мозга, приводящее к прогрессирующему истощению и слабости мышц. Обычно он начинается в младенчестве или детстве и поражает примерно 1 из 11 000 детей.
Обычно он начинается в младенчестве или детстве и поражает примерно 1 из 11 000 детей.
Что вызывает мышечную атрофию позвоночника?
СМА — аутосомно-рецессивное заболевание. Это означает, что как мужчины, так и женщины страдают в равной степени, и что изменения или мутации в двух копиях гена SMN1 (обычно по одному унаследованному от каждого родителя) необходимы для возникновения этого состояния.Примерно 1 из 50 американцев является носителем SMA.
Тестирование на SMA проводится путем поиска делеций (почти в 95 процентах случаев SMA) или, в меньшем количестве случаев, поиска мутаций в гене SMN1 . Симптомы у людей любого возраста могут быть проверены с помощью исследований ДНК, которые обычно проводятся на основе образца крови. Кроме того, в некоторых случаях пренатальное тестирование может выявить будущих родителей, которые подвержены риску рождения ребенка с СМА, и при желании может быть проведено дополнительное тестирование плода.Когда оба родителя являются носителями, вероятность рождения ребенка с СМА составляет каждый четвертый, или 25 процентов, при каждой беременности.
Каковы симптомы спинальной мышечной атрофии?
Спинальную мышечную атрофию иногда сложно диагностировать, поскольку симптомы могут напоминать другие состояния или медицинские проблемы. Каждый ребенок может испытывать симптомы по-разному, но все дети проявляют признаки слабости, которая со временем постепенно ухудшается без признаков задержки когнитивных функций. Существует четыре типа мышечной атрофии позвоночника в зависимости от симптомов и возраста начала.У ребенка могут быть следующие симптомы естественного течения болезни (или нелеченая форма):
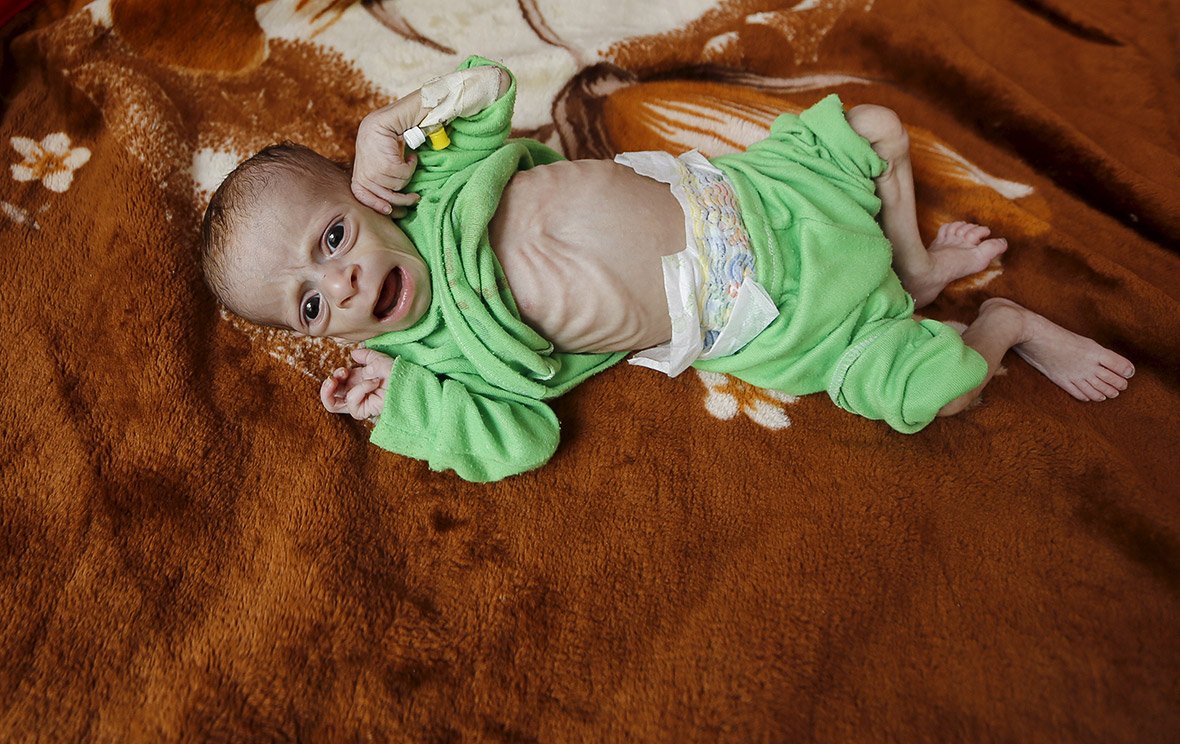
- Тип I (также называемый СМА Верднига-Гофмана или СМА с младенческим началом). Это самый тяжелый тип СМА, который может присутствовать при рождении или в первые шесть месяцев жизни. Младенцы плохо держат голову, сосут, кормят, глотают и обычно очень мало двигаются. Симптомы могут не проявляться сразу при рождении и могут стать более очевидными в течение первых нескольких месяцев жизни и постепенно прогрессировать.
 Также поражаются мышцы груди, что может влиять на дыхание. Движение языка описывается как «червеобразное» движение (также известное как фасцикуляции). Обычно смерть наступает в возрасте от двух до шести лет от проблем с дыханием. Детям с СМА типа I часто требуется дополнительная поддержка дыхания и питания.
Также поражаются мышцы груди, что может влиять на дыхание. Движение языка описывается как «червеобразное» движение (также известное как фасцикуляции). Обычно смерть наступает в возрасте от двух до шести лет от проблем с дыханием. Детям с СМА типа I часто требуется дополнительная поддержка дыхания и питания. - Тип II. Начало этой формы СМА обычно наблюдается у детей в возрасте от шести до 18 месяцев. У них, как правило, наблюдается общая мышечная слабость, и, хотя они могут сохранять независимое сидение, когда их размещают, им трудно переходить в сидение, и они с большей вероятностью будут ползать на животе, чем на четвереньках.По определению, эти дети клинически не достигают самостоятельного статуса (естественная история болезни при отсутствии лечения). По мере прогрессирования заболевания дети со СМА типа II также могут подвергаться риску возникновения проблем с кормлением, проблем с дыханием (особенно во сне или при болезни) и ортопедических проблем (таких как контрактуры, сколиоз и вывих бедра).
- Тип III (также называемый Кугельберг-Веландером или ювенильная SMA). Эта форма СМА поражает детей старше 18 месяцев или в подростковом возрасте.Эти дети имеют ощутимую мышечную слабость и могут рано проявлять признаки неуклюжести, а затем начинают испытывать трудности при ходьбе, вставании или подъеме по лестнице. Обычно такие дети доживают до взрослого возраста. Частота проблем с кормлением или дыханием в этой группе меньше по сравнению с людьми со СМА типа I или типа II.
- Тип IV. Эта форма СМА обычно поражает взрослых в возрасте от тридцати до сорока лет, что приводит к затруднениям при ходьбе и легкой утомляемости.
Симптомы SMA могут напоминать другие проблемы или заболевания. Всегда консультируйтесь с врачом вашего ребенка для постановки диагноза. Если есть подозрение на СМА, или есть необъяснимая слабость или низкий тонус, вас следует направить для дальнейшего обследования к неврологу (желательно к тому, кто имеет опыт обследования детей с нервно-мышечными заболеваниями).
Как диагностируется спинальная мышечная атрофия?
Диагноз спинальной мышечной атрофии ставится после внезапного или постепенного появления специфических симптомов, связанных с прогрессирующей слабостью, и после диагностического тестирования.Во время медицинского осмотра врач вашего ребенка получит полную историю болезни вашего ребенка, и он или она может также спросить, есть ли в семейном анамнезе какие-либо проблемы со здоровьем.
Диагностические тесты, которые могут быть выполнены для подтверждения диагноза спинальной мышечной атрофии, включают следующее:
- Генетические тесты: диагностические тесты, которые оценивают состояния, которые имеют тенденцию протекать в семьях.
Другие тесты:
- Анализы крови
- Биопсия мышцы: небольшой образец мышцы удаляется и исследуется для определения и подтверждения диагноза или состояния.
- Электродиагностические исследования (ЭМГ / исследование нервной проводимости): тест, который измеряет электрическую активность нервов, а также измеряет мышцу или группу мышц и функцию связанных нервов.
 ЭМГ может обнаружить аномальную электрическую активность мышц из-за заболеваний и нервно-мышечных состояний.
ЭМГ может обнаружить аномальную электрическую активность мышц из-за заболеваний и нервно-мышечных состояний.
Если известен семейный анамнез или если известно, что родители являются носителями, тестирование можно провести раньше. Некоторые семьи будут проходить пренатальное тестирование, включая генетическое тестирование во время беременности, чтобы определить, поражен ли плод.Тестирование также может проводиться после рождения новорожденного, чтобы определить, поражен ли ребенок СМА, даже до появления симптомов.
Теперь, когда доступны варианты лечения, важно провести тест на СМА при подозрении на нее или при наличии семейного анамнеза (или если родители являются известными носителями), поскольку более раннее лечение лучше для двигательной функции.
Лечение спинальной мышечной атрофии
Специфическое лечение спинальной мышечной атрофии будет назначено врачом вашего ребенка на основании:
- Возраст вашего ребенка, общее состояние здоровья и история болезни
- Степень заболевания
- Тип позвоночника мышечная атрофия
- Толерантность вашего ребенка к определенным лекарствам, процедурам или методам лечения
- Способность вашего ребенка функционировать по сравнению с его / ее группой сверстников
- Ожидания в отношении течения состояния
- Ваше мнение или предпочтения
Ключ к медицинским показаниям Управление спинальной мышечной атрофией осуществляется путем раннего выявления.

Существуют новые методы лечения пациентов со спинальной мышечной атрофией: первое лечение, одобренное FDA (утверждено в декабре 2016 года), и новые методы лечения, проходящие клинические испытания. Утвержденный FDA препарат для лечения СМА называется Спинраза (Нусинерсен), и это лекарство, которое вводится в пространство спинномозговой жидкости (через процедуру спинномозговой пункции). Наша команда Детского национального центра гордится тем, что может предложить это лечение нашим пациентам с СМА. В Детском национальном центре у нас есть большая программа как по лечению, так и по тщательному мониторингу и систематическому клиническому наблюдению до и после начала лечения.Хотя лечение может улучшить, замедлить или остановить заболевание, оно не может полностью предотвратить возникновение аспектов болезни. Таким образом, по-прежнему существует роль тщательного междисциплинарного наблюдения для решения других проблем, которые могут возникнуть у детей и молодых людей с СМА.
Респираторные органы: При тщательном наблюдении пульмонолога мы оценим дыхательную функцию вашего ребенка. Некоторым детям может потребоваться помощь во время болезни (например, помощь от кашля, аспирация или небулайзерная терапия).Некоторым детям может потребоваться дополнительная поддержка для дыхания во сне или во время сна (например: BiPAP). У других детей могут быть более серьезные проблемы с дыханием, и им может потребоваться дыхательный аппарат, чтобы облегчить ребенку дыхание. Во время респираторных заболеваний детям может потребоваться более тщательный мониторинг и оценка.
Некоторым детям может потребоваться помощь во время болезни (например, помощь от кашля, аспирация или небулайзерная терапия).Некоторым детям может потребоваться дополнительная поддержка для дыхания во сне или во время сна (например: BiPAP). У других детей могут быть более серьезные проблемы с дыханием, и им может потребоваться дыхательный аппарат, чтобы облегчить ребенку дыхание. Во время респираторных заболеваний детям может потребоваться более тщательный мониторинг и оценка.
Кормление / общение: Мы очень внимательно следим за способностью ребенка есть и глотать, чтобы оценить риск удушья или аспирации. Мы также отслеживаем вес наших пациентов, чтобы определить, получают ли они достаточно калорий при пероральном кормлении, или им требуется дополнительная помощь (например, добавка калорий или использование зонда для кормления в качестве добавки).Логопед, участвующий в нашей программе, также следит за языковыми и коммуникативными навыками ребенка и, при наличии показаний, направляет на текущие амбулаторные методы лечения или стратегии общения.
Костно-мышечная / ортопедическая: Наши команды нервно-мышечной, физиотерапевтической и реабилитационной, физиотерапевтической и ортопедической групп работают вместе, чтобы определить потребности вашего ребенка. Сюда могут входить режимы терапии, программы растяжки, фиксации, оборудование для передвижения и перемещения, а в некоторых случаях — хирургическое вмешательство (например, сколиоз).Наша команда также работает над отслеживанием двигательной и неврологической функции с течением времени.
Нашим центром по уходу за пациентами с SMA в Детском национальном университете руководят Сара (Салли) Эванс, доктор медицины, и Диана Баруча-Гебель, доктор медицины, и координирует работу Кэтлин Смарт. Мы гордимся тем, что являемся одним из первых сайтов сети центров обслуживания Cure SMA Care Center в США. Наша команда стремится предоставить нашим пациентам современные, индивидуализированные, комплексные и передовые методы лечения и ухода. Мы внимательно служим источником информации для наших пациентов и их семей, когда мы общаемся с их школами, терапевтами и группами стационарного лечения во время госпитализации.
Спинальная мышечная атрофия (СМА): виды, диагностика и лечение
Что такое спинальная мышечная атрофия (СМА)?
Спинальная мышечная атрофия (СМА) — это группа генетических заболеваний, вызывающих слабость и истощение произвольных мышц у младенцев и детей и, реже, у взрослых. Это одно из наиболее распространенных генетических заболеваний, поражающих детей. По оценкам, каждый 6000–10 000 младенцев в мире рождается со СМА.
В более чем 95 процентах случаев СМА вызывается неадекватной выработкой белка, называемого белком двигательного нейрона выживания (SMN), который необходим для двигательных нейронов.SMN производится SMN1 и в меньшей степени SMN2 . Эти гены находятся на хромосоме 5. Обычно у людей есть две копии гена SMN1 и до двух копий гена SMN2 в каждой из их мотонейронных клеток. У людей со спинальной мышечной атрофией обе копии гена SMN1 изменены или отсутствуют. Наличие дополнительных копий (трех или более) гена SMN2 связано с более легким заболеванием, частично компенсируя отсутствующие SMN1 . В редких случаях СМА вызывается мутациями в генах, отличных от SMN (не хромосома 5).
В редких случаях СМА вызывается мутациями в генах, отличных от SMN (не хромосома 5).
Моторные нейроны лежат в переднем роге спинного мозга и непосредственно контролируют скелетные мышцы тела. Без адекватного белка SMN мотонейроны спинного мозга начинают сокращаться и умирать. Когда это происходит, мозг ребенка не может управлять произвольными мышцами тела, особенно в руках и ногах, а также в голове и шее. Мышцы начинают слабеть и истощаться. Это влияет на движения, такие как ходьба, ползание, контроль головы и шеи, глотание и дыхание.
Какие бывают типы мышечной атрофии позвоночника?
Существует четыре различных типа мышечной атрофии позвоночника. Классификация определяется этапами развития ребенка, которые достигаются к моменту начала заболевания. Типы I и II являются наиболее распространенными.
Типы спинальной мышечной атрофии (СМА):
- Тип 1 (тяжелая форма) SMA : Этот тип также называется болезнью Верднига-Гофмана.
 Это самый тяжелый и самый распространенный тип СМА.Обычно это проявляется при рождении или в первые несколько месяцев после него (0-6 месяцев). Симптомы включают гибкость конечностей и слабое движение туловища. Дети с этим типом обычно имеют очень ограниченную способность двигаться. Им также будет трудно кормить и глотать, поднимать голову и дышать. СМА типа 1 быстро прогрессирует с ослаблением мышц, что приводит к частым респираторным инфекциям и, как правило, к смерти к 2 годам. Младенцы со СМА типа 1 никогда не могут сидеть.
Это самый тяжелый и самый распространенный тип СМА.Обычно это проявляется при рождении или в первые несколько месяцев после него (0-6 месяцев). Симптомы включают гибкость конечностей и слабое движение туловища. Дети с этим типом обычно имеют очень ограниченную способность двигаться. Им также будет трудно кормить и глотать, поднимать голову и дышать. СМА типа 1 быстро прогрессирует с ослаблением мышц, что приводит к частым респираторным инфекциям и, как правило, к смерти к 2 годам. Младенцы со СМА типа 1 никогда не могут сидеть. - Тип 2 (средний уровень) SMA : Симптомы обычно появляются в возрасте от 7 до 18 месяцев.Скорость прогрессирования может сильно различаться. Болезнь поражает скорее ноги ребенка, чем его руки. Дети с СМА типа 2 никогда не могут стоять. Респираторные инфекции также распространены при этом типе СМА. Ожидаемая продолжительность жизни может варьироваться от раннего детства до взрослого возраста, в зависимости от тяжести состояния пациента.

- Тип 3 (легкая форма) СМА : Этот тип СМА также называется Кугельберг-Веландером или ювенильной спинальной мышечной атрофией. Симптомы могут впервые появиться в течение многих лет, от 18 месяцев до раннего взросления.Пациенты с СМА 3 типа могут стоять и ходить, но могут испытывать затруднения при вставании из положения сидя. У них также может наблюдаться легкая мышечная слабость и повышенный риск респираторных инфекций. У большинства пациентов со СМА 3-го типа продолжительность жизни близка к нормальной.
- Тип 4 (взрослый) SMA : Симптомы этого редкого типа SMA обычно не проявляются до второго или третьего десятилетия жизни. Пациенты со СМА 4 типа могут ходить в зрелом возрасте, но обычно будут испытывать медленно прогрессирующую мышечную слабость и другие типичные симптомы СМА.
Если вы заметили какой-либо из этих симптомов у своего ребенка или у себя, немедленно обратитесь к врачу.
Кто страдает мышечной атрофией позвоночника?
Спинальная мышечная атрофия может поражать людей любой расы и пола. Дополнительно
Дополнительно
- Каждый 40 человек несет ген, вызывающий СМА.
- Ребенок от двух генных носителей имеет 25-процентный шанс родиться со спинальной мышечной атрофией.
- По оценкам, семьдесят пять миллионов американцев являются носителями гена спинальной мышечной атрофии.
- Считается, что более 25 000 американцев страдают от мышечной атрофии позвоночника.
Последний раз проверял медицинский работник Cleveland Clinic 24.11.2015.
Список литературы
- Даррас Б.Т., Марковиц Дж. А., Монани У. Р., Де Виво, округ Колумбия.Спинальные мышечные атрофии. В: Даррас Б.Т., Джонс Х.Р. и др., Редакторы. Нервно-мышечные расстройства младенчества, детства и подросткового возраста.
 2-е изд. Амстердам: Academic Press, отпечаток Elsevier; 2014: Глава 8.
2-е изд. Амстердам: Academic Press, отпечаток Elsevier; 2014: Глава 8. - Амато А.А., Рассел Дж. А. Спинальные мышечные атрофии. В: Amato AA, Russell JA. ред. Нервно-мышечные расстройства, 2д. Нью-Йорк, штат Нью-Йорк: Макгроу-Хилл; 2015.
- Genetics Домашний справочник. Спинальная мышечная атрофия Дата обращения 24.11.2015.
- Национальный институт исследования генома человека.Изучение спинальной мышечной атрофии, дата обращения 24.11.2015.
- Ассоциация мышечной дистрофии (MDA). Спинальная мышечная атрофия Дата обращения 24.11.2015.
Получите полезную, полезную и актуальную информацию о здоровье и благополучии
е Новости Клиника Кливленда — некоммерческий академический медицинский центр. Реклама на нашем сайте помогает поддерживать нашу миссию. Мы не поддерживаем продукты или услуги, не принадлежащие Cleveland Clinic.
Политика
Реклама на нашем сайте помогает поддерживать нашу миссию. Мы не поддерживаем продукты или услуги, не принадлежащие Cleveland Clinic.
Политика
Младенец с дискетами | Американская академия педиатрии
Цели
После прочтения этой статьи читатели должны уметь:
Охарактеризовать отличительные черты гипотонии и мышечной слабости.
Опишите различия между центральными и периферическими причинами гипотонии.
Создайте дифференциальный диагноз гипотонии у младенцев.
Обсудите соответствующую медико-генетическую оценку гипотонии у младенцев.
Понимать необходимость подозревать детский ботулизм у ребенка младше 6 месяцев с такими признаками и симптомами, как запор, вялость, плохое питание, слабый крик, снижение рвотного рефлекса и гипотония.

Введение
«Гибкий младенец» представляет собой диагностическую проблему для педиатров общего профиля. Младенцы могут иметь гипотонию, вызванную аномалиями центральной или периферической нервной системы, миопатиями, генетическими нарушениями, эндокринопатиями, метаболическими заболеваниями, а также острыми или хроническими заболеваниями (Таблица 1). Системный подход к ребенку с гипотонией, с уделением внимания анамнезу и клиническому обследованию, имеет первостепенное значение для локализации проблемы в конкретном регионе нервной системы.
| Заболевания клеток переднего рога |
|
| Врожденные моторные или сенсорные невропатии |
|
| Нарушения нервно-мышечного соединения |
| Врожденные миопатии |
| Мышечные дистрофии |
|
| Метаболические и мультисистемные заболевания |
|

Дифференциальная диагностика нервно-мышечных заболеваний у новорожденных
Важно…
Спинальная мышечная атрофия: причины, симптомы и лечение
Что такое спинальная мышечная атрофия?
Спинальная мышечная атрофия (СМА) чаще всего поражает младенцев и детей и мешает им использовать свои мышцы. Когда у вашего ребенка СМА, нервные клетки головного и спинного мозга разрушаются. Мозг перестает посылать сообщения, управляющие движением мышц.
Когда это происходит, мышцы вашего ребенка становятся слабыми и сокращаются, и у детей могут возникнуть проблемы с контролем движения головы, сидением без посторонней помощи и даже ходьбой. В некоторых случаях у них могут возникнуть проблемы с глотанием и дыханием по мере обострения болезни.
Существуют разные типы СМА, и насколько серьезна она, зависит от того, какой тип у вашего ребенка. Лекарства нет, но лечение может улучшить некоторые симптомы, а в некоторых случаях помочь вашему ребенку прожить дольше. Исследователи работают над поиском новых способов борьбы с болезнью.
Исследователи работают над поиском новых способов борьбы с болезнью.
Имейте в виду, что каждый ребенок или взрослый, страдающий СМА, будет иметь разный опыт. Независимо от того, насколько ограничены движения вашего ребенка, болезнь никак не влияет на его интеллект. Они по-прежнему смогут заводить друзей и общаться.
Симптомы спинальной мышечной атрофии
Симптомы сильно различаются в зависимости от типа SMA:
Тип 0. Это самая редкая и самая тяжелая форма SMA, которая развивается, пока вы беременны. Младенцы с этим типом СМА меньше двигаются в утробе матери и рождаются с проблемами суставов, слабым мышечным тонусом и слабыми мышцами для дыхания.Часто они не выживают из-за проблем с дыханием.
Тип 1. Это также тяжелый тип СМА. Ребенок может не поддерживать голову или сидеть без посторонней помощи. У них могут быть гибкие руки и ноги и проблемы с глотанием.
Наибольшую озабоченность вызывает слабость мышц, контролирующих дыхание. Большинство детей с СМА типа 1 не доживают до 2 лет из-за проблем с дыханием.
Большинство детей с СМА типа 1 не доживают до 2 лет из-за проблем с дыханием.
Поддерживайте связь со своей медицинской бригадой, членами семьи, духовенством и другими людьми, которые могут оказать вам эмоциональную поддержку, в которой вы нуждаетесь, пока ваш ребенок борется с этой болезнью.
Тип 2. Поражает детей в возрасте 6-18 месяцев. Симптомы варьируются от умеренных до тяжелых и обычно затрагивают ноги больше, чем руки. Ваш ребенок может сидеть и ходить или стоять с помощью.
Продолжение
Тип 2 также называется хронической инфантильной СМА.
Тип 3. Симптомы этого типа проявляются в возрасте 2-17 лет. Это самая легкая форма болезни. Ваш ребенок, скорее всего, сможет стоять или ходить без посторонней помощи, но у него могут быть проблемы с бегом, подъемом по лестнице или вставанием со стула.В более позднем возрасте им может понадобиться инвалидное кресло для передвижения.
Тип 3 также называют болезнью Кугельберга-Веландера или ювенильной СМА.
Тип 4. Эта форма SMA начинается, когда вы становитесь взрослым. У вас могут быть такие симптомы, как мышечная слабость, подергивание или проблемы с дыханием. Обычно поражаются только плечи и ноги.
Симптомы будут проявляться на протяжении всей жизни, но вы можете продолжать двигаться и даже поправляться с помощью упражнений, которые вы будете выполнять с помощью физиотерапевта.
Важно помнить, что существует множество вариантов того, как этот тип СМА влияет на людей. Например, многие люди могут работать долгие годы. Спросите своего врача, как можно встретиться с другими людьми, у которых такое же заболевание, и узнать, через что вы проходите.
Причины мышечной атрофии позвоночника
СМА — это заболевание, передающееся от семьи. Если у вашего ребенка СМА, это потому, что у него есть две копии сломанного гена, по одной от каждого родителя.
Когда это произойдет, их организм не сможет производить определенный вид белка. Без него клетки, контролирующие мышцы, умирают.
Если ваш ребенок получит дефектный ген только от одного из вас, он не получит SMA, но станет носителем болезни. Когда ваш ребенок вырастет, он может передать сломанный ген своему ребенку.
Диагноз спинальной мышечной атрофии
СМА трудно диагностировать, потому что симптомы могут быть похожи на другие состояния. Чтобы понять, что происходит, врач может спросить вас:
- Пропустил ли ваш ребенок какие-либо вехи в развитии, например, поднятие головы вверх или переворачивание?
- Вашему ребенку трудно самостоятельно сидеть или стоять?
- Вы видели, что у вашего ребенка проблемы с дыханием?
- Когда вы впервые заметили симптомы?
- Были ли у кого-нибудь в вашей семье подобные симптомы?
Продолжение
Ваш врач может также назначить некоторые анализы, которые помогут поставить диагноз.Например, они могут взять образец крови у вашего ребенка, чтобы проверить отсутствие или повреждение генов, которые могут вызвать СМА. Ваш врач также может назначить анализ крови на креатинкиназу (КК). Это фермент, который вытекает из ослабленных мышц. Высокий уровень КФК в крови не всегда вреден, но указывает на возможное повреждение мышц.
Ваш врач также может назначить анализ крови на креатинкиназу (КК). Это фермент, который вытекает из ослабленных мышц. Высокий уровень КФК в крови не всегда вреден, но указывает на возможное повреждение мышц.
Другие тесты исключают состояния с похожими симптомами:
- Нервные тесты, такие как электромиограмма (ЭМГ). Ваш врач накладывает небольшие пластыри на кожу вашего ребенка и посылает электрические импульсы по нервам, чтобы проверить, посылают ли они сигналы мышцам.
- CT. Это мощный рентгеновский снимок, который позволяет детально снимать внутреннюю часть тела вашего ребенка.
- МРТ. Он использует мощные магниты и радиоволны для создания изображений органов и структур внутри вашего ребенка.
- Биопсия мышечной ткани. В этом тесте врач удаляет мышечные клетки через иглу в мышце или через небольшой разрез на коже вашего ребенка.
Вопросы для врача
- Лечили ли вы других людей с этим заболеванием?
- Какие процедуры вы рекомендуете?
- Есть ли терапия, которая может помочь моему ребенку оставаться сильными?
- Что я могу сделать, чтобы помочь моему ребенку стать более независимым?
- Как я могу связаться с другими членами семьи, у которых есть SMA?
Лечение мышечной атрофии позвоночника
FDA одобрило три препарата для лечения СМА: нусинерсен (Спинраза), онасемноген абепарвовец-xioi (Золгенсма) и рисдиплам (Эврисди). Обе формы генной терапии влияют на гены, участвующие в СМА. Гены SMN1 и SMN2 дают вашему телу инструкции по выработке белка, который помогает контролировать движение мышц.
Обе формы генной терапии влияют на гены, участвующие в СМА. Гены SMN1 и SMN2 дают вашему телу инструкции по выработке белка, который помогает контролировать движение мышц.
- Нусинерсен (Спинраза). Эта процедура регулирует ген SMN2 и позволяет ему производить больше белка. Используется как для детей, так и для взрослых с СМА. Медицинская бригада вашего ребенка введет препарат в жидкость вокруг спинного мозга. Включая время на подготовку и восстановление, это может занять не менее 2 часов, и его нужно будет делать несколько раз, а затем новую дозу каждые 4 месяца.Исследования показывают, что он помогает примерно 40% употребляющих его людей, делая их сильнее и замедляя течение болезни.
- Онасемноген abeparvovec-xioi (Zolgensma). Это включает замену проблемного гена SMN1. Применяется для детей до 2 лет. Медицинская бригада вашего ребенка вставит крошечную трубку, называемую катетером, прямо в вену на руке или руке (IV). Затем они отправят копию гена SMN через трубку в определенную группу клеток мотонейрона.
 Это нужно будет сделать только один раз.В исследованиях онасемноген abeparvovec-xioi помогал детям со СМА быстрее достигать определенных этапов развития, таких как способность контролировать голову или сидеть без поддержки.
Это нужно будет сделать только один раз.В исследованиях онасемноген abeparvovec-xioi помогал детям со СМА быстрее достигать определенных этапов развития, таких как способность контролировать голову или сидеть без поддержки. - Рисдиплам (Эврисди) . Это лечение работает, чтобы остановить гены SMN2 от нарушения производства белка, позволяя белку достигать нервных клеток по мере необходимости. Ваш ребенок принимает его внутрь один раз в день после еды. Дозировка определяется их массой. Клинические испытания показали улучшение мышечной функции через 12 месяцев у 41% принимавших его.
Продолжение
Помимо генной терапии, ваш врач может предложить несколько других способов облегчить симптомы:
- Дыхание. При СМА, особенно 1-го и 2-го типов, слабые мышцы не позволяют воздуху легко попадать в легкие и выходить из них. Если это произойдет с вашим ребенком, ему может потребоваться специальная маска или загубник. При серьезных проблемах ваш ребенок может использовать машину, которая помогает ему дышать.

- Глотание и питание. Когда мышцы рта и горла ослаблены, младенцы и дети со СМА могут испытывать трудности с сосанием и глотанием.В этой ситуации ваш ребенок может не получать полноценного питания и у него могут возникнуть проблемы с ростом. Ваш врач может посоветовать обратиться к диетологу. Некоторым младенцам может потребоваться зонд для кормления.
- Механизм. Физическая терапия и трудотерапия, при которой используются упражнения и регулярные повседневные занятия, могут помочь защитить суставы вашего ребенка и сохранить мышцы сильными. Терапевт может посоветовать скобы для ног, ходунки или электрическую инвалидную коляску. Специальные инструменты могут управлять компьютерами и телефонами, помогать писать и рисовать.
- Предыдущие выпуски. Когда СМА начинается в детстве, у детей может появиться искривление позвоночника. Врач может посоветовать вашему ребенку носить спинной бандаж, пока его позвоночник все еще растет.
 Когда они перестают расти, им может быть сделана операция, чтобы решить проблему.
Когда они перестают расти, им может быть сделана операция, чтобы решить проблему.
Уход за ребенком со спинальной мышечной атрофией
Вы можете многое сделать как семья, чтобы помочь своему ребенку с некоторыми из основных задач повседневной жизни. Команда врачей, терапевтов и групп поддержки может помочь вам в уходе за вашим ребенком и позволить им поддерживать дружеские отношения и заниматься с вашей семьей.
Вашему ребенку, вероятно, потребуется пожизненный уход у разных врачей. Возможно, им потребуется посетить:
- Пульмонологи, врачи, лечащие легкие
- Неврологи, специалисты по нервным проблемам
- Ортопеды, врачи, занимающиеся проблемами костей
- Гастроэнтерологи, специалисты по заболеваниям желудка
- Диетологи, специалисты по влиянию пищи здоровье вашего ребенка
- Физиотерапевты, люди, обученные использованию физических упражнений для улучшения движений вашего ребенка
Эта группа может помочь вам принять решение о здоровье вашего ребенка.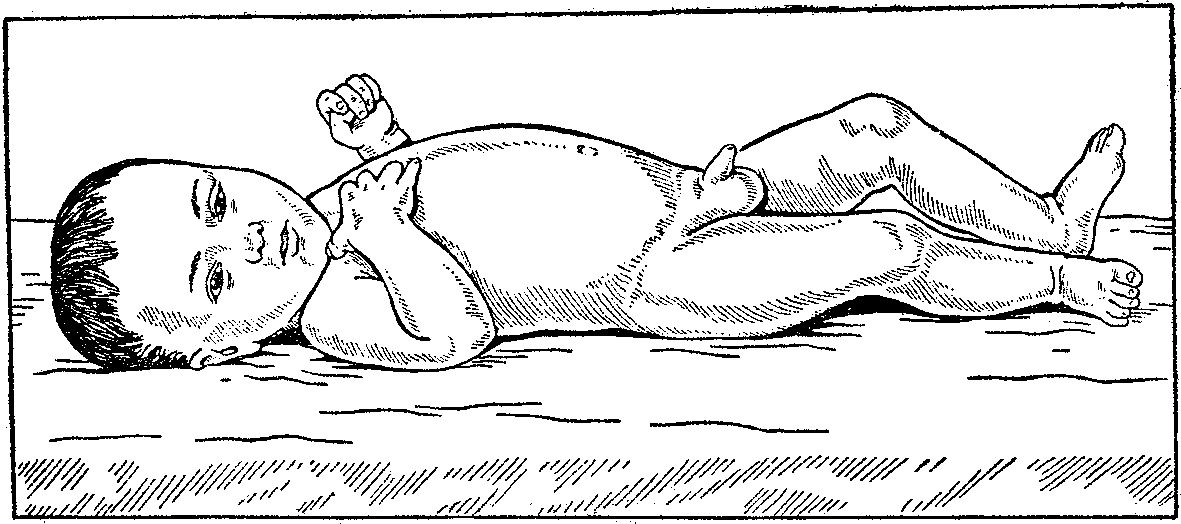 Важно не позволять себе перегружать себя задачей управления уходом. Найдите группы поддержки, которые позволят вам поделиться своим опытом с другими людьми, оказавшимися в аналогичной ситуации.
Важно не позволять себе перегружать себя задачей управления уходом. Найдите группы поддержки, которые позволят вам поделиться своим опытом с другими людьми, оказавшимися в аналогичной ситуации.
Прогноз мышечной атрофии позвоночника
Прогноз зависит от того, когда появились симптомы и насколько серьезны они. Если у вашего ребенка тип 1, тяжелая форма СМА, симптомы могут появиться в любом месте от рождения до возраста 6 месяцев. В целом, у большинства детей с этим типом заболевания признаки болезни появляются в возрасте 3 месяцев.Вы начнете замечать, что их развитие задерживается, и они не могут ни сидеть, ни ползать.
Продолжение
Даже несмотря на то, что дети с этим типом обычно не доживают до двух лет, с помощью ваших врачей и группы поддержки вы можете сделать их жизнь комфортной.
При других типах СМА врачи могут помочь облегчить симптомы у ребенка на многие годы, а во многих случаях — на протяжении всей жизни.
Имейте в виду, что каждый ребенок или взрослый, страдающий СМА, будет иметь разный опыт. План лечения, разработанный специально для вашего ребенка, может помочь ему улучшить качество жизни.
План лечения, разработанный специально для вашего ребенка, может помочь ему улучшить качество жизни.
Поддержка спинальной мышечной атрофии
Подобные организации могут предложить вам поддержку:
- Cure SMA. Он финансирует исследования, направленные на лечение и лечение СМА. Его инициатива SMArt Moves подчеркивает важность ранней диагностики и лечения. Cure SMA также предлагает поддержку людям и семьям в местных отделениях и на своем веб-сайте, в том числе предлагает информацию тем, кому впервые поставлен диагноз.
- Ассоциация мышечной дистрофии. В этой группе есть информация и ссылки на службы и группы поддержки в вашем регионе.
- SMA Foundation. Его миссия — активизировать поиск методов лечения СМА, работать с исследователями, проводить клинические испытания и помогать другим людям узнавать об этом генетическом заболевании.
Гипотония — Причины — NHS
Гипотония (снижение мышечного тонуса) — это скорее симптом, чем состояние. Это может быть вызвано рядом основных проблем, которые могут быть неврологическими или не неврологическими.
Это может быть вызвано рядом основных проблем, которые могут быть неврологическими или не неврологическими.
Неврологические состояния — это состояния, поражающие нервы и нервную систему. Гипотония чаще всего связана с неврологическим контролем мышечного тонуса.
Нормальное функционирование мышц зависит от сигналов двигательных нервов. Эти сигналы могут быть нарушены на уровне головного и спинного мозга (центральная гипотония) или в результате повреждения нервов между спинным мозгом и мышцами (периферическая гипотония).
Неврологические состояния
Неврологические состояния, которые влияют на центральную нервную систему и могут вызывать центральную гипотонию, включают:
- церебральный паралич — неврологические проблемы при рождении, которые влияют на движения и координацию ребенка
- Повреждение головного и спинного мозга — включая кровотечение в головном мозге
- серьезные инфекции — такие как менингит (инфекция внешней оболочки головного мозга) и энцефалит (инфекция самого мозга)
Неврологические состояния, которые влияют на периферическую нервную систему и могут вызывать периферическую гипотонию, включают:
- мышечная дистрофия — группа генетических состояний, которые постепенно вызывают ослабление мышц, что приводит к увеличению, но изменчивому уровню инвалидности
- myasthenia gravis — заболевание, вызывающее у взрослых слабость и повышенную утомляемость, а не гипотонию; младенцы, рожденные от матерей с миастенией, также могут быть затронуты, и в таком случае у них обычно будет гипотония
- Спинальная мышечная атрофия — генетическое заболевание, вызывающее мышечную слабость и прогрессирующую потерю подвижности
- Болезнь Шарко-Мари-Тута — наследственное заболевание, поражающее вещество под названием миелин, которое покрывает нервы и помогает передавать сообщения в мозг и из него
Неневрологические проблемы
К неневрологическим проблемам, которые могут вызвать гипотонию у новорожденных и маленьких детей, относятся:
- Синдром Дауна — генетическое заболевание, присутствующее при рождении, которое влияет на нормальное физическое развитие человека и вызывает трудности в обучении
- Синдром Прадера-Вилли — редкий генетический синдром, вызывающий широкий спектр симптомов, включая постоянный голод, ограничение роста и трудности в обучении
- Болезнь Тея-Сакса — редкое и обычно смертельное генетическое заболевание, вызывающее прогрессирующее поражение нервной системы
- врожденный гипотиреоз — при рождении ребенка с недостаточной активностью щитовидной железы; в Великобритании младенцы проходят обследование и раннее лечение
- Синдром Марфана и Синдром Элерса-Данлоса — наследственные синдромы, которые влияют на соединительные ткани, которые обеспечивают структуру и поддержку других тканей и органов
- Нарушения соединительной ткани — соединительная ткань, такая как коллаген, обеспечивает тканям тела силу и поддержку и находится в связках и хрящах
- преждевременные роды (до 37 недели беременности) — недоношенные дети иногда имеют гипотонию, потому что их мышцы не полностью развиты к моменту рождения
Гипотония в более старшем возрасте
Гипотония иногда может возникать у детей старшего возраста и взрослых, хотя встречается реже.
Это может быть вызвано некоторыми из проблем, упомянутых выше, но другие возможные причины включают:
- рассеянный склероз — при котором миелин, покрывающий нервные волокна, повреждается, что нарушает их способность передавать электрические сигналы от головного и спинного мозга к остальным частям тела
- Болезнь двигательных нейронов — редкое заболевание, которое постепенно повреждает двигательные нервы и приводит к истощению мышц
Слабость, проблемы с подвижностью и равновесием также являются обычным явлением для этих состояний.
Последняя проверка страницы: 11 июня 2018 г.
Срок следующей проверки: 11 июня 2021 г.
NW Клинические рекомендации для новорожденных — Гипотония новорожденных
NW Клинические рекомендации для новорожденных — Гипотония новорожденныхГипотония новорожденных | Отзыв Мелиндера Нолана (неврология) |
| июнь 2015 |
Врожденная гипотония — относительно частый диагноз в период новорожденности. Это
определяется как субъективное снижение сопротивления пассивному диапазону движений в
новорожденный и может быть вызван дефектом на любом уровне нервной системы.
Это
определяется как субъективное снижение сопротивления пассивному диапазону движений в
новорожденный и может быть вызван дефектом на любом уровне нервной системы.
Причины включают (но не ограничиваются):
| Центральный (наиболее часто встречающийся) |
|
| Спинной мозг |
|
| Ячейка переднего рога |
|
| Нервно-мышечное соединение |
|
| Мышцы |
|
| Периферические нервы |
|
| Метаболические миопатии |
|
Первая цель диагностики источника неонатальной гипотонии — установить, он центральный (верхний мотонейрон) или периферический (нижний мотонейрон). Центральные причины являются наиболее частыми. Это разграничение определит исследования, которые, скорее всего, принесут диагноз.
- Любая значительный семейный анамнез затронул родителей или братьев и сестер, родство, мертворожденных, детских смертей
- Материнская болезнь диабет, эпилепсия, миотоник дистрофия (может не распознаваться)
- Беременность и история доставки лекарственного средства или тератогена
- Уменьшено шевеление плода
- Ненормальный презентация
- Многоводие / олигогидрамнион
- Апгар набрал
- Реанимация требования
- Шнур газы
- История
с момента доставки
- Респираторный усилие
- Способность кормить
- Уровень бдительности
- Уровень спонтанной активности
- Персонаж крика
Необходимо провести подробный физический осмотр, оценить мышечный тонус, любые
асимметрия, сила младенцев, глубокие сухожильные рефлексы (DTR) и любые
дисморфические или необычные черты лица.
Центральный | Ячейка переднего рога | Нерв | Нервно-мышечное соединение | Мышца |
| нормальный прочность | обобщенный слабость | слабость, дистальный> проксимальный | слабость, лицо / глаза / бульбар | слабость, проксимальный> дистальный, лицевой, EOM |
| нормальный / увеличенные ДТР + | уменьшено / отсутствуют ДТР | уменьшено / отсутствуют ДТР | нормальный DTRs | уменьшено DTRs |
| +/- изъятия | фасцикуляции | +/- фасцикуляции | нет фасцикуляции | |
| +/- дисморфический особенности, пониженная настороженность | часто описан как предупреждение | +/- артрогрипоз | +/- контрактуры |
+ Иногда у детей с выраженной центральной гипотонией может отсутствовать DTR, поэтому отсутствие DTR хотя бы в первые дни жизни не исключало бы центрального причина гипотонии
* Обратите внимание, что наличие глубокой слабости, а также гипотонии предполагает расстройство нижнего мотонейрона.
Признаком этого может быть слабый крик. Слабое место редко встречается при центральной гипотонии, за исключением стадии обострения.
Артрогрипоз (фиксация суставов при рождении) может быть связаны с неонатальной гипотонией, чаще с нижним двигательным нейроном единичные или мультисистемные аномалии.
Дополнительно ключи, которые могут указывать на конкретный диагноз:
- Гепатоспленомегалия нарушения памяти, врожденные инфекции
- Почечная кисты, высокий лоб, широкий родничок, синдром Зеллвегера
- Гепатомегалия, пигментный ретинит неонатальная адренолейкодистрофия
- Врожденный катаракта, окулоцереброренальный синдром (Лоу) глаукома
- Ненормальный нарушение обмена запаха
- Гипопигментация, неопущенные яички Prader Willi
Обследование матери также важно при подозрении на врожденные миотоническая дистрофия или миастения.
Большинство исследований показали, что на центральные причины приходится 60-80% случаев и что
Диагноз обычно можно установить на основе тщательного анамнеза и обследования. Однако,
может быть смешанная картина. Младенцы с периферийной причиной их
гипотония может иметь повышенный риск проблем во время родов, родоразрешения и
реанимация и развитие гипоксической ишемической энцефалопатии.
Однако,
может быть смешанная картина. Младенцы с периферийной причиной их
гипотония может иметь повышенный риск проблем во время родов, родоразрешения и
реанимация и развитие гипоксической ишемической энцефалопатии.
Далее при расследовании необходимо руководствоваться анамнезом и осмотром.
- Если младенец гипотоничен, но имеет определенную степень силы, что является основной причиной наиболее вероятно, и исследования должны быть направлены на это.
- Если младенец гипотоничен и слаб, возможна периферическая причина и раннее осмотр неврологической службой является обязательным.
Основные причины |
|
Периферийные причины |
|
| 1 | Фенихель
GM. Неонатальная неврология, 3-е издание. Черчилль Ливингстон Инк.1990 Неонатальная неврология, 3-е издание. Черчилль Ливингстон Инк.1990 |
| 2 | Паро-Панджан Д., Нойбауэр Д. Врожденная гипотония: есть ли алгоритм? Журнал Детская неврология; Июнь 2004 г., Том 19 (6): 439-43 |
| 3 | Прасад А.Н., Прасад С. Младенец с гибкостью: вклад генетических и метаболических расстройства. Мозг и развитие; Октябрь 2003 г., том 25 (7): 457-76 |
Спинальная мышечная атрофия — НОРД (Национальная организация по редким заболеваниям)
УЧЕБНИКИ
Руссман Б.С.Спинальная мышечная атрофия. В: The NORD Guide to Rare Disorders, Philadelphia, PA: Lippincott, Williams and Wilkins, 2003: 637.
СТАТЬИ ИЗ ЖУРНАЛА
Wu JS, Darras BT, Rutkove SB. Оценка спинальной мышечной атрофии с помощью количественного ультразвукового исследования // Неврология. 2010; 75 (6): 526-31.
2010; 75 (6): 526-31.
Руткове С.Б., Шефнер Дж. М., Грегас М. и др. Характеристика спинальной мышечной атрофии с помощью электроимпедансной миографии. Мышечный нерв. 2010; 42 (6): 915-21.
Левелт А., Кроссчелл К.Дж., Скотт С. и др.Потенциал действия сложных мышц и двигательная функция у детей со спинальной мышечной атрофией. Мышечный нерв. 2010; 42 (5): 703-8.
Ренбаум П., Келлерман Э., Джарон Р. и др. Спинальная мышечная атрофия с понтоцеребеллярной гипоплазией вызвана мутацией в гене VRK1. Am J Hum Genet. 2009; 85 (2): 281-9.
Бах-младший. Использование искусственной вентиляции легких уместно у детей с генетически подтвержденной мышечной атрофией позвоночника 1 типа: движение для. Педиатр Респир Ред. 2008; 9 (1): 45-50.
Brichta L, et al. Активация SMN in vivo у носителей спинальной мышечной атрофии и пациентов с вальпроатом. Энн Нейрол. 2006; 59: 970-5.
Кауфманн П., Мунтони Ф .; Международный координационный комитет подкомитета SMA по дизайну клинических испытаний SMA. Вопросы дизайна клинических исследований СМА. Международный координационный комитет (ICC) Подкомитета SMA по дизайну клинических испытаний SMA. Нейромышечное расстройство. 2007; 17 (6): 499-505.
Вопросы дизайна клинических исследований СМА. Международный координационный комитет (ICC) Подкомитета SMA по дизайну клинических испытаний SMA. Нейромышечное расстройство. 2007; 17 (6): 499-505.
Swoboda KJ, Prior TW, Scott CB и др. Естественное течение денервации при СМА: отношение к возрасту, количеству копий SMN2 и функции.Энн Нейрол. 2005; 57 (5): 704-12.
Mellies U, Dohna-Schwake C, Stehling F, Voit T. Нарушение дыхания во сне при спинальной мышечной атрофии. Нейромышечное расстройство. 2004; 14 (12): 797-803.
Puruckherr M, Mehta JB, Girish MR, Byrd RP Jr, Roy TM. Тяжелое обструктивное апноэ во сне у пациента с атрофией спинных мышц. Сундук. 2004; 126 (5): 1705-7.
Brichta L, et al. Вальпроевая кислота увеличивает уровень белка SMN2: препарат, хорошо известный как потенциальное средство для лечения спинальной мышечной атрофии.Hum Mol Genet. 2003; 12: 2481-9.
Руссман Б.С. и др. Фаза 1 испытания рилузола при спинальной мышечной атрофии. Арка Neurol. 2003; 60: 1601-03.
2003; 60: 1601-03.
Бах Дж., Вега Дж., Майорс Дж., Фридман А. Спинальная мышечная атрофия типа 1 — качество жизни. Am J Phys Med Rehabil. 2003; 82 (2): 137-42.
Sporer SM, Смит Б.Г. Вывих бедра у пациентов со спинальной мышечной атрофией. J Pediatr Orthop. 2003; 23 (1): 10-4.
Laufersweiler-Plass C, Rudnik-Schöneborn S, Zerres K, Backes M, Lehmkuhl G, von Gontard A.Поведенческие проблемы у детей и подростков со спинальной мышечной атрофией и у их братьев и сестер. Dev Med Child Neurol. 2003; 45 (1): 44-9.
Bromberg MB, Swoboda KJ. Оценка количества двигательных единиц у младенцев и детей со спинальной мышечной атрофией. Мышечный нерв. 2002; 25 (3): 445-7.
Courtens W, Johansson AB, Dachy B, Avni F, Telerman-Toppet N, Scheffer H. Вариант инфантильной мышечной атрофии позвоночника с врожденными переломами у новорожденного женского пола: доказательства аутосомно-рецессивного наследования.J Med Genet. 2002; 39 (1): 74-7.
Бах Дж. Р., Бэрд Дж. С., Плоски Д., Навадо Дж., Уивер Б. Спинальная мышечная атрофия 1 типа: лечение и результаты. Педиатр Пульмонол. 2002; 34 (1): 16-22.
С., Плоски Д., Навадо Дж., Уивер Б. Спинальная мышечная атрофия 1 типа: лечение и результаты. Педиатр Пульмонол. 2002; 34 (1): 16-22.
Миллер Р., Мур Д.Х., Дронски В. и др. Плацебо-контролируемое испытание габапентина при спинальной мышечной атрофии. J Neurol Sci. 2001; 15; 191 (1-2): 127-31.
Гозал Д., Легочные проявления нервно-мышечной болезни с особым упором на мышечную дистрофию Дюшенна и спинальную мышечную атрофию.Педиатр Пульмонол. 2000; 29: 141-50.
Strober JB и др., Прогрессирующие мышечные атрофии позвоночника. J Child Neurol. 1999; 14: 691-95.
Андерссон П. Б. и др. Нервно-мышечные расстройства у детей. Curr Opin Pediatr. 1999; 11: 497-503.
Лю Ю.Б. и др., Остановка предсердий в случае синдрома Кугельберга-Веландера с поражением сердца: электрофизиологическое исследование. Int J Cardiol. 1999; 70: 207-10.
Zerres K, Rudnick-Schoneborn S, Forrest E, et al. Совместное исследование естественного течения проксимальной СМА с дебютом у детей и подростков (СМА типа II и III): 569 пациентов. J Neurol Sci. 1997; 146: 67-72.
J Neurol Sci. 1997; 146: 67-72.
Cunha MC, et al., Спинальная мышечная атрофия II типа (промежуточный) и III (Кугельберг-Веландер). Эволюция 50 пациентов с физиотерапией и гидротерапией в бассейне. Arq Neuropsiquiatr. 1996; 54: 402-06.
Исодзуми К., Делонг Р., Каплан Дж. И др. Связь спинальной мышечной атрофии лопатки и надкостницы с хромосомой 12q24.1-q24.31. Hum Mol Genet. 1996; 5 (9): 1377-82.
Thomas NH, Dubowitz V. Естественное течение СМА типа I (тяжелой).Нервно-мышечное расстройство. 1994; 4: 497-502.
Brzustowicz LM, et al., Оценка неаллельной генетической гетерогенности хронической (тип II и III) спинальной мышечной атрофии. Hum Hered. 1993; 43: 380-87.
Майлз Дж. М. и др., Патологический случай месяца. Спинальная мышечная атрофия 3 типа (болезнь Кугельберга-Веландера). Am J Dis Child. 1993; 147: 793-94.
Iannaccone ST, Browne RH, Samaha FL, et al. Группа DCN / SMA: проспективное исследование SMA в возрасте до шести лет. Pediatr Neurol.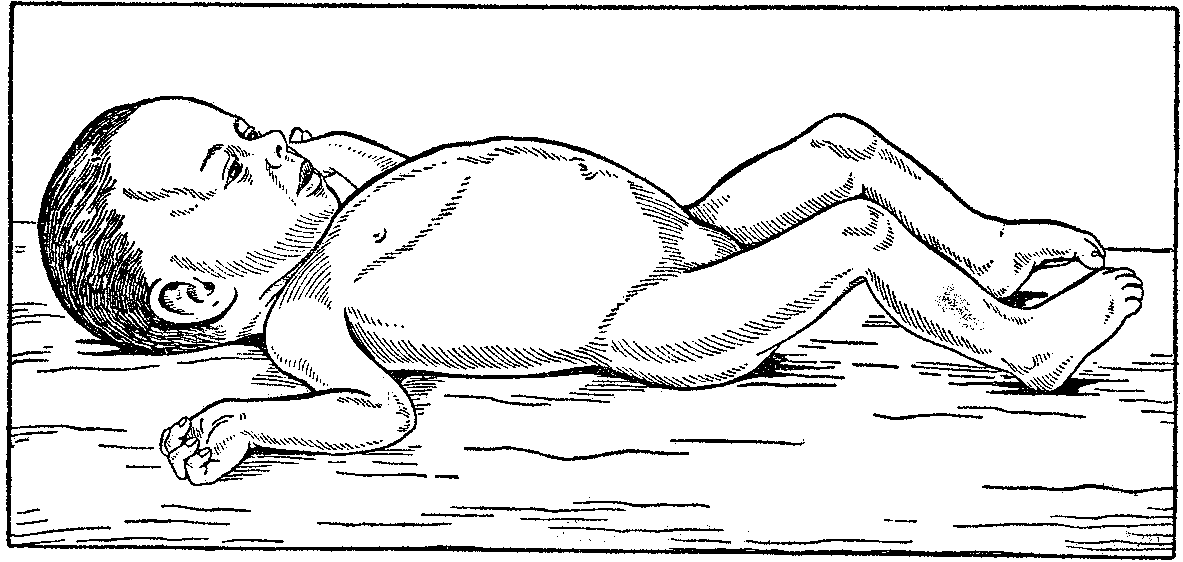 1993; 9: 187-193.
1993; 9: 187-193.
Russman BS, Iannaccone ST, Buncher CR, et al. Новые наблюдения за естественной историей
SMA. J Child Neurol. 1992; 7: 347-353.
Fischbeck KH, Souders D, La Spada A. Ген-кандидат для X-связанной спинальной мышечной атрофии. Adv Neurol. 1991; 56: 209-13.
Goutières F, Bogicevic D, Aicardi J. Преимущественно шейная форма спинальной мышечной атрофии. J Neurol Neurosurg Psychiatry. 1991; 54 (3): 223-5.
Йоханнан М., Патель П., Колаволе Т., Малабарей Т., Махди А.Атрофия мозга при болезни Верднига-Гофмана. Acta Neurol Scand. 1991; 84 (5): 426-8.
Brzustowicz LM, et al., Генетическое картирование хронической мышечной атрофии позвоночника в детском возрасте по хромосоме 5q11.2-13.3. Природа. 1990; 344: 540-41.
Чоу С.М., Гилберт Э.Ф., Чун Р.В. и др. Детская оливопонтоцеребеллярная атрофия со спинальной мышечной атрофией (инфантильная OPCA + SMA). Clin Neuropathol. 1990; 9 (1): 21-32.
Урбанек К. и др., АКТГ и стероиды при болезни Кугельберга-Веландера. Acta Univ Palacki Olomuc Fac Med.1990; 126: 147-50.
Acta Univ Palacki Olomuc Fac Med.1990; 126: 147-50.
Браун Дж. С., Целлер Дж. Л., Суонк С. М., Фурумасу Дж., Варат С.Л. Хирургические и функциональные результаты спондилодеза при спинальной мышечной атрофии. Позвоночник (Phila Pa 1976). 1989; 14 (7): 763-70.
Merlini L, Granata C, Bonfiglioli S, Marini ML, Cervellati S, Savini R. Сколиоз при спинальной мышечной атрофии: естественная история и лечение. Dev Med Child Neurol. 1989; 31 (4): 501-8.
Карни А., Навон Р., Садех М. Дефицит гексозаминидазы А, проявляющийся в виде спинальной мышечной атрофии с поздним началом.Энн Нейрол. 1988; 24 (3): 451-3.
Johnson WG, Wigger HJ, Karp HR, Glaubiger LM, Rowland LP. Ювенильная спинальная мышечная атрофия: новый фенотип дефицита гексозаминидазы. Энн Нейрол. 1982; 11 (1): 11-6.
Эванс Г.А., Дреннан Дж.С., Руссман Б.С. Функциональная классификация и ортопедическое лечение мышечной атрофии позвоночника. J Bone Joint Surg Br. 1981; 63В (4): 516-22.
ИНТЕРНЕТ
Приор Т. В., Руссман Б.С. (Обновлено 27 января 2011 г.). Спинальная мышечная атрофия. В: GeneReviews at GeneTests: Medical Genetics Information Resource (онлайн-база данных).Авторское право, Вашингтонский университет, Сиэтл. 1993-2012 гг. Доступно на http://www.genetests.org. По состоянию на 9 февраля 2012 г.
В., Руссман Б.С. (Обновлено 27 января 2011 г.). Спинальная мышечная атрофия. В: GeneReviews at GeneTests: Medical Genetics Information Resource (онлайн-база данных).Авторское право, Вашингтонский университет, Сиэтл. 1993-2012 гг. Доступно на http://www.genetests.org. По состоянию на 9 февраля 2012 г.
Онлайн-Менделирующее наследование в человеке (OMIM). Университет Джона Хопкинса. Спинальная мышечная атрофия III типа; SMA3. Запись №: 253400. Последнее редактирование 15 ноября 2011 г. Доступно по адресу: http://www.ncbi.nlm.nih.gov/omim/. По состоянию на 9 февраля 2012 г.
Онлайн-Менделирующее наследование в человеке (OMIM). Университет Джона Хопкинса. Спинальная мышечная атрофия I типа; SMA3.Запись №: 253300. Последняя редакция 5 декабря 2011 г. Доступно по адресу: http://www.ncbi.nlm.nih.gov/omim/. По состоянию на 9 февраля 2012 г.
Онлайн-Менделирующее наследование в человеке (OMIM). Университет Джона Хопкинса. Спинальная мышечная атрофия, тип II; SMA2. Запись №: 253550.

 ч.врожденная миотоническая дистрофия)
ч.врожденная миотоническая дистрофия):max_bytes(150000):strip_icc()/level-2-nicu-getty-Alvis-Upitis-56a765b33df78cf772958db0.jpg) Диагноз
сделан анамнезом и осмотром Диагностические исследования ограничены
ценность.
Диагноз
сделан анамнезом и осмотром Диагностические исследования ограничены
ценность.