Что такое гестоз? — Медицинский Центр ADONIS в Киеве
Гестоз, или поздний токсикоз – это осложнение беременности, которое развивается во 2 и 3 триместрах. Заподозрить его развитие на ранних этапах можно по образованию отеков и повышению давления. При этом подтвердить или опровергнуть диагноз можно только по результатам анализов крови и мочи.
Поздний токсикоз, по сравнению с ранним, развивается нечасто. По данным Всемирной организации здравоохранения, его симптомы проявляются в среднем у 8% беременных. При этом на территории стран СНГ этот показатель достигает 10-17%.
Тяжелые формы гестоза встречаются редко, но риск таких осложнений нельзя игнорировать. В отличие от раннего токсикоза поздний несет серьезную угрозу жизни матери и ребенка. Он является одной из основных причин перинатальной заболеваемости и материнской смертности.
Хотя последствия гестоза и кажутся пугающими, не стоит волноваться раньше времени. Во-первых, отеки и гипертензия могут возникать и по другим причинам.
На каком сроке начинается поздний токсикоз
Поздний токсикоз чаще всего начинается после 34 недели беременности, но иногда и на более ранних сроках – уже с 20 недели. Считается, что раннее начало гестоза ассоциируется с тяжелым течением и нередко приводит к преждевременным родам, в том числе путем кесарева сечения.
Причины позднего токсикоза у беременных
Что именно провоцирует развитие гестоза у беременных женщин, не установлено. Существует несколько теорий, имеющих разное количество сторонников, но ни одна из них не позволяет точно определить, у какой женщины будет развиваться поздний токсикоз, а у какой нет.
В группе риска находятся беременные с:
- Гипертонией;
- Заболеваниями почек, печени, желчевыводящих путей, щитовидной железы, надпочечников, легких и/или сердца;
- Нарушением жирового обмена и ожирением;
- Анемией;
- Задержкой развития плода;
- Резус-конфликтом;
- Многоплодной беременностью;
- Родами или абортом в течение последних двух лет;
- В возрасте до 19 лет или после 36.

Вероятность развития позднего токсикоза возрастает на фоне хронических заболеваний. Однако даже при наличии нескольких факторов риска нельзя с уверенностью утверждать, что осложнение будет.
Как проявляется гестоз
При развитии гестоза у женщины сначала происходит спазм всех сосудов и нарушение циркуляции крови, а также ее свертываемости и текучести. Из-за этого может развиваться гипоксия, влияющая на работу сердца, почек, печени, головного мозга и плаценты. В результате в этих органах могут происходить дистрофические изменения.
Выделяют 4 стадии гестоза:
- Отеки;
- Нефропатия;
- Преэклампсия;
- Эклампсия.
На первой стадии поздний токсикоз проявляется отеками на ногах, руках, животе и в области лица и шеи. Чаще всего они не провоцируют значительного ухудшения самочувствия у беременной или развития у нее тяжелых осложнений. Кроме того, при своевременно начатой терапии следующие формы гестоза развиваются не более чем в 20% случаев.
При нефропатии, кроме отеков, появляется гипертония и нарушение функций почек, которое определяется по выделению белка в моче.
Преэклампсия является третьей стадией гестоза, которая развивается всего у 5% беременных женщин. Она характеризуется изменениями в центральной нервной системе, провоцирующими тошноту, рвоту, головную боль и другие симптомы.
Самой сложной стадией позднего токсикоза является эклампсия. При ее развитии патологические нарушения усугубляются, и, кроме перечисленных симптомов, у женщины также появляются судороги, резкое повышение давления и риск инсульта.
В результате позднего токсикоза могут появляться:
- Сильные отеки;
- Повышенное давление;
- Нарушения функций почек, печени и других органов;
- Отслоение плаценты, приводящее к гипоксии плода, замедлению его развития, преждевременным родам и перинатальным патологиям.
При тяжелом течении гестоза состояние беременной женщины может становиться критическим.
Особенности лечения гестоза
Для диагностики гестоза назначают ряд лабораторных анализов крови и мочи, проводят УЗИ, осмотр глазного дна и при необходимости другие обследования.
При легком течении позднего токсикоза беременных, которое проявляется только отеками, акушеры-гинекологи рекомендуют лечение в условиях дневного стационара или дома. Если у беременной также развивается гипертензия, выделяется белок в мочу или проявляются другие симптомы патологий, ей может потребоваться госпитализация в акушерский стационар.
Гестоз (поздний токсикоз беременных) — причины, диагностика и лечение
Слово «токсикоз» не раз приходилось слышать каждой женщине, родившей хотя бы одного ребенка. Осложнение беременности, на протяжении многих лет носящее название позднего токсикоза, с 1996 года стало именоваться термином «гестоз». Это состояние характеризуется глубоким расстройством функции жизненно важных органов и систем.
Гестозы принято разделять на «чистые» и «сочетанные». К «чистым» относят гестозы, которые возникают у беременных женщин, которые ранее никакими заболеваниями не страдали. Но чаще наблюдаются сочетанные гестозы, которые развиваются на фоне предшествовавшего заболевания. Наиболее неблагоприятно протекает гестоз у беременных с гипертонической болезнью, заболеваниями почек (гломерулонефрит, пиелонефрит), печени и желчевыводящих путей (состояния после перенесенного ранее гепатита, нарушение моторики желчевыводящих путей), патологией эндокринных органов (щитовидной железы, поджелудочной железы, надпочечников), нарушениями жирового обмена.
К «чистым» относят гестозы, которые возникают у беременных женщин, которые ранее никакими заболеваниями не страдали. Но чаще наблюдаются сочетанные гестозы, которые развиваются на фоне предшествовавшего заболевания. Наиболее неблагоприятно протекает гестоз у беременных с гипертонической болезнью, заболеваниями почек (гломерулонефрит, пиелонефрит), печени и желчевыводящих путей (состояния после перенесенного ранее гепатита, нарушение моторики желчевыводящих путей), патологией эндокринных органов (щитовидной железы, поджелудочной железы, надпочечников), нарушениями жирового обмена.
Причины
Несмотря на многочисленные исследования, причины и механизм развития гестозов до сих пор окончательно не установлены.
Актуальными в настоящее время считаются несколько теорий:
- Кортикивисцеральная теория рассматривает гестоз как своеобразный невроз беременных с нарушением физиологических взаимоотношений между корой и подкорковыми образованиями головного мозга, ведущим за собой изменения в работе сосудистой системы и нарушение кровообращения.

- По мнению сторонников эндокринной теории , нарушение регуляции сердечнососудистой системы, кровоснабжения внутренних органов, обмена веществ в органах и тканях происходит вследствие изменения функции эндокринных органов, вырабатывающих биологически активные вещества, регулирующие сосудистый тонус, текучесть и свертываемость крови.
- Сторонники
- Выдвижение генетической теории основано на подтвержденном статистикой увеличении частоты гестозов у тех беременных, чьи матери страдали гестозом в период беременности. Не отвергается также существование «генов преэклампсии».
- Положения плацентарной теории основаны на том, что при гестозах отсутствуют характерные для физиологически протекающей беременности изменения в сосудах матки, питающих плаценту.

- В настоящее время большинство исследователей пришли к выводу, что единого механизма развития гестозов не существует, а наблюдается комбинированное воздействие различных факторов, в конечном итоге приводящих к нарушению функции внутренних органов.
Что происходит?
Изменения, происходящие в организме женщины при гестозе, изучены намного лучше, чем их причина. Их основу составляет спазм всех кровеносных сосудов, уменьшение объема циркулирующей крови, изменение свертываемости и текучести крови, нарушение микроциркуляции. Кроме того, при гестозах происходит ослабление работы сердца и уменьшение объема циркулирующей крови. Все это приводит к значительному снижению кровоснабжения тканей с развитием в них дистрофических изменений вплоть до гибели ткани. Органами, наиболее чувствительными к недостатку кровоснабжения, являются почки, печень и головной мозг.
Как проявляется?
В зависимости от проявлений гестозы делят на 4 стадии: отеки беременных, нефропатия, преэклампсия и эклампсия.
Отеки бывают скрытые и явные. На ранней стадии гестоза появляются именно скрытые отеки, связанные с задержкой жидкости в тканях. Понимать это очень важно, поскольку попытка самолечения с помощью мочегонных препаратов не только не уменьшит объем отеков, а только ухудшит общее состояние беременной и плода. Следует помнить, что не все отеки, отмечающиеся при беременности, связаны с гестозом. Не пугайтесь раньше времени, а обязательно посоветуйтесь со своим врачом.
Нефропатия — поражение почек — развивается после 20-ой неделей беременности. Может быть легкой, средней тяжести и тяжелой. Она проявляется тремя основными симптомами: отеки, гипертензия, протеинурия. Гипертензия — повышение артериального давления, систолического («верхнего») на 30 мм рт. ст. от исходного до беременности, а диастолического («нижнего») — на 15 мм рт. ст. и выше. Гипертензия является одним из важных проявлений гестоза, ибо отражает тяжесть спазма сосудов. Протеинурия — это появление белка в моче.
Может быть легкой, средней тяжести и тяжелой. Она проявляется тремя основными симптомами: отеки, гипертензия, протеинурия. Гипертензия — повышение артериального давления, систолического («верхнего») на 30 мм рт. ст. от исходного до беременности, а диастолического («нижнего») — на 15 мм рт. ст. и выше. Гипертензия является одним из важных проявлений гестоза, ибо отражает тяжесть спазма сосудов. Протеинурия — это появление белка в моче.
Преэклампсия — тяжелая стадия гестоза, развивающаяся у 5% беременных, чаще первородящих. При этом на фоне тяжелой нефропатиии (отеки, протеинурия, гипертензия) появляются признаки поражения центральной нервной системы. Женщину беспокоит чувство тяжести в затылке или головные боли, тошнота, рвота, нарушение зрения, возможно неадекватное восприятие происходящего, т.е. изменения в психической сфере. Тяжелая степень преэклампсии выражается преимущественно в нарушении кровоснабжения центральной нервной системы, в частности клеток головного мозга.
Эклампсия — самая тяжелая стадия гестоза, выражающаяся сложным комплексом симптомов, самым характерным из которых являются приступы судорог поперечнополосатой (скелетной) мускулатуры всего тела. Во время приступа из-за скачкообразного подъема артериального давления может произойти разрыв мозгового сосуда, что вызывает инсульт — внутричерепное кровоизлияние. Также вероятна преждевременная отслойка плаценты, что может стать причиной гибели плода.
Проявления гестоза могут быть различными: от растянутой на месяцы малосимптомной формы, которая может даже не беспокоить женщину, до молниеносной и катастрофической по своим последствиям.
Диагностика и лечение
Диагноз «гестоз» ставится на основании клинических и лабораторных данных. Для ранней диагностики заболевания необходима своевременная постановка на учет в женской консультации, обязательны регулярные плановые осмотры гинеколога и тех специалистов, к которым вас отправят на консультацию. Вот примерный перечень мероприятий, которые ожидают вас в том случае, если врач заподозрил у вас гестоз:
- общий анализ крови с определением абсолютного количества эритроцитов и тромбоцитов;
- биохимическое исследование крови с определением количества белка, концентрации электролитов, азота мочевины и креатинина;
- исследование свертывающих и текучих свойств крови;
- анализы мочи: клинический, суточной мочи с определением количества выделенного белка, биохимический;
- контроль диуреза; правильное представление о накоплении жидкости в организме можно получить, сопоставляя ежедневное количество выпитой и выделенной жидкости и измеряя в динамике массу тела;
- измерение артериального давления в динамике на обеих руках, поскольку при наличии распространенного сосудистого спазма возможна значительная разница в показателях АД слева и справа, которая также будет свидетельствовать о глубине происходящих нарушений;
- контроль за массой тела;
- осмотр глазного дна, поскольку состояние сосудов глаза аналогично состоянию сосудов головного мозга и сосудистой системы женщины в целом;
- ультразвуковое исследование, включая допплерометрию плода;
- консультации терапевта, нефролога, невропатолога.

Что касается лечения, то можно сказать, что современная медицина не в состоянии полностью излечить от гестоза, однако в большинстве случаев возможен контроль этого состояния. Своевременное и правильное лечение способствует профилактике тяжелых форм гестоза. Самолечение недопустимо, поскольку без профессионального индивидуального лечения возможно утяжеление гестоза, что приведет к ухудшению состояния как беременной, так и плода.
Принципы лечения гестозов заключаются в следующем:
- создание лечебно-охранительного режима для нервной системы женщины, в зависимости от степени заболевания назначаются различные седативные препараты, от пустырника и валерианы при минимальных проявлениях гестоза до сильнодействующих успокаивающих средств при эклампсии;
- медикаментозное восстановление функции жизненно важных органов;
- своевременное и бережное родоразрешение. При поддающемся лечению гестозе врачи не стимулируют проведение преждевременных родов. Преждевременное родоразрешение проводится при неэффективности проводимого лечения, при ухудшении состояния как беременной, так и ребенка.

Лечение гестозов достаточно индивидуально, и его своевременное начало способно предотвратить развитие тяжелых осложнений. Еще раз повторим: не занимайтесь самолечением! Если врач назначил вам лечение, необходимо дисциплинированно выполнять все его назначения.
Александр Гавриленко
Журнал «9 месяцев» №8 2002
Гестоз при беременности на поздних сроках | Пузёныш — канал для будущих мам
Не каждый раз беременность проходит так, как вы хотели бы. В течение всего срока есть риск возникновения всевозможных неприятностей. Иногда они заключаются в неосложненном токсикозе в первые недели, но могут вылиться и в тяжело протекающий гестоз в последнем триместре. И хотя проводятся различные исследования, механизм и причины развития гестоза до конца не изучены. Так как же распознать гестоз при беременности на поздних сроках и определить клинические симптомы с помощью врача.
Гестоз при беременности на поздних срокахКлинические симптомы и признаки гестоза
Гестоз (другое название – поздний токсикоз) – не самостоятельная болезнь, а клиническое проявление неспособности организма матери гарантировать все потребности плода, который развивается. Поздний гестоз появляется чаще всего с 28 недели беременности и имеет один из следующих ярко выраженных признаков: отеки, протеинурия, гипертензия.
Поздний гестоз появляется чаще всего с 28 недели беременности и имеет один из следующих ярко выраженных признаков: отеки, протеинурия, гипертензия.
Главные признаки проявления позднего гестоза
- Повышенное артериальное давление;
- Отечность;
- Белок в моче.
Степень выраженности симптомов при гестозе:
- I Степень: отечность конечностей, рвота около 5 раз в сутки, обычно наблюдается после приема пищи либо по утрам на голодный желудок, потеря массы примерно до 3 кг;
- II Степень: отечность живота и конечностей, рвота около 10 раз в сутки, не связанная с пищей, потеря в весе 2-3 кг за 10-20 дней, частота пульса около 90-100 ударов в минуту, повышение температуры до 37,0-37,5, понижение артериального давления, у 20-40% женщин обнаруживается ацетон в моче;
- III Степень: отечность касается конечностей, живота, лица и шею, постоянная рвота больше 20 раз в сутки, увеличение температуры до 37,5, частота пульса 100-120 ударов в минуту, пониженное артериальное давление, уменьшение массы тела на 9-10 кг, снижение количества мочи, в анализе мочи может обнаружиться белок, в крови увеличение гемоглобина за счет загустения крови, увеличение креатинина и билирубина, обильное выделение слюны.

Самые первые и зачастую единственные симптомы гестоза – отеки либо водянка. Повышенное давление, характеризующее начало гестоза, наблюдается в районе больше 20% от нормального давления до беременности. Белок в моче в норме совсем отсутствует. Его возникновение указывает на начало третьей стадии гестоза.
Поздний гестоз – это наиболее тяжелое состояние, и для грамотной диагностики/лечения выделяются несколько основных его форм:
- Водянка беременных – первый этап позднего токсикоза. Вследствие водянки у женщин прибавляется лишний вес. Подобное скопление жидкости в женском организме способно добавлять по 0,5–0,8 кг веса за неделю.
- Нефропатия – характеризуется повышением артериального давления и последующих изменений в сердце/почках/печени. Она способна очень быстро развиться в самую тяжелую, и по этой причине необходимо немедленное лечение.
- Преэклампсия – сочетает все перечисленные симптомы, дополнительно возникает белок в моче, тошнота, рвота, головные боли, нарушение зрения, психические расстройства.

- Эклампсия – наиболее тяжелая стадия, добавляются судороги, возникает риск инсульта, преждевременных родов и отслойки плаценты
Лишь в 15% случаев возможны все признаки позднего гестоза, увеличение давления с отечностью – в 32% случаев, повышенное давление с белком в моче – в 12% случаев, белок в моче в сочетании с отечностью – в 3% случаев. При этом явная отечность наблюдается в 25%, а скрытая – в 13% случаев.
Гестоз при беременности на поздних срокахДиагностика гестоза
Диагностировать гестоз несложно. При готовом анамнезе жизни беременной женщины, лабораторных анализов и объективных сведений доктор сможет поставить верный диагноз.Изредка при отсутствии явной отечности, но при большой прибавке в весе, врач может предложить будущей роженице пробу Маклюра-Олдрича: беременной под кожу вводится физиологический раствор и засекается время рассасывания папулы. Если оно составляет 35 минут – то гестоз на поздних сроках беременности подтвердится.
Если вам сложно сгибать пальцы, надевать на них кольца, вы испытываете онемение конечностей – это указывает на отечность.
Множество женщин считают, что для устранения отечности хватит в течение нескольких дней пропить мочегонные средства, что в корне неверно, как и любое самолечение. Это не только не поможет, и скорее наоборот, способно усугубить ваше состояние: сосуды и так потеряли много жидкости, а мочегонные средства лишь увеличат вязкость крови, усугубив протекание болезни и только приблизив поздние стадии гестоза. Не занимайтесь самолечением, своевременно делайте обследования и следуйте советам доктора.
Оригинал статьи размещен здесь:http://puzenush.ru/beremennost/gestoz-pri-beremennosti-na-pozdnix-srokax/
🎈 Если вам понравилась статья, поддержите ее лайком 👍 (ПАЛЕЦ ВВЕРХ). Это поможет другим людям узнать о ней
⚡ Будем признательны, если вы поделитесь статьей в соцсетях со своими друзьями!
✅ Подпишитесь на нас, чтобы получать новые статьи наших авторов первыми!
В погоне за мутациями.
 Гестоза
Гестоза Фото носит иллюстративный характер. Из архива «МВ».
Если у нынешней бабушки, в молодости ожидавшей рождения ребенка, был токсикоз, а у ее беременной дочки — гестоз, то какой диагноз поставить внучке, оказавшейся в интересном положении? Правильный ответ: преэклампсия.
Самое любопытное в этой загадке то, что во всех 3 случаях речь идет об одной и той же патологии, которая характеризуется нарушением взаимодействия между плодным яйцом и материнским организмом. Классическая триада симптомов — отек, протеинурия и гипертензия. Просто в разные времена названия отличались.
В Беларуси заканчивается период, когда врачи по старинке диагностируют гестоз. Вскоре, по примеру других стран, обновятся клинические протоколы диагностики и лечения в акушерстве и гинекологии; тогда наши медики станут использовать современный термин — преэклампсия.
Смысл в «игре слов» есть, поскольку меняется не только классификация, но и представление о природе патологии, а стало быть, и подходы к диагностике, профилактике и лечению. От «токсикоза» в 70-х годах прошлого века отказались потому, что со временем выяснилось: дело, по большому счету, не в токсинах. Гестоз — вообще термин «ни о чем», даже забавный для обозначения болезни: gestatio в переводе с латинского — вынашивание, беременность. Т. е., надо понимать, беременность — болезнь. А вот с эклампсией все ясно: в переводе с древнегреческого — вспышка, внезапное возникновение. Термин в мире используется для классификации острой формы патологии. Соответственно, преэклампсия — форма легкая, предшествующая.
От «токсикоза» в 70-х годах прошлого века отказались потому, что со временем выяснилось: дело, по большому счету, не в токсинах. Гестоз — вообще термин «ни о чем», даже забавный для обозначения болезни: gestatio в переводе с латинского — вынашивание, беременность. Т. е., надо понимать, беременность — болезнь. А вот с эклампсией все ясно: в переводе с древнегреческого — вспышка, внезапное возникновение. Термин в мире используется для классификации острой формы патологии. Соответственно, преэклампсия — форма легкая, предшествующая.
Впрочем, пока не произошла официальная «смена вывески», будем придерживаться действующей классификации.
Именно гестоз фигурирует в отраслевой научно-технической программе «Здоровая мать — здоровое дитя — сильное государство», которая в 2013–2015 годах выполнялась совместно сотрудниками кафедры акушерства и гинекологии БГМУ, специалистами РНПЦ «Мать и дитя» и учеными Института генетики и цитологии НАНБ. Речь шла о разработке комплексного метода диагностики и лечения позднего гестоза, чтобы снизить удельный вес репродуктивных потерь, преждевременных родов и досрочных родоразрешений по экстренным показаниям. Тема завершена, а интересные исследования продолжаются.
Тема завершена, а интересные исследования продолжаются.
— Нашей задачей было выявить генетическую предрасположенность женщин к развитию гестоза, — поясняет профессор кафедры акушерства и гинекологии БГМУ доктор мед. наук Елена Барановская. — Пока нельзя сказать, что ответ на вопрос получен. Но уже собран интересный материал по генетическим вариациям, который обрабатывается статистически и осмысливается. Когда будет существенно пополнена база данных, с помощью клиницистов, генетиков, иммунологов и биохимиков сможем подготовить четкие рекомендации практической медицине. Конечно, предрасположенность к развитию гестоза сопряжена с несколькими генами. Но пока мы тестируем мутацию одного из них — отвечающего за метаболизм фолиевой кислоты (витамина В9). Предполагается, что он имеет отношение к развитию гестоза. Подтверждение тому — факт, что прием фолиевой кислоты за 3 месяца до зачатия (рождение ребенка однозначно должно быть планируемым) и в 1-м триместре беременности предупреждает развитие аномалий плода, минимизирует осложнения.
Доказано, что В9 уменьшает содержание аминокислоты гомоцистеина в крови, тем самым предотвращая патологию эндотелия.
При повышенном содержании гомоцистеина нарушается тонус сосудистой стенки, ее проницаемость, повышается склонность к тромбообразованию, в т. ч. в формирующейся плацентарной системе. А это предрасполагающий фактор для развития гестоза. Измерив концентрацию гомоцистеина, мы, в случае отклонения от нормы, можем рекомендовать прием фолиевой кислоты, витаминов группы В не в профилактической дозе, а в более высокой, но точно рассчитанной…
Когда удастся составить «генетический портрет» гестоза, борьба с ним значительно упростится. Женщине сделают анализ крови и скажут, какова опасность недуга и что предпринять, чтобы минимизировать последствия сбоя генетической программы.
Но уже сегодня, считает Елена Барановская, даже без исследования генотипа есть ответы на многие вопросы. Например, априори тревогу вызывает повышенное артериальное давление. Когда женщина с артериальной гипертензией беременеет, у нее почти гарантированно формируется гестоз. В таком случае ни генетическое тестирование, ни прием фолиевой кислоты ситуацию не поправят. Останется только одно — прибегнуть к паллиативной помощи.
В таком случае ни генетическое тестирование, ни прием фолиевой кислоты ситуацию не поправят. Останется только одно — прибегнуть к паллиативной помощи.
И без генетического анализа известно, что к развитию гестоза предрасполагают лишний вес и сахарный диабет. Кроме того, если гестоз был во время предыдущей беременности, то высока вероятность его повторения.
На бытовом уровне существует предубеждение, что гестоз (ради ребенка, которому лекарства могут навредить) нужно просто перетерпеть, не лечить, он без последствий исчезнет после родов. Это не так. И лечить нужно, и последствия легкомысленного отношения женщины к здоровью — своему и малыша — могут быть тяжелыми (включая нарушения функции почек, печени, сердца и головного мозга).
— Даже в стационаре все сводится к патогенетической и симптоматической терапии, — уточняет Елена Барановская. — О серьезности многих случаев говорит то, что пациенток с тяжелыми формами мы лечим в отделении реанимации Городского клинического роддома № 2 Минска, где находится клиническая база кафедры. С более легкими проявлениями — в отделении патологии беременных или в обсервации (2-м акушерском). Гестоз закладывается на ранних сроках беременности, и, пока она продолжается, избавиться от патологии невозможно. Цель врача — минимизировать проявления, не допустить прогрессирования, избежать тяжелых осложнений для матери и плода, сделать все, чтобы женщина выносила ребенка.
С более легкими проявлениями — в отделении патологии беременных или в обсервации (2-м акушерском). Гестоз закладывается на ранних сроках беременности, и, пока она продолжается, избавиться от патологии невозможно. Цель врача — минимизировать проявления, не допустить прогрессирования, избежать тяжелых осложнений для матери и плода, сделать все, чтобы женщина выносила ребенка.
Каждый день, неделя продленной беременности приближают к физиологическому сроку родов, улучшая прогноз для новорожденного.
Говоря о долговременных последствиях нелеченного гестоза, нужно отметить, что он пагубно влияет на организм матери и плода. Когда нарушается транспорт питательных веществ, ухудшается иммунная функция плаценты, плод получает меньше кислорода, гормонов. При длительной хронической гипоксии — начинает отставать в росте. При выраженной гипертензии у матери может произойти преждевременная отслойка плаценты, тогда возникнет острая гипоксия плода вплоть до его гибели.
Поэтому гестоз считают тяжелой патологией. Застраховаться от него нельзя, но грамотно подготовиться к зачатию и регулярно обследоваться, выполняя все врачебные предписания, — реально.
Застраховаться от него нельзя, но грамотно подготовиться к зачатию и регулярно обследоваться, выполняя все врачебные предписания, — реально.
Дмитрий Патыко
Фото: Евгений Креч
Медицинский вестник, 29 февраля 2016
Поделитесь
Гестоз при беременности на поздних сроках: признаки и лечение
Гестоз – специфическое заболевание, возникающее исключительно на поздних сроках беременности. По медицинской классификации оно относится к поздним токсикозам. При этом больше всего страдают почки, а также сосуды и система кровоснабжения, в том числе плода. Таким образом, гестоз – это патология беременности, осложненная нарушениями функций важнейших систем организма.
Проявляется заболевание триадой клинических признаков, к которым относятся:
- скрытые или явные отеки;
- наличие белка в моче;
-
регулярное повышение давления.
Сочетание любых двух из перечисленных симптомов может свидетельствовать о развитии гестоза при беременности. О серьезности заболевания говорит тот факт, что по статистике оно включено в лидирующую тройку распространенных причин сложных родов (по разным оценкам в 10-15% случаев).
Причины
Диагноз «гестоз» ставится примерно каждой третьей беременной. Невзирая на глубокое изучение патологии, единого мнения о первопричине ее возникновения в медицинской общественности не сформировано. Поэтому в акушерстве ее называют «болезнью гипотез». Приведем наиболее авторитетные из них:
- Главенствующая теория объясняет гестоз нарушением взаимодействия различных отделов головного мозга. Поклонники данного толкования склонны считать его специфическим неврозом беременных, который приводит к негативным изменениям сосудистого русла.
-
Эндокринная концепция определяет главным виновником гормональный сбой, возникающий при беременности.

- Иммунологическая теория говорит об иммунном несоответствии тканей материнского организма и плода.
- Генетическое толкование отсылает к наследственным механизмам, связанным с наличием «генов гестоза».
Большинство практикующих врачей придерживаются мнения, что к состоянию позднего токсикоза приводит совпадение сразу нескольких перечисленных моментов.
Факторы риска
Гестозы подразделяются на два типа: чистые и сочетанные. К первому виду принято относить токсикозы, не обремененные какими-либо прочими недугами. Такое неосложненное течение болезни встречается у 25-30% беременных. Наиболее часто наблюдается второй тип патологии, который возникает на фоне ряда заболеваний. Среди них:
- гипертония;
- заболевания почек, печени;
- гормональные нарушения;
- ожирение;
-
повышенная нервозность, стрессы.

Вероятность осложнения нарастает при слишком ранней (до 18 лет), возрастной (после 35 лет), а также многоплодной беременности.
Хотя точный механизм гестозов до сих пор неясен, врачам удалось разработать систему их прогнозирования. Все беременные проходят специфические обследования и оцениваются врачами по группам риска, чтобы вовремя приступить к надлежащей профилактике и лечению.
Механизм образования
Первые признаки гестоза обнаруживаются после 16-18-й недели беременности, но диагноз, как правило, ставится только в III триместре. При этом в организме образуются соединения, делающие сосуды проницаемыми. Через поврежденные сосуды в различные ткани из крови начинает просачиваться жидкость.
Появляются отеки, которые вначале имеют скрытый характер. Обнаружить их помогает регулярное взвешивание. При этом настороженность должен вызывать неравномерный или чрезмерный набор массы тела (более 300 г в неделю).
Микроповреждения образуются и в почечных сосудах. Через них белок проникает в мочу. Поэтому будущей маме важно сдавать анализы мочи так часто, как предписывает врач. Регулярная диагностика позволяет определить ранние признаки болезни, лечить которые гораздо легче.
На поздних стадиях стойкий спазм сосудов организм компенсирует повышением АД. Более густая кровь имеет высокую свертываемость, поэтому велик риск тромбообразования. Недостаток объема крови в сосудистом русле приводит к неполноценному питанию тканей. Особенно страдают от кислородного дефицита почки и головной мозг. Плацента, которая пронизана огромным количеством сосудов, также чутко реагирует на начальные признаки гестоза.
Виды гестоза при беременности
Развитие гестоза проходит в несколько этапов: от наиболее легкого до тяжелого, который опасен как для жизни женщины, так и плода. Специалисты различают четыре степени болезни, развивающиеся друг за другом.
1. Водянка беременных
Первичным признаком заболевания служат отеки. Сначала отекают ноги, затем живот, грудь, в редких случаях лицо. К вечеру отечность усиливается. Самочувствие женщины, как правило, страдает незначительно. При сильных отеках беременные могут жаловаться на повышенную усталость, ощущать постоянную жажду, тяжесть в ногах.
Однако отеки сами по себе еще не значат наличие гестоза. Ни в коем случае нельзя пытаться избавиться от излишнего накопления жидкости самостоятельно, например, принимая мочегонные препараты. Только акушер-гинеколог может разобраться в причинах возникновения отечности и назначить адекватное лечение.
2. Нефропатия
Если отеки сопровождаются стойким повышением АД и наличием белка в моче, болезнь переходит в следующую стадию – возникает поражение почек. Нефропатия при беременности развивается обыкновенно после 20-й недели.
Для оценки гипертензии женщина должна знать свои обычные показатели АД. О неблагополучии сигнализирует повышение верхних значений на 30, нижних — на 15 мм рт. ст. и более. Особенно тревожным при гестозе считается увеличение диастолического (сердечного) давления. Такая ситуация опасна при беременности, так как может приводить к кислородной недостаточности плода. Типичные жалобы при нефропатии: головная боль, раздражительность, слабость.
О неблагополучии сигнализирует повышение верхних значений на 30, нижних — на 15 мм рт. ст. и более. Особенно тревожным при гестозе считается увеличение диастолического (сердечного) давления. Такая ситуация опасна при беременности, так как может приводить к кислородной недостаточности плода. Типичные жалобы при нефропатии: головная боль, раздражительность, слабость.
3. Преэклампсия
Если не лечить гестоз во время беременности он может перейти в более угрожающую форму. При этом состояние женщины заметно ухудшается. К признакам нефропатии добавляются:
- зрительные нарушения, которые проявляются туманом и мельканием перед глазами «мушек»;
- тошнота;
- ослабление памяти;
- боли под ребрами справа;
- расстройства сна, раздражительность;
- психические отклонения.
При этом развивается почечная недостаточность, нарушается кровообращение в ЦНС, возникает гипоксия плода и другие опасные изменения.
4. Эклампсия
Признак финальной стадии позднего токсикоза – судорожный приступ, чреватый угрозой жизни плода и женщины.
Чем опасен гестоз?
В противоположность раннему токсикозу, гестоз – коварная и тяжелая патология. Тревогу у медиков вызывает непредсказуемость этого состояния. Для него характерно как длительное малосимптомное течение, так и ураганное развитие.
Что делать при подозрении на поздний токсикоз беременности? Ответ банален, но единственно правилен. Необходимо незамедлительно обратиться к гинекологу, пройти соответствующее обследование и грамотное лечение.
В противном случае не исключена угроза здоровью как самой женщины, так и будущего малыша. Даже если признаки патологии не ярко выражены, плод может страдать от кислородного дефицита и отравления токсичными продуктами обмена. Помимо этого, он недополучает необходимые питательные вещества из-за ухудшения кровоснабжения плаценты.
Шкала оценки гестоза
Расшифровка результатов:
- до 7 бал. — легкая степень;
- 8-11 бал. — средняя;
- 12 и более — тяжелая.
Лечение гестоза
На сегодняшний день медицина не располагает панацеей для полного избавления от позднего токсикоза беременности. Однако она научилась контролировать подобные состояния и сводить риск неблагоприятного исхода практически до нуля.
Главное помнить, что любое самолечение недопустимо. Помните о непредсказуемости гестозов и не рискуйте самым дорогим – здоровьем малыша. Легкий гестоз может лечиться дома, но под пристальным наблюдением специалистов. На второй и третьей стадии требуется обязательная госпитализация.
Медикаментозное лечение гестозов строго индивидуальное. По имеющимся показаниям врач может назначить:
- седативные препараты;
- мочегонные средства;
-
лекарства для регулирования давления и кровотока.

Стационарное лечение гестоза заключается во введении через капельницу препаратов плазмы, которые восполняют недостаток белка. Применяются также медикаменты, разжижающие кровь и стимулирующие выделительную функцию. Параллельно проводится терапия плацентарной недостаточности.
Если назначенное лечение не дает ощутимых положительных результатов медики могут принять решение о проведении преждевременных родов. Досрочное родоразрешение проводится чаще всего при помощи кесарева сечения. Но возможны и естественные роды с предварительной гормональной подготовкой.
Диета при гестозе
Беременным с гестозом рекомендован питьевой режим и ограниченное употребление соли. В день не следует выпивать более 1 л жидкости, включая супы и напитки. Показана низко-солевая белковая диета. Основу питания должен составлять животный белок в легкоусвояемой форме.
Предпочтительны диетические сорта мяса (телятина, птица, кролик), морская рыба, творожные продукты. В качестве источника клетчатки и витаминов обогащайте рацион тыквой, свеклой, морской капустой, ягодами, фруктами, зеленью. Отличный источник восполнения жидкости – свежевыжатые соки. Исключите острые, жареные блюда, заменив их паровыми, отварными, запеченными. Не увлекайтесь сладостями и сдобой.
В качестве источника клетчатки и витаминов обогащайте рацион тыквой, свеклой, морской капустой, ягодами, фруктами, зеленью. Отличный источник восполнения жидкости – свежевыжатые соки. Исключите острые, жареные блюда, заменив их паровыми, отварными, запеченными. Не увлекайтесь сладостями и сдобой.
Лучшее лечение гестоза – его предупреждение
Профилактику данного осложнения следует начинать со II триместра беременности. Некоторые акушеры советуют делать это еще на этапе планирования беременности. К важнейшей задаче следует отнести лечение заболеваний, способствующих возникновению гестоза.
Особые меры предосторожности следует предпринять женщинам, знакомым с гестозом по предшествующей беременности. Для них обязательно устранение провоцирующих факторов, таких как стрессы, вредные привычки, переутомление.
Для выявления начальных признаков необходимо следить за динамикой набора веса. Помните, что нормой считается прирост не более 300-400 г за неделю. Не пренебрегайте рекомендациями о прогулках, полноценном сне и отдыхе. Показана гимнастика для беременных, плавание, дыхательные упражнения. Посильная двигательная активность стимулирует кровоток и насыщает ткани необходимым кислородом.
Не пренебрегайте рекомендациями о прогулках, полноценном сне и отдыхе. Показана гимнастика для беременных, плавание, дыхательные упражнения. Посильная двигательная активность стимулирует кровоток и насыщает ткани необходимым кислородом.
Не забывайте, что лучшие друзья будущей счастливой мамы – душевный покой, положительные эмоции и позитивный настрой.
Мне нравится 0
Похожие посты
Оставить комментарий
Внимание: гестоз!
Беременность — важный и ответственный период в жизни любой женщины. Ребёнка мы ждём, как чуда, связываем с его появлением надежды на будущее семейное счастье. Но пока чудо ещё не произошло, надеяться приходится только на себя и на свои силы. Маленький комочек каждый день растёт, изменяется внутри и зачастую требует для полноценного развития больше, чем мы готовы ему дать. Организм женщины не справляется, и возникают различные патологии. Известно, что токсикоз на ранней стадии беременности — явление вполне закономерное и наблюдается не только в человеческом, но и в животном мире. Например, у собак в период щенности часто проявляются такие симптомы, как рвота, отказ от еды, «выборочный» аппетит. А вот поздний токсикоз (другое название — «гестоз») развивается уже на поздних сроках и поражает только беременных женщин. Как и в связи с чем это происходит, мы попытались разобраться, обратившись к заведующей кафедрой акушерства и гинекологии педиатрического факультета Уральской государственной медицинской академии Обоскаловой Татьяне Анатольевне.
ЯМ: Татьяна Анатольевна, что такое гестоз, и чем опасен этот недуг для беременной женщины?
Т. А.: В первую очередь, надо отметить, что гестоз — это осложнение беременности. Вне беременности данное заболевание возникнуть не может. Гестоз поражает различные органы: почки, печень, головной мозг.
А.: В первую очередь, надо отметить, что гестоз — это осложнение беременности. Вне беременности данное заболевание возникнуть не может. Гестоз поражает различные органы: почки, печень, головной мозг.
ЯМ: Опишите, пожалуйста, механизм протекания болезни.
Т.А.: Клиника гестоза начинается с того, что нарушается функционирование плаценты. И именно в плаценте заводятся механизмы болезненных симптомов. Классическими признаками гестоза являются повышение артериального давления, отёки и появление белка в моче. По мере нарастания тяжести гестоза присоединяется плацентарная недостаточность, вследствие чего развивается синдром задержки развития плода, кислородная недостаточность (гипоксия), в некоторых случаях происходит отслойка плаценты. Эклампсия — крайняя тяжесть проявления гестоза. Она характеризуется нарушениями функций головного мозга. У женщины наступает так называемая «судорожная готовность» и, как итог, приступ судорог, во время которого может произойти остановка дыхания у беременной, и погибнуть плод.
ЯМ: Поясните, пожалуйста, как плацентарная недостаточность влияет на развитие гипотрофии или гипоксии плода?
Т.А.: Беременность — особое состояние, при котором ни на минуту не прерывается связь системы «мать — плацента — плод». Когда у женщины повышается давление, то спазм (сужение) сосудов происходит везде, в том числе и в плаценте. Следовательно, и кровь к ребёнку поступает в недостаточных количествах, а ведь именно с ней развивающийся организм получает кислород и питательные вещества. Нехватка питательных веществ приводит к гипотрофии — замедлению роста и развития плода, а недостаток кислорода — к гипоксии.
ЯМ: Что чувствует женщина, страдающая гестозом?
Т.А.: Здесь важно представить процесс протекания болезни: при гестозе происходит спазм мелких кровеносных сосудов всех органов, в результате чего резко снижается количество крови, несущей кислород и питательные вещества. Органы перестают получать необходимое количество кислорода и питательных веществ, поэтому их работа нарушается. Из-за спазма мелких сосудов растет количество крови в крупных кровеносных сосудах, что увеличивает артериальное давление. Жидкость, которая находится в тканях организма, не выводится почками, поэтому появляются отеки, а женщина испытывает жажду, так как кровь становится густой. Изменения в почках ведут к появлению белка в моче. Страдает мозг — могут появляться головные боли и мелькание мушек перед глазами. Тошнота, сухость, зуд кожи, которые испытывает женщина, вызваны изменениями в печени.
Из-за спазма мелких сосудов растет количество крови в крупных кровеносных сосудах, что увеличивает артериальное давление. Жидкость, которая находится в тканях организма, не выводится почками, поэтому появляются отеки, а женщина испытывает жажду, так как кровь становится густой. Изменения в почках ведут к появлению белка в моче. Страдает мозг — могут появляться головные боли и мелькание мушек перед глазами. Тошнота, сухость, зуд кожи, которые испытывает женщина, вызваны изменениями в печени.
ЯМ: Кто входит в группу риска по формированию гестоза?
Т.А.: Это в первую очередь те женщины, у которых есть предшествующие заболевания: гипертония, вегето-сосудистая дистония по гипертоническому типу, пиелонефрит, гломерулонефрит. Если болезнь развилась ещё до зачатия, то, конечно, к ней легче присоединятся симптомы гестоза, и она будет протекать более тяжело на фоне беременности. Кроме того, к группе риска могут быть отнесены девушки-подростки, решившиеся рожать до 18 лет.
ЯМ: Однако поздние роды тоже не приветствуются медиками. Врачи советуют женщинам с хроническим заболеванием почек рожать в более юном возрасте (18-25 лет). Действительно ли это так важно?
Врачи советуют женщинам с хроническим заболеванием почек рожать в более юном возрасте (18-25 лет). Действительно ли это так важно?
Т.А.: Конечно, стаж заболевания играет существенную роль. Одно дело, если он составляет 5-6 лет и совсем другое, если хроническое заболевание продолжается на протяжении 10-15 лет. Опасность развития гестоза, соответственно, увеличивается вдвое.
ЯМ: Можно ли излечить гестоз?
Т.А.: Излечить гестоз невозможно до завершения беременности. Наша задача не допустить развития тяжёлых степеней гестоза. Важно, чтобы болезнь не прогрессировала, а осталась на той стадии, на которой её выявили.
ЯМ: Выходит, если осложнение возникло, то оно будет сопутствовать женщине на протяжении всей беременности. Почему?
Т.А.: При гестозе складывается тревожная картина: кругом отёки, а в кровяном русле, наоборот, гиповолемия — недостаток жидкости. В этой ситуации в материнском организме поднимается артериальное давление — для того, чтобы плод не страдал от недостатка питания. Снижая артериальное давление матери, тем самым мы угнетаем жизнедеятельность ребёнка, который тут же своим стрессовым состоянием его вновь поднимает. Получается замкнутый круг.
Снижая артериальное давление матери, тем самым мы угнетаем жизнедеятельность ребёнка, который тут же своим стрессовым состоянием его вновь поднимает. Получается замкнутый круг.
ЯМ: Как распознать гестоз на ранней стадии?
Т.А.: Распознать гестоз довольно сложно. Отёки, например, возникают при нарушении кровообращения в нижних конечностях, при венозной недостаточности. Водянка может быть следствием патологии почек самой по себе. Повышенное давление часто беспокоит женщин при гипертонической болезни. Поэтому наша задача в том, чтобы отличить ту гипертонию, которая развилась раньше, от той, которая возникла во время беременности. То же касается и пиелонефрита. А гломерулонефрит вообще очень сложно отличить от гестоза, потому что при этом заболевании могут появиться и отёки, и гипертония, и белок в моче.
ЯМ: Какой симптом при гестозе даёт обычно знать о себе первым?
Т.А.: Даже патологическая прибавка веса уже может послужить тревожным сигналом. Отёки внешне ещё никак не проявились, но жидкость уже задержалась в организме. А это как раз и свидетельствует о нарушении функции почек.
А это как раз и свидетельствует о нарушении функции почек.
ЯМ: Достаточное ли это основание для госпитализации?
Т.А.: С диагнозом водянка мы обычно не кладём в круглосуточный стационар. А вот если к отёкам присоединяются ещё такие симптомы, как гипертония и повышенный уровень белка в моче, то это, однозначно, показание к стационарному лечению.
ЯМ: Как можно в домашних условиях помочь своему организму? Существуют ли эффективные народные средства?
Т.А.: В данной ситуации главное — не навредить организму. Для того чтобы справиться с отёками, иногда достаточно нормализовать питание и выровнять режим дня, побольше отдыхать. Мочегонные средства принимать строго противопоказано, их действие может только усугубить болезнь. Отёки, скорее всего, спадут, зато поднимется артериальное давление. А вот кислородные коктейли попить можно. Они оказывают благотворное влияние на весь организм в целом. Но здесь опять нужно быть осторожным — коктейли, приготовленные на основе яичного белка, лучше не употреблять, так как существует опасность заразиться сальмонеллезом. От банных процедур тоже следует воздержаться, они могут спровоцировать гипертонию. Баню отлично заменит контрастный душ. К тому же, это ещё и хорошая тренировка для сосудистого тонуса.
От банных процедур тоже следует воздержаться, они могут спровоцировать гипертонию. Баню отлично заменит контрастный душ. К тому же, это ещё и хорошая тренировка для сосудистого тонуса.
ЯМ: В каких случаях гестоз может служить показанием к досрочным родам и кесареву сечению?
Т.А.: При лёгкой степени приэклампсии беременность можно доносить практически до срока (36-37 недель). Но если гестоз доходит до тяжёлой стадии, то тогда уже остро встаёт вопрос об экстренном родоразрешении и зачастую об операции «кесарево сечение».
ЯМ: Каковы последствия гестоза для матери и ребёнка?
Т.А.: Если говорить о младенце, то для него будет последствием не гестоз сам по себе, а то, как успел сформироваться плод. Были ли это роды своевременные или преждевременные, родился ребёнок с нормальной массой тела или недостаточной. Длительное кислородное голодание может стать причиной перинатальных поражений нервной системы. Проявляется оно обычно сниженной как физической, так и умственной активностью, снижением тонуса мышц, неправильными рефлексами. Зачастую неврологические проявления связывают с родовой травмой, а на самом деле ? это проявление гипоксии.
Зачастую неврологические проявления связывают с родовой травмой, а на самом деле ? это проявление гипоксии.
У мамы ребёнка ненормальная функция почек и сосудистого тонуса, которая возникла во время беременности, может закрепиться на будущее и, как следствие, сформироваться гипертоническая болезнь.
ЯМ: Как долго могут держаться симптомы гестоза в послеродовом периоде?
Т.А.: Обычно симптомы держатся несколько дней. При тяжёлом гестозе зачастую приходится переводить пациентку в терапевтическое отделение, чтобы нормализовать у неё давление или функцию почек. Если же признаки гестоза продолжаются месяца два, то это уже может свидетельствовать о том, что патология беременности перешла в болезнь. В таких случаях нужно незамедлительно обращаться к терапевту по месту жительства.
ЯМ: Как избежать такого осложнения как гестоз? Существует ли профилактика позднего токсикоза?
Т.А.: Причины развития гестоза специалистам пока неизвестны. Но ясно одно — организм мамы не может правильно приспособиться к развитию плода, в результате чего и возникают множественные нарушения. Одной из предпосылок к развитию гестоза является неправильно заложенная плацента. Такое нарушение обычно возникает из-за болезней, приобретённых ещё до зачатия. Поэтому чтобы избежать осложнения, профилактику лучше начинать до беременности (за несколько месяцев, а не дней). Это касается не только хронических заболеваний, но и таких очагов инфекции, как кариозные зубы, ангина, инфекции, передающиеся половым путем. Важные составляющие профилактики — режим дня и рациональное питание, прогулки на свежем воздухе. Продолжительность сна не менее 9 часов в сутки. Правильное питание — одно из основных условий благополучного течения беременности. Пища должна быть разнообразной и содержать все питательные вещества: белки, жиры, углеводы, витамины, микроэлементы. До 20 недель беременности рекомендуется четырехразовое питание, а после 20 недель — уже пяти-шестиразовое, последний прием пищи — за три — два с половиной часа до сна.
Одной из предпосылок к развитию гестоза является неправильно заложенная плацента. Такое нарушение обычно возникает из-за болезней, приобретённых ещё до зачатия. Поэтому чтобы избежать осложнения, профилактику лучше начинать до беременности (за несколько месяцев, а не дней). Это касается не только хронических заболеваний, но и таких очагов инфекции, как кариозные зубы, ангина, инфекции, передающиеся половым путем. Важные составляющие профилактики — режим дня и рациональное питание, прогулки на свежем воздухе. Продолжительность сна не менее 9 часов в сутки. Правильное питание — одно из основных условий благополучного течения беременности. Пища должна быть разнообразной и содержать все питательные вещества: белки, жиры, углеводы, витамины, микроэлементы. До 20 недель беременности рекомендуется четырехразовое питание, а после 20 недель — уже пяти-шестиразовое, последний прием пищи — за три — два с половиной часа до сна.
Основным в рационе питания беременной является белок — 250 граммов в сутки. При этом 70% — доля животных белков (рыба, мясо, птица, яйца, творог, сыр). Остальные 30% — растительный белок (бобовые, крупы, орехи). Потребность в жирах составляет около 80 граммов в сутки, из них 40 граммов — животные жиры (сливочное масло, сметана) и 40 граммов — растительные жиры. Необходимое количество углеводов в сутки — 400-450 граммов (преимущественно фрукты, овощи, капуста, зеленый салат, а также хлеб, крупы, макароны, сухофрукты). В период беременности следует ограничить употребление сахара, кондитерских изделий, сладких десертов, газированных сладких напитков. Прием жидкости до 22 недель — 1,5 литра в сутки, после 22 недель — 1-1,2 литра. Количество соли в сутки — не более 6-8 граммов. Желательно исключить из рациона копченые, соленые, острые, жареные продукты, крепкие куриные и мясные продукты. Потребность организма в витаминах во время беременности значительно возрастает. К сожалению, витаминов, содержащихся во фруктах, овощах и других продуктах, не хватает, поэтому важно принимать витамины для беременных («Элевит», «Пренатал», «Прегнавит» и др.
При этом 70% — доля животных белков (рыба, мясо, птица, яйца, творог, сыр). Остальные 30% — растительный белок (бобовые, крупы, орехи). Потребность в жирах составляет около 80 граммов в сутки, из них 40 граммов — животные жиры (сливочное масло, сметана) и 40 граммов — растительные жиры. Необходимое количество углеводов в сутки — 400-450 граммов (преимущественно фрукты, овощи, капуста, зеленый салат, а также хлеб, крупы, макароны, сухофрукты). В период беременности следует ограничить употребление сахара, кондитерских изделий, сладких десертов, газированных сладких напитков. Прием жидкости до 22 недель — 1,5 литра в сутки, после 22 недель — 1-1,2 литра. Количество соли в сутки — не более 6-8 граммов. Желательно исключить из рациона копченые, соленые, острые, жареные продукты, крепкие куриные и мясные продукты. Потребность организма в витаминах во время беременности значительно возрастает. К сожалению, витаминов, содержащихся во фруктах, овощах и других продуктах, не хватает, поэтому важно принимать витамины для беременных («Элевит», «Пренатал», «Прегнавит» и др. ). Недостаток фолиевой кислоты в организме, особенно на ранних стадиях беременности, ведет к порокам развития плода. Поэтому её необходимо принимать за 1-3 месяца до планируемой беременности и в течение ее первых 12 недель по 400 микрограммов в день.
). Недостаток фолиевой кислоты в организме, особенно на ранних стадиях беременности, ведет к порокам развития плода. Поэтому её необходимо принимать за 1-3 месяца до планируемой беременности и в течение ее первых 12 недель по 400 микрограммов в день.
ЯМ: Подведём итог. Перечислите, пожалуйста, основные моменты, на которые женщине необходимо обратить внимание, чтобы избежать осложнений во время беременности?
Т.А.: В первую очередь, планировать беременность вовремя — то есть тогда, когда организм уже готов к предстоящему испытанию — не в подростковом возрасте. Но и не затягивать, разумеется. По возможности избежать абортов, особенно при первой беременности. Важно также именно планировать беременность, то есть заранее подлечить все заболевания, которые могут в дальнейшем спровоцировать патологию. Во время беременности — правильное, сбалансированное питание, прогулки на свежем воздухе, полноценный отдых и регулярное наблюдение у гинеколога. Соблюдать эти рекомендации нетрудно, избавиться от последствий в будущем гораздо сложнее.
*Статистика: Гестоз беременных остается одной из актуальных проблем современного акушерства. Заболевание стабильно занимает 2 место в структуре причин материнской и детской смертности. Частота его составляет от 12 до 27% от общего количества родов.
*При лёгкой и средней степени гестоза преждевременно родятся 8-9% детей, при тяжёлой — 19-20%, при переходе гестоза в стадию эклампсии — до 32% детей. Низкую массу тела имеют 30-35% младенцев, рождённых у женщин с диагнозом «гестоз».
Словарик:
Вегето-сосудистая дистония — одно из проявлений вегетативных неврозов, протекающее с выраженными колебаниями сосудистого тонуса. При вегето-сосудистой дистонии больные жалуются, прежде всего, на боли в области сердца, возникающие после переживаний, конфликтных ситуаций. Раньше таким больным ставили диагноз «кардионевроз» или «невроз сердца».
«Водянка» — отёки нижних конечностей у беременных.
Гипертония — хроническая болезнь, характеризующаяся постоянным или почти постоянным повышением артериального давления. Последствия артериальной гипертонии уносят больше жизней, чем СПИД, раковые заболевания и туберкулез, вместе взятые.
Последствия артериальной гипертонии уносят больше жизней, чем СПИД, раковые заболевания и туберкулез, вместе взятые.
Гломерулонефрит характеризуется преимущественным поражением клубочкового аппарата почек, является частой причиной развития хронической почечной недостаточности.
Пиелонефрит — воспаление ткани почки.
Эклампсия — высшая стадия позднего токсикоза. Тяжелое состояние указывает на нарушение деятельности всех важнейших систем и органов. Самый значительный симптом — судороги мускулатуры тела, сопровождающиеся потерей сознания (кома). Эклампсия, как правило, возникает в моменты родов, реже — после и во время беременности.
Гестоз при беременности на поздних сроках – признаки и профилактика
Гестоз – тяжелое состояние
Гестоз еще называют вторым токсикозом, только возникает он, как правило, на поздних сроках. И если токсикоз считается вполне нормальным для беременности явлением, то гестоз относят к осложнениям. Это состояние связано с нарушением нормальной работы ряда органов. В зависимости от симптомов гестоз подразделяют на четыре степени «тяжести» — водянка беременных, нефропатии, преэклампсия и эклампсия. Начиная от обычных отеков на теле будущей мамы, гестоз может стать реальной угрозой жизни матери и ребенка, если качественное лечение не будет проведено вовремя. Вот почему «позднего токсикоза» все так опасаются.
Это состояние связано с нарушением нормальной работы ряда органов. В зависимости от симптомов гестоз подразделяют на четыре степени «тяжести» — водянка беременных, нефропатии, преэклампсия и эклампсия. Начиная от обычных отеков на теле будущей мамы, гестоз может стать реальной угрозой жизни матери и ребенка, если качественное лечение не будет проведено вовремя. Вот почему «позднего токсикоза» все так опасаются.
В основном женщины сталкиваются с гестозом во время первой беременности. В группе риска – обладательницы хронических заболеваний, проблем с почками, давлением или печенью, избыточным весом, беременные несколькими малышами, те, кто младше двадцати и старше тридцати пяти лет. Но, к счаcтью, если в первую беременность мама не столкнулась с гестозом, во вторую и последующие познакомиться с ним шансов еще меньше.
О том, по каким причинам у беременных женщин развивается гестоз, спорят десятилетиями. По одной версии, из-за нарушения кровообращения в коре головного мозга, по другой – по причине расстройства работы гормонов в различных органах, по третьей – из-за иммунологической несовместимости матери и плода. Есть также мнение, что гестоз в основном передается по наследству. В любом случае, это довольно серьезное заболевание для беременной пациентки, которое, к счастью, поддается лечению и профилактике.
Есть также мнение, что гестоз в основном передается по наследству. В любом случае, это довольно серьезное заболевание для беременной пациентки, которое, к счастью, поддается лечению и профилактике.
Признаки гестоза
Источник фото:
shutterstock.com
Обычно гестоз возникает ближе к третьему триместру беременности. Эта болезнь коварна и может длительной время проходить скрыто, и будущие мамы, уже привыкшие к дискомфорту, не уделяют им должного внимания. Насторожить должны внезапный набор массы тела, обнаружение белка в анализе мочи, повышенные показатели давления и отекшие конечности. Кстати, именно поэтому гинеколог на каждом приеме большое внимание уделяет всем этим параметрам. На следующей стадии гестоза о себе дают знать боль в голове, тошнота и рвота, пелена и мушки перед глазами. Возникает реальный риск внутричерепного кровоизлияния, то есть инсульта, или отслойки плаценты, что может привести уже к гибели плода.
Гестоз может долгое время проходить без ярко выраженных тревожных симптомов, а может разрушить жизнь мамы и ее малыша за считанные дни. Это – один из аргументов того, почему необходимо вовремя проходить все обследования у гинеколога и сдавать анализы столько раз, сколько этого требует врач.
Первая «стадия» гестоза – так называемая водянка беременных — знакома многим женщинам. Жидкость задерживается в организме, из-за чего отекают руки, ноги и лицо. Иногда отеки бывают скрытыми, их наличие выдает только патологическая прибавка беременной женщины в весе. В норме женщина в положении должна прибавлять не больше четырехсот граммов в неделю.
Отеки, в свою очередь, тоже разделяются специалистами на степени: первая – отеки голеней, вторая – голени и живота, третья – ног, передней области живота и лица, четвертая степень – распространение отеков на ноги, туловище, руки и лицо. Неопытному человеку можно попробовать определить отеки, нажав на участок кожи и отпустив палец: если белый след будет оставаться на коже в течение какого-то времени, значит, отек есть.
Еще одна характерная черта этой патологии – наличие белка в моче и его прогрессирующее увеличение. Одновременно с этим у беременной женщины стремительно убывает ежедневный объем выделяемой мочи, до полулитра в день и меньше, что считается очень скудным количеством. Тогда уже врачи говорят о нефропатии, и чем она дольше протекает, тем хуже прогноз состояния будущей мамы. То же самое касается и ежедневного объема мочи: чем меньше – тем хуже.
Если беременная женщина и на этом этапе не обратиться за помощью к специалистам, гестоз продолжит развиваться и перейдет уже в стадию преэклампсии. К уже имеющимся симптомам прибавятся нарушения в работе центральной нервной системы. Сначала это головная боль, тошнота и рвота, тяжесть в затылке, дискомфорт в желудке и правом подреберье, а затем – нарушения зрения в виде «мушек» или «искр» перед глазами и даже возможные пробелы в памяти. Преэклампсия свидетельствует о том, что кровообращение нарушилось уже в головном мозге, а сетчатка глаз поражена.
Эклампсия
Источник фото: shutterstock.com
Самая неприятная степень гестоза – эклампсия, когда появляются судорожные припадки длительностью до нескольких минут. Возникают приступы при внешних раздражителях вроде яркого света, громкого звука или стрессовой ситуации.
Чаще всего приступ начинается с судорог мышц лица, которые распространяются на руки, ноги, а затем и мускулатуру всего тела. Взгляд останавливается, глаза закатываются, а кисти сжимаются в кулаки. Примерно через полминуты начинаются тонические судороги – человек выгибается, запрокидывает голову, сжимает челюсти. Кожа синеет, может прекратиться дыхание и наступить потеря сознания. Такое состояние может привести к смерти беременной или уже клоническим судорогам, когда женщина бьет руками и ногами.
Припадок эклампсии прекращается через несколько минут, у человека выделяется пена изо рта, появляется хриплое дыхание, судороги стихают. Еще через полминуты кожа беременной приобретает розовый оттенок, дыхание становится нормальным, зрачки — прежними. Женщина испытывает слабость и совершенно ничего не помнит о только что произошедшем припадке. Следующий такой приступ может начаться при появлении любого внешнего раздражителя.
Гестоз будет протекать еще тяжелее, если он «сочетанный», то есть развился при наличии у беременной женщины хронических заболеваний. Диагноз может вызвать также осложнения – отек легких, кровоизлияние в кишечник, печень или другие жизненно важные органы. Кроме того, при гестозе есть риск того, что начнет отслаиваться изначально нормально расположенная плацента, что приведет к гипоксии плода и возможной задержке развития младенца.
Лечение гестоза
При лечении гестоза медики стремятся положить беременную пациентку «на сохранение», восстановить функции пораженных органов и организовать быстрое и безопасное родоразрешение.
Водянку начальной стадии могут лечить гинеколог и терапевт в женской консультации, при средней степени тяжести – в условиях дневного стационара. Пациенток с тяжелой стадией гестоза уже госпитализируют в специализированные клиники с реанимационным отделением и возможностями для выхаживания недоношенных малышей.
Пациенток с тяжелой стадией гестоза уже госпитализируют в специализированные клиники с реанимационным отделением и возможностями для выхаживания недоношенных малышей.
Лечение гестоза – это целый набор мер, где нельзя упускать ни одной меры. Именно поэтому врачи будут действовать комплексно и наверняка порекомендуют беременной следующее:
- Рацион с увеличенным количеством белка, витаминов и минералов;
- Сокращение количества выпитой жидкости и соли;
- Препараты с успокаивающим эффектом;
- Медикаменты, улучшающие кровообращение, внутривенно;
- Препараты, снижающие повышенное артериальное давление;
- Профилактика плацентарной недостаточности;
- Мочегонные средства для уменьшения отеков.
Если все меры не приводят к результату и уменьшению степени гестоза, единственным возможным вариантом решения проблемы остаются роды, чаще всего методом кесарева сечения.
Профилактика гестоза
Источник фото: shutterstock.com
Чтобы не сталкиваться со всеми перечисленными выше ужасами, гестоз лучше вовремя предотвратить, тем более что профилактика этого заболевания не является чем-то невероятно сложным. Скорее наоборот, это – набор необходимых мер по поддержанию здоровья беременной женщины и ее будущего малыша.
Итак, не допустить развития гестоза помогут следующие меры:
- Правильное питание, ограниченное потребление сладкого и мучного, пряного и копченого, соленого и жареного.
- Потребление достаточного количества чистой питьевой воды. Оптимальный объем для беременной женщины – около одного литра, но не более 1,2 л.
- Умеренная физическая активность, длительные пешие прогулки на свежем воздухе.
- Отвар шиповника и клюквенный морс – как профилактика отеков во время беременности.

- Прием лекарственных препаратов для профилактики отеков, если их порекомендовал врач. Чаще всего беременным советуют принимать Цистон, Цистенал и Канефрон.
- Регулярное посещение консультаций гинеколога и своевременная сдача анализов крови и мочи.
- Отслеживание своего веса и артериального давления.
- Достаточный сон (7-8 часов).
Если пациентка находится в группе риска, вероятнее всего ей необходимо будет пройти медикаментозную профилактику гестоза, задача которой будет оптимизировать работу важных органов и систем организма, а также обеспечить нормальную свертываемость крови.
С диагнозом «гестоз» не пожелала бы столкнуться ни одна будущая мама, однако список мер по профилактике этого состояния говорит сам за себя – болезнь совсем не сложно предотвратить. В этом же заинтересован и любой врач, контролирующий ход беременности своих пациенток. Поэтому не стоит жаловаться на постоянную сдачу анализов и проверку веса – эти показатели действительно важны в период ожидания вашего ребенка.
Что такое гестоз? Признаки, симптомы и решения
Гестоз — общий термин для обозначения ряда заболеваний, связанных с беременностью. Если вы заметили какие-либо признаки этого состояния, немедленно примите меры, чтобы минимизировать риск для матери и будущего ребенка. Вот на что обращать внимание:
Гестоз — это общий термин для обозначения различных заболеваний, которые возникают только во время беременности. Некоторые называют это токсемией или разновидностью отравления при беременности, поскольку оно вызывает симптомы, включая высокое кровяное давление и гипертонию.Мы не знаем, что именно вызывает преэклампсию или токсемию, и симптомы могут варьироваться от человека к человеку. Эти симптомы могут появиться впервые во время беременности или из-за ранее существовавших состояний у беременной женщины .
Есть разница между появлением симптомов до или после 20-недельной отметки. Ранние признаки включают легкую и тяжелую тошноту по утрам . К поздним гестозам относятся преэклампсия (ранее называвшаяся токсемия ) и тяжелые формы эклампсии, сопровождающиеся повышением артериального давления, протеинурией, задержкой воды, нарушениями функции печени и почек.
Почти все беременные женщины в первом триместре обычно страдают от утреннего недомогания, которое включает чувство тошноты и периодическую рвоту. Однако по сравнению с «нормальным» утренним недомоганием с гиперемезис беременных протекает гораздо тяжелее. Симптомы включают сильную чувствительность к запахам и позыв к рвоте, чувствительность к свету, чувство обморока и учащенное сердцебиение. страдающих чрезмерной рвотой воспринимают это как тяжелое испытание. Частая рвота может вызвать симптомы дефицита и нарушения водного и минерального баланса.В крайних случаях могут потребоваться инфузии, чтобы обеспечить беременной женщине все потребности в жидкости и питательных веществах.
Типичные симптомы преэклампсии , такие как повышение артериального давления и задержка воды. Это состояние обычно проявляется только во второй половине беременности. Преэклампсия очень редко возникает в первой половине беременности.
Это состояние обычно проявляется только во второй половине беременности. Преэклампсия очень редко возникает в первой половине беременности.
Преэклампсия может быть различной степени тяжести. Легкая преэклампсия встречается довольно часто, т.е. е. она есть у каждой десятой матери, впервые родившей ребенка. Будущие мамы почти не замечают легкой формы. Гинеколог может определить симптомы преэклампсии. По этой причине при каждом обследовании проверяется артериальное давление и моча на белок. Лечение варьируется в зависимости от тяжести преэклампсии. Регулярный контроль артериального давления необходим для всех форм. Если повышение артериального давления слишком велико, врачи назначат лекарства для его снижения. В случае тяжелой преэклампсии будущая мама помещается в больницу для тщательного наблюдения .
Это редкое, но опасное состояние с припадками, которые угрожают здоровью будущего ребенка и матери. Эклампсия может возникнуть во время беременности и родов, а также в последующие дни. Будущая мама должна немедленно обратиться в больницу , так как это состояние может вызвать такие осложнения, как острая почечная недостаточность, отек мозга, тромбозы, повреждение сетчатки, кровотечение и недостаточность плаценты. Признаки и симптомы эклампсии включают мерцающее зрение, дискомфорт, сильные головные боли и судороги .
Будущая мама должна немедленно обратиться в больницу , так как это состояние может вызвать такие осложнения, как острая почечная недостаточность, отек мозга, тромбозы, повреждение сетчатки, кровотечение и недостаточность плаценты. Признаки и симптомы эклампсии включают мерцающее зрение, дискомфорт, сильные головные боли и судороги .
Долгое время HELLP-синдром считался самым тяжелым осложнением гестоза. Однако, согласно последним данным, симптомы могут возникать внезапно без предшествующих признаков гестоза.
Доктор Луис Вайнштейн использовал термин HELLP-синдром в 1982 году для описания следующих симптомов:
- H Гемолиз — разрушение или разрушение эритроцитов
- EL Повышенные ферменты печени
- LP Низкое количество тромбоцитов
A полностью развитый HELLP-синдром ставит под угрозу жизнь матери и ее будущего ребенка.Поэтому в большинстве случаев врачи решают без промедления выполнить кесарево сечение . Во многих случаях мать должна быть помещена в реанимацию. На сегодняшний день четко не выяснено, что вызывает синдром HELLP. Обычно он развивается в течение нескольких часов с болью в правой верхней части живота и появлением отека и задержки воды в конечностях и / или лице.
Во многих случаях мать должна быть помещена в реанимацию. На сегодняшний день четко не выяснено, что вызывает синдром HELLP. Обычно он развивается в течение нескольких часов с болью в правой верхней части живота и появлением отека и задержки воды в конечностях и / или лице.
Другие симптомы, которые могут указывать на HELLP-синдром, включают:
- Нарушение зрения
- Изменение цвета кожи на желтый
- Внезапная тошнота
- Диарея
- Или сильный зуд кожи
Профилактических мер в настоящее время не существует.К счастью, HELLP-синдром — это редкое состояние , которое статистически встречается только в 0,2–0,85% всех беременностей.
Поскольку на сегодняшний день не существует эффективной профилактики различных гестозов, особенно важно воспользоваться преимуществами пренатальных скрининговых тестов . Информацию о медицинской помощи во время беременности и после родов можно получить в Центрах по контролю и профилактике заболеваний. В рекомендациях указываются тип и объем необходимой медицинской помощи и приводятся отчеты о большинстве проверок, выполняемых врачами.
В рекомендациях указываются тип и объем необходимой медицинской помощи и приводятся отчеты о большинстве проверок, выполняемых врачами.
Хотя эти процедуры могут показаться сложными, помните, что вы не одиноки! Друзья, семья и группы поддержки также могут предоставить вам отличную информацию и поддержку во время беременности. Но если у вас есть дополнительные медицинские вопросы, обязательно спросите своего врача, чтобы получить оптимальную медицинскую помощь.
Липидно-белковые комплексы в мембране эритроцитов при позднем гестозе
В. Р. Акоев, С. П. Щербинина, А. В. Матвеев, и др. , Бюл. Эксп. Биол. Med., 123 , № 3, 279-284 (1997).
Google ученый
Болдырев А.А., Курелла Э.Г., Павлова Т.Н., Биологические мембраны , Москва (1992).
Колосова М.В., Новицкий В.В., Степовая Е.Л., Кравец Е.Б., Бюлл. Эксп. Биол. Med. , 129 , № 3, 306-309 (2000).
Google ученый
Лебеденко В.С., Перекисное окисление липидов, плацентарная недостаточность и малолетние плоды , Автореф. Med. Sci. Москва (1988).
А.Г. Максина, Н.П. Микаелян, Б.А. Дайняк, Ю. А. Князев, Биофизика , 39 , № 3, 475-478 (1994).
PubMed Google ученый
А.Г. Максина, Н.П. Микаелян, Т.Г. Тареева, и др. , Вопр.Med. Хим. , № 1, 34–37 (2000).
, Вопр.Med. Хим. , № 1, 34–37 (2000).
Н.П. Микаелян, Нарушение состояния плода и энергетического обмена у беременных с хроническими неспецифическими заболеваниями легких , Автореф. Med. Sci. Москва (1993).
Н.П. Микаелян, Ю. А. Князев, А. Г. Максина, А. В. Микаелян, Вестн. Россияйск. Акад. Med. 1997. Т. , № 7. С. 54-56.
Текучесть мембран в биологии , Под ред.Р. Эллиот, Киев (1989).
M. Bryszewska, C. Watala, W. Tozzecka, Br. J. Haematol. , 62 , № 1, 111-116 (1986).
PubMed Google ученый
I. M. C. Cuttaridge, FEBS Lett. , 157 , № 1, 37-40 (1983).
PubMed Google ученый
E. D. Harris, Soc.Exp. Биол. Med. , 28 , 130-140 (1994).
Google ученый
П. Клилхолма, К. Пол, П. Пакаринен и М. Гронроос, Acta Obstet. Гинеколь. Сканд. , 63 , № 7, 629-631 (1984).
PubMed Google ученый
N. Nimeh and R. Bishop, Med. Clin. N. Am. , 64 , 631-645 (1980).
PubMed Google ученый
C. Watala, Ann. Акад. Med. (Лондон) , 33 , №№ 3-4, 5-33 (1995).
Google ученый
| ||||||||||||||||||||||||||||||||||||||||||
эклампсия | Вы и ваши гормоны от Общества эндокринологов
Альтернативные названия для преэклампсии
Преэкламптическая токсемия; ДОМАШНИЙ ПИТОМЕЦ; Гестоз EPH; метаболическая токсемия на поздних сроках беременности
Что такое преэклампсия?
Преэклампсия — это заболевание, которое встречается примерно в 5% всех беременностей. Хотя широко распространено мнение, что происхождение преэклампсии лежит в событиях первых четырех-восьми недель беременности, симптомы возникают в середине и на поздних сроках беременности и обычно включают высокое кровяное давление у матери и белок в ее моче. Чем тяжелее преэклампсия, тем выше риск серьезных осложнений для матери и ребенка. Легкая преэклампсия может вызвать несколько симптомов; однако тяжелая преэклампсия может привести к серьезным осложнениям для матери и ребенка с риском смерти.
Хотя широко распространено мнение, что происхождение преэклампсии лежит в событиях первых четырех-восьми недель беременности, симптомы возникают в середине и на поздних сроках беременности и обычно включают высокое кровяное давление у матери и белок в ее моче. Чем тяжелее преэклампсия, тем выше риск серьезных осложнений для матери и ребенка. Легкая преэклампсия может вызвать несколько симптомов; однако тяжелая преэклампсия может привести к серьезным осложнениям для матери и ребенка с риском смерти.
Только у 1 из 100 женщин с преэклампсией развивается полная эклампсия — тип приступа и опасное для жизни осложнение преэклампсии. В Великобритании около шести женщин и несколько сотен младенцев ежегодно умирают в результате осложнений, возникающих в тяжелых случаях заболевания, но ранняя диагностика и лечение значительно снижают эти риски. В развивающихся странах, где ранняя диагностика и лечение недоступны, показатели материнской смертности от преэклампсии намного выше.
Другие редкие проблемы, которые могут возникнуть в результате этого состояния, включают инсульт, плацентарное кровотечение (которое может привести к появлению маленьких детей и риску прекращения кровоснабжения ребенка во время родов), осложнения с легкими, печенью или почками и проблемы с кровью. и функция клеток печени (известная как синдром HELLP).
и функция клеток печени (известная как синдром HELLP).
Что вызывает преэклампсию?
Причина преэклампсии неизвестна, но исследования подтверждают ряд возможных теорий.
- У матери иммунный ответ на плаценту в утробе матери.Иммунная система матери обнаруживает «чужеродную» плаценту, которая на 50% состоит из генов отца, и вызывает воспалительную реакцию, в которой участвует ряд гормонов и химических веществ.
- Кровеносные сосуды в утробе матери (по которым кровь поступает к плаценте) могут недостаточно расшириться, чтобы позволить необходимому кислороду и питательным веществам достичь развивающегося ребенка. Это может быть вызвано изменениями нормального уровня гормонов, которые необходимы для контроля расслабления и сокращения кровеносных сосудов, таких как ангиотензин, адреномедуллин, тромбоксин, эндотелин-1 и простациклин, или сосуды, которые физически не могут расширяться в ответ на беременность.
Исследования показали, что уровни факторов роста, которые обычно способствуют формированию и поддержанию здоровых кровеносных сосудов, включая фактор роста плаценты и фактор роста эндотелия сосудов, снижаются у женщин, у которых развивается преэклампсия.
 Также может быть связь с плохим развитием кровеносных сосудов внутри самой плаценты, что может препятствовать оптимальной передаче питательных веществ от матери к ребенку. Также может быть связь с низким уровнем белка в рационе матери, ведущим к изменениям уровня ангиотензина, что может привести к снижению переноса питательных веществ и преэклампсии.
Также может быть связь с плохим развитием кровеносных сосудов внутри самой плаценты, что может препятствовать оптимальной передаче питательных веществ от матери к ребенку. Также может быть связь с низким уровнем белка в рационе матери, ведущим к изменениям уровня ангиотензина, что может привести к снижению переноса питательных веществ и преэклампсии. - Другая школа мысли заключается в том, что ранее существовавшие аутоиммунные состояния могут обострять или запускать изменения в матке, которые приводят к развитию преэклампсии. Известно, что женщины с определенными заболеваниями (например, диабет, высокое кровяное давление, почечные проблемы, антифосфолипидный синдром) подвергаются повышенному риску развития преэклампсии.
Вероятно, что существует несколько причин преэклампсии, которые у разных людей различаются, но приводят к схожему набору симптомов, характеризующих это состояние.Исследования по изучению всех этих возможностей продолжаются.
Каковы признаки и симптомы преэклампсии?
Симптомы преэклампсии могут возникать после 20 недель беременности, но чаще всего возникают в период с 32 недель до 1 недели после родов. При легкой преэклампсии симптомы могут быть незначительными или отсутствовать, поэтому важно провести скрининг на беременность, чтобы выявить заболевание на ранней стадии. Женщины, которые думают, что у них наблюдаются симптомы преэклампсии, должны немедленно обратиться к врачу для дальнейшего обследования.
При легкой преэклампсии симптомы могут быть незначительными или отсутствовать, поэтому важно провести скрининг на беременность, чтобы выявить заболевание на ранней стадии. Женщины, которые думают, что у них наблюдаются симптомы преэклампсии, должны немедленно обратиться к врачу для дальнейшего обследования.
Больные женщины страдают от очень высокого кровяного давления, а также от утечки белка из почек в мочу. Люди могут испытывать сильные головные боли, нечеткое зрение, боль в животе (обычно в верхней правой части живота), рвоту на поздних сроках беременности и внезапный отек рук и ног (из-за задержки жидкости). Считается, что женщины, у которых впервые во время беременности наблюдается высокое кровяное давление, без белка в моче, страдают от «гестационного высокого кровяного давления», а не от преэклампсии.
Изменения уровней различных гормонов были также описаны при преэклампсии, включая хорионический гонадотропин человека (ХГЧ) и кортикотропин-высвобождающий гормон (CRH), которые вырабатываются плацентой и, как видно, повышаются при преэклампсии. Также может быть повышен уровень тиреотропного гормона (ТТГ), что может быть связано с повышенным риском развития гипотиреоза у матери.
Также может быть повышен уровень тиреотропного гормона (ТТГ), что может быть связано с повышенным риском развития гипотиреоза у матери.
Признаки дистресса плода могут возникать в результате преэклампсии, например, когда ребенок мал для гестационного возраста, малый объем околоплодных вод окружает ребенка, а ребенок испытывает дистресс до или во время родов.
Насколько распространена преэклампсия?
Преэклампсия поражает около 5% всех беременностей во всем мире. Считается, что женщины подвергаются большему риску развития преэклампсии, если:
Передается ли преэклампсия по наследству?
Хотя заболевание не считается переданным по наследству, женщины подвергаются более высокому риску, если их близкие родственники, такие как их мать или сестра, также были затронуты. Исследования не выявили генетической связи с этим заболеванием, но некоторые исследования показали, что отец также может способствовать риску преэклампсии.Это связано с тем, что мужчины, рожденные в результате преэкламптической беременности, с большей вероятностью родят ребенка во время беременности, которая также осложняется преэклампсией. Некоторые мужчины также несут более высокий риск преэкламптической беременности, чем другие.
Некоторые мужчины также несут более высокий риск преэкламптической беременности, чем другие.
Как диагностируется преэклампсия?
Артериальное давление измеряется на обычных приемах у акушерки на протяжении всей беременности. Преэклампсия диагностируется, если у женщины повышенное артериальное давление (140/90 и выше), а также белок в моче после 20-й недели беременности.Чтобы подтвердить это, артериальное давление следует измерять как минимум в двух разных случаях с интервалом не менее 4–6 часов; белок в моче обычно проверяется с помощью одного теста с полосками или путем сбора мочи в течение 24 часов.
В настоящее время перед медицинским сообществом стоит задача улучшить методы выявления лиц с повышенным риском развития преэклампсии на ранних сроках беременности, а затем потенциально обеспечить профилактическое лечение. В настоящее время врачи полагаются на измерения кровотока в артериях матки с помощью ультразвуковой допплерографии; это один из методов прогнозирования состояния, поскольку у женщин с плохим кровотоком вероятность развития преэклампсии более чем в шесть раз выше. Однако метод, использованный для этого измерения, оказался неточным при прогнозировании этого расстройства, и он не считается полезным для рутинного скрининга всех беременных женщин, а только тех, которые уже относятся к группе высокого риска. Альтернативный подход — это анализ определенных маркеров в крови и моче (таких как урокортин, анандамид и ангиотензин II) на ранних сроках беременности, который может предсказать, у каких женщин с наибольшей вероятностью разовьется это заболевание в дальнейшем. В этой области необходимы дальнейшие исследования, прежде чем такие тесты будут регулярно использоваться для прогнозирования преэклампсии.
Однако метод, использованный для этого измерения, оказался неточным при прогнозировании этого расстройства, и он не считается полезным для рутинного скрининга всех беременных женщин, а только тех, которые уже относятся к группе высокого риска. Альтернативный подход — это анализ определенных маркеров в крови и моче (таких как урокортин, анандамид и ангиотензин II) на ранних сроках беременности, который может предсказать, у каких женщин с наибольшей вероятностью разовьется это заболевание в дальнейшем. В этой области необходимы дальнейшие исследования, прежде чем такие тесты будут регулярно использоваться для прогнозирования преэклампсии.
Как лечится преэклампсия?
Лечение преэклампсии направлено на предотвращение развития полной эклампсии и других перечисленных выше осложнений. В настоящее время единственное полное излечение от преэклампсии — это роды и плацента (считается, что это связано с причиной заболевания). Это происходит либо путем стимуляции родов, либо путем кесарева сечения. После родов у матери обычно нормализуется артериальное давление. Этот метод подходит, когда преэклампсия возникает на поздних сроках беременности, но если это состояние возникает на более ранних сроках беременности, у преждевременно родившегося ребенка могут возникнуть дополнительные проблемы.В таких случаях следует учитывать несколько факторов, в том числе тяжесть состояния и то, как оно влияет на ребенка, и какое влияние окажут ранние роды.
После родов у матери обычно нормализуется артериальное давление. Этот метод подходит, когда преэклампсия возникает на поздних сроках беременности, но если это состояние возникает на более ранних сроках беременности, у преждевременно родившегося ребенка могут возникнуть дополнительные проблемы.В таких случаях следует учитывать несколько факторов, в том числе тяжесть состояния и то, как оно влияет на ребенка, и какое влияние окажут ранние роды.
Другие виды лечения, которые могут быть назначены до рождения ребенка, включают:
- Лекарство для снижения артериального давления у матери
- стероидов для созревания легких ребенка в случае преждевременных родов
- , который, как считается, снижает вероятность развития экламптических припадков у матери.
Подходы к предотвращению развития этого состояния у женщин, относящихся к группе высокого риска, в настоящее время очень ограничены, и исследования показали очень неоднозначные результаты. Текущие исследования продолжают определять, могут ли такие факторы, как упражнения, контроль веса и использование антиоксидантов, помочь снизить риск. Очень важно следить за артериальным давлением и ростом плода во время беременности.
Текущие исследования продолжают определять, могут ли такие факторы, как упражнения, контроль веса и использование антиоксидантов, помочь снизить риск. Очень важно следить за артериальным давлением и ростом плода во время беременности.
Есть ли у лечения побочные эффекты?
Ранние роды в дальнейшем при беременности (с 34 недель) редко вызывают дальнейшие осложнения; однако, если ребенку меньше 32 недель, его или ее легкие могут еще не быть достаточно зрелыми, и они могут испытывать долгосрочные осложнения для здоровья, связанные с преждевременным рождением.Недоношенным детям (рожденным до 37-й недели беременности) может потребоваться пребывание в отделении интенсивной терапии новорожденных, целью которого является воспроизведение условий в утробе матери, пока ребенок полностью развивается.
Каковы более долгосрочные последствия преэклампсии?
В большинстве случаев преэклампсия лечится эффективно, и это не сказывается на здоровье матери и ребенка в долгосрочной перспективе. Постоянный мониторинг артериального давления и образцов мочи на послеродовых приемах очень важен для обеспечения их возвращения к нормальному уровню.Преэклампсия может быть связана с более высоким риском развития сердечно-сосудистых заболеваний у пострадавших женщин, таких как ишемическая болезнь сердца или инсульт, в более позднем возрасте. Однако риск развития этих состояний можно снизить за счет различных изменений образа жизни, включая регулярные упражнения, поддержание здорового веса, сбалансированное питание и отказ от курения.
Постоянный мониторинг артериального давления и образцов мочи на послеродовых приемах очень важен для обеспечения их возвращения к нормальному уровню.Преэклампсия может быть связана с более высоким риском развития сердечно-сосудистых заболеваний у пострадавших женщин, таких как ишемическая болезнь сердца или инсульт, в более позднем возрасте. Однако риск развития этих состояний можно снизить за счет различных изменений образа жизни, включая регулярные упражнения, поддержание здорового веса, сбалансированное питание и отказ от курения.
В некоторых случаях преэклампсии наблюдается недостаточный приток крови к плаценте, что означает, что ребенок не получает всех питательных веществ, необходимых для полноценного развития.Это может привести к тому, что ребенок не станет таким большим, как должен, — состояние, известное как ограничение роста плода. Это может привести к различным проблемам после рождения ребенка и в более зрелом возрасте, поскольку повышает вероятность развития сердечно-сосудистых заболеваний и диабета.
Последнее обновление: март 2018
Симптом преэклампсии «гестоз», его опасности и тактика лечения
Преэклампсия — серьезное функциональное нарушение жизненно важных органов и систем будущей матери, тяжелая форма гестоза, за которой следует повышение артериального давления, присутствие белка в моче, отек, нарушение работы центральной нервной системы и некоторых других жизненно важных органов. .Понятие «преэклампсия» появилось в медицинской практике в 1996 году; Ранее все болезненные симптомы и довольно опасные состояния во второй половине беременности определялись термином «поздний токсикоз». В отличие от раннего токсикоза, который в большинстве случаев не представляет опасности, преэклампсия является довольно серьезным осложнением беременности и может привести к смерти как женщины, так и плода.
Преэклампсия — серьезное функциональное нарушение жизненно важных органов и систем будущей матери, часто основанное на уже существующих заболеваниях, таких как гипертония, заболевания почек, печени и желчевыводящих путей, эндокринные заболевания. Все причины преэклампсии остаются неизвестными, так как есть исключения, когда поздняя преэклампсия возникает у женщин, которые до наступления беременности не имели хронических заболеваний и серьезных проблем со здоровьем.
Все причины преэклампсии остаются неизвестными, так как есть исключения, когда поздняя преэклампсия возникает у женщин, которые до наступления беременности не имели хронических заболеваний и серьезных проблем со здоровьем.
Преэклампсия может проявляться по-разному: в виде очень серьезных состояний, которые невозможно пропустить, и в виде симптомов, которые поначалу не кажутся опасными, однако могут быть признаками действительно серьезных проблем.
Не пропустите следующие симптомы преэклампсии:
1.Припухлость. Эта проблема может быть связана или не быть связана с преэклампсией. Довольно часто незначительные отеки нижних конечностей являются нормальным явлением и не представляют опасности для будущей мамы. Все же желательно обсудить этот вопрос с врачом, наблюдающим беременность. Ни в коем случае не стоит заниматься самолечением. Это может затруднить постановку проблемы, затруднить диагностику на ранней стадии и привести к плачевным последствиям.
2. Повышенное артериальное давление и протеинурия (наличие белка в моче) — эти симптомы должны насторожить врача, так как требуют тщательного обследования, наблюдения и, при необходимости, неотложной помощи.
3. Судороги скелетных мышц. Во время судорог резко повышается артериальное давление, что подвергает беременную женщину риску сердечного приступа. В группе риска может оказаться и ребенок из-за возможности преждевременной отслойки плаценты.
4. Преэклампсия бывает легкой, средней и тяжелой формы. В тяжелых случаях признаки нарушения центральной нервной системы сочетаются с перечисленными выше симптомами: сильными головными болями, тошнотой, рвотой, болью в эпигастрии, нечеткостью зрения, болезненными психологическими реакциями.
Своевременная диагностика и своевременное лечение, которое врач назначает строго индивидуально, на основании лабораторных исследований и инструментальных исследований, позволяют держать это состояние под контролем. Поэтому очень важно регулярно посещать врача и проходить все обследования по его рекомендациям.
Если врач подозревает преэклампсию, легкая форма требует домашнего лечения, тогда как более тяжелая форма требует пребывания в больнице. В условиях стационара врачи сделают все возможное, чтобы восстановить работу жизненно важных органов и исключить риски как для матери, так и для ребенка.
В условиях стационара врачи сделают все возможное, чтобы восстановить работу жизненно важных органов и исключить риски как для матери, так и для ребенка.
Иногда, в самых тяжелых случаях, когда лечение оказывается неэффективным и состояние пациента ухудшается, врачи рекомендуют досрочные роды. Однако врачи прибегают к этой крайней мере лишь в тех случаях, когда все альтернативные возможности лечения исчерпаны.
Способ диагностики позднего гестоза
(57) Резюме:
Метод может быть использован в медицине, в частности, для диагностики поздних гестозов беременных.Определите количество слоносперматозоидоглобулина в слюне беременных и его содержание равное или более 128 мкг / мл, чтобы диагностировать поздний гестоз беременных. Предлагаемый метод прост и позволяет с высокой точностью (96,1%) диагностировать поздний гестоз на 28 неделе беременности. Таблица 1. Изобретение относится к медицине, а именно к акушерству и гинекологии, и может быть использовано для ранней диагностики гестоза беременных. Поздняя преэклампсия является наиболее частым и тяжелым осложнением беременности и является одной из основных причин перинатальной и материнской смертности, в т.ч. некоторые случаи сменяются акушерскими кровотечениями.В нашей стране частота гестозов колеблется от 3,5 до 12%. Согласно официальной статистике, частота гестозов в 1995 г. увеличилась до 15,7%. Заболевание, даже в легкой форме, часто лежит в основе тяжелых осложнений, которые возникают у матери и плода у новорожденных и детей в первые годы жизни, и остается одним из самых серьезных лекарств, поздний гестоз невозможно вылечить, а при интенсивном лечении можно только предотвратить преэклампсию в более тяжелой форме. В настоящее время реальная профилактика гестоза основана на диагностике субклинических нарушений и их профилактической коррекции, что предотвращает развитие тяжелых форм заболевания, определяет снижение материнской и перинатальной заболеваемости и смертности.Известен способ диагностики доклинической стадии позднего гестоза беременных путем электрофоретического фракционирования белков крови в полиакриламидном геле в щелочной среде.
Поздняя преэклампсия является наиболее частым и тяжелым осложнением беременности и является одной из основных причин перинатальной и материнской смертности, в т.ч. некоторые случаи сменяются акушерскими кровотечениями.В нашей стране частота гестозов колеблется от 3,5 до 12%. Согласно официальной статистике, частота гестозов в 1995 г. увеличилась до 15,7%. Заболевание, даже в легкой форме, часто лежит в основе тяжелых осложнений, которые возникают у матери и плода у новорожденных и детей в первые годы жизни, и остается одним из самых серьезных лекарств, поздний гестоз невозможно вылечить, а при интенсивном лечении можно только предотвратить преэклампсию в более тяжелой форме. В настоящее время реальная профилактика гестоза основана на диагностике субклинических нарушений и их профилактической коррекции, что предотвращает развитие тяжелых форм заболевания, определяет снижение материнской и перинатальной заболеваемости и смертности.Известен способ диагностики доклинической стадии позднего гестоза беременных путем электрофоретического фракционирования белков крови в полиакриламидном геле в щелочной среде. Фракционированию подвергают активированную эуглобулиновую фракцию плазмы крови и при наличии полос белка с коэффициентом электрофоретической подвижности 0,41 — между 0,46 и 0,61-0,67 и диагностируют поздний гестоз беременных. Точность метода по данным литературы не известна. Метод имеет недостатки:
Фракционированию подвергают активированную эуглобулиновую фракцию плазмы крови и при наличии полос белка с коэффициентом электрофоретической подвижности 0,41 — между 0,46 и 0,61-0,67 и диагностируют поздний гестоз беременных. Точность метода по данным литературы не известна. Метод имеет недостатки: Метод трудоемок, сложен в техническом исполнении (метод 2 прибора: для электрофореза в полиакриламидном геле и результатов микроденситометра), выполнение метода занимает несколько дней.- Метод оценки варьируется в зависимости от условий метода (это плотность геля, CaII фракция эуглобулина). — Метод основан, по сути, на определении фракции эуглобулина плазмы крови, которая содержит 25% фибринового, плазминогена, плазмина, плазминогена. активаторы, протромбин и другие факторы свертывания крови, которые, как отдельные параметры, имеют широкую границу колебаний и могут изменяться при других заболеваниях (ДВС-синдром, заболевание печени, тромбоз, геморрагический васкулит). — Инвазивный способ проведения необходимого исследования венозной крови и что возможность заражения ВИЧ.
 Наиболее близким техническим решением является метод ранней диагностики доклинической стадии позднего гестоза для определения уровня кортизола и количества сенсибилизированных к антигенам лимфоцитов плаценты, а также их коэффициента корреляции ниже 50 с диагностированным поздним гестозом. Точность метода по данным литературы не известна. Недостатками способа-прототипа являются:
Наиболее близким техническим решением является метод ранней диагностики доклинической стадии позднего гестоза для определения уровня кортизола и количества сенсибилизированных к антигенам лимфоцитов плаценты, а также их коэффициента корреляции ниже 50 с диагностированным поздним гестозом. Точность метода по данным литературы не известна. Недостатками способа-прототипа являются: — Вариабельность уровня кортизола в зависимости от срока беременности. — Не стандартизирован антигенный состав плаценты, это комплекс антигенов и поэтому невозможно определить, что привело к сенсибилизации.- Инв. Целью изобретения является ранняя диагностика доклинических проявлений поздней преэклампсии у беременных для определения содержания слоно-сперматозоидного глобулина (ГСПГ) в слюне беременных. Эта цель достигается исследованиями в В слюне женщин с гестационным сроком 28 недель уровень слизисто-сперматозоидного глобулина (ГСПГ) и при его содержании равен или более 128 мкг / мл диагностирован поздний гестоз в 96,1% случаев.
 Новизна изобретения заключается в том, что Дело в том, что этот параметр используется впервые для диагностики позднего гестоза беременности.Ранее исследования слюны на ГСПГ у беременных с диагнозом поздний гестоз не проводились. В 1982 г. при изучении антигенного состава семенной плазмы Шевченко О.П. и соавт. впервые идентифицирован термостабильный белок с подвижностью альфа-1-глобулина и молекулярной массой 600007000 D. Новый белок при нагревании в течение 1 часа при 100- o C не меняет иммунологических и физико-химических свойств, поэтому называется термостабильным альфа- 1-гликопротеин (ТАГ), позже названный RESS.ГСПГ при иммунодиффузионном анализе определяли у женщин только в слюне и ткани околоушной железы, а у мужчин еще в ткани семенников и сперматозоидов. По-видимому, белок секретируется этими железами и секретируется со слюной и спермой. В исследованиях Л.С. Посисеевой был повышен уровень ГСПГ с fre «ptx2»> Метод заключается в следующем: исследование ГСПГ методом двойной иммунодиффузии в агаре со стандартной тест-системой против ГСПГ.
Новизна изобретения заключается в том, что Дело в том, что этот параметр используется впервые для диагностики позднего гестоза беременности.Ранее исследования слюны на ГСПГ у беременных с диагнозом поздний гестоз не проводились. В 1982 г. при изучении антигенного состава семенной плазмы Шевченко О.П. и соавт. впервые идентифицирован термостабильный белок с подвижностью альфа-1-глобулина и молекулярной массой 600007000 D. Новый белок при нагревании в течение 1 часа при 100- o C не меняет иммунологических и физико-химических свойств, поэтому называется термостабильным альфа- 1-гликопротеин (ТАГ), позже названный RESS.ГСПГ при иммунодиффузионном анализе определяли у женщин только в слюне и ткани околоушной железы, а у мужчин еще в ткани семенников и сперматозоидов. По-видимому, белок секретируется этими железами и секретируется со слюной и спермой. В исследованиях Л.С. Посисеевой был повышен уровень ГСПГ с fre «ptx2»> Метод заключается в следующем: исследование ГСПГ методом двойной иммунодиффузии в агаре со стандартной тест-системой против ГСПГ. Метод полуколичественный. Перед производством анализа готовится серия разведений анализируемой слюны в дистиллированной воде в лунках с полиэтиленовой матрицей соответственно 1: 1, 1: 2, 1: 4, 1: 8, 1:16, 1:32, 1:64. .Реакцию проводят на нежирных предметных стеклах, залитых расплавленным 1% -ным раствором агара типа «Дифко» с 25% -ным раствором хлорида натрия из расчета 5 мл геля на один анализ. Отвердевание агара в нем пробивают специальными стандартными штампами «семерки». Тонкой иглой удаляют агар из лунок. В центральную лунку каждой из «семерок» с помощью пипетки Пастера залить антисигарету против ГСПГ, в две противоположные — раствор стандартного антигена, а в оставшиеся 4 — исследованную слюну в разных разведениях.Стекла помещают в чашки Петри с влажной средой. Продолжительность иммунопрофилирования 18-24 часа. Результаты считываются на следующий день в проходящем свете. Учтена последняя линия выпадения осадка АЦК возле лунок с соответствующим разведением исследуемой слюны. Итак, получаем полуколичественную оценку результата.
Метод полуколичественный. Перед производством анализа готовится серия разведений анализируемой слюны в дистиллированной воде в лунках с полиэтиленовой матрицей соответственно 1: 1, 1: 2, 1: 4, 1: 8, 1:16, 1:32, 1:64. .Реакцию проводят на нежирных предметных стеклах, залитых расплавленным 1% -ным раствором агара типа «Дифко» с 25% -ным раствором хлорида натрия из расчета 5 мл геля на один анализ. Отвердевание агара в нем пробивают специальными стандартными штампами «семерки». Тонкой иглой удаляют агар из лунок. В центральную лунку каждой из «семерок» с помощью пипетки Пастера залить антисигарету против ГСПГ, в две противоположные — раствор стандартного антигена, а в оставшиеся 4 — исследованную слюну в разных разведениях.Стекла помещают в чашки Петри с влажной средой. Продолжительность иммунопрофилирования 18-24 часа. Результаты считываются на следующий день в проходящем свете. Учтена последняя линия выпадения осадка АЦК возле лунок с соответствующим разведением исследуемой слюны. Итак, получаем полуколичественную оценку результата. Это разбавление слюны SG от женщин с нормальной беременностью. При настройке ответа на УКГ-на-одном анализе используется одно предметное стекло с агаром. Существенными отличиями заявленного способа являются:
Это разбавление слюны SG от женщин с нормальной беременностью. При настройке ответа на УКГ-на-одном анализе используется одно предметное стекло с агаром. Существенными отличиями заявленного способа являются: — во-первых, нами предложен новый диагностический параметр слюны женщины ГСПГ равный или более 128 мкг / мл. для диагностики позднего гестоза;
— во-вторых, вы используете другую биологическую среду — слюну женщины.Преимущества предлагаемого способа:
1. Исследование слюны происходит с 28 недель беременности, что позволяет рано принять решение о возможности позднего гестоза беременной и своевременно провести комплекс лечебных мероприятий.2. Высокая точность метода — 96,1%
3. Абсолютная безопасность и доступность метода связана с исследованием ГСПГ в слюне женщины, так как нет необходимости в заборе крови у беременной женщины и других травмах. 4. Простота и удобство использования тест-систем для ГСПГ позволяют широко использовать его в медицинской практике.Тест-системы для SHBG производятся несколькими диагностическими компаниями, уполномоченными на внедрение.
 В настоящее время тест-систему на SHBG можно приобрести по адресу: 117896. AMI:
В настоящее время тест-систему на SHBG можно приобрести по адресу: 117896. AMI: Пример 1. Беременная А. 17 лет, срок беременности 30 недель. Эта первая беременность протекала без осложнений. Через 30 недель объективно: жалоб нет. Артериальное давление 110/70 мм рт.ст .; прибавка в весе за неделю 300 г (обычно не более 200). WSDM — 30 см, RC — 82 см. Сердцебиение плода четкое, ритмичное до 142 в минуту, отеков не видно.Общий анализ мочи без патологии. Заключение по УЗИ: размер плода соответствует 30 неделе беременности, матка в норме, количество околоплодных вод в норме. Поставлен клинический диагноз: Беременность 30 недель, риск возникновения позднего гестоза. В обследовании указано: SSG обнаружен в слюне в концентрации 1:32, что составляет 128 мкг / мл, эти данные позволили диагностировать поздний гестоз. При изучении динамики на 3 неделе беременности А. возникновение пастозности большеберцовой кости и передней брюшной стенки, аномального набора веса за неделю 350. Беременная, положена в клинику с диагнозом: Беременность 33 недели.
 Поздний гестоз (водянка 1 степени). Перфорада в 18 лет. Беременность закончилась своевременными родами и рождением доношенного новорожденного массой 3200 г, ростом 60 см, III степень. Беременная К. 28 лет, срок гестации 28 недель. Это вторая беременность. Первая беременность закончилась индуцированными преждевременными родами в сроке 33 недели по поводу тяжелой поздней преэклампсии (нефропатия II-III степени) и рождения недоношенного ребенка массой 1900 г., ростом 45 см по шкале Апгар 4-5. балеты. Ребенок умер через 3 дня.При отнесении беременной к группе риска по развитию позднего гестоза. Эта беременность протекает без осложнений. Через 28 недель объективно: жалоб нет, АД — 120/80 мм рт. Изобразительное искусство. отеков нет, белка в моче нет, прибавка в весе за неделю — 200 г. По данным США: беременность 28 нед, плод соответствует сроку беременности. Диагноз: беременность 35 недель, риск позднего гестоза. При обследовании заявленным способом ГСПГ в слюне был обнаружен в концентрации 1: 4, что составляет 16 мкг / мл и у этой беременной нет признаков позднего гестоза.
Поздний гестоз (водянка 1 степени). Перфорада в 18 лет. Беременность закончилась своевременными родами и рождением доношенного новорожденного массой 3200 г, ростом 60 см, III степень. Беременная К. 28 лет, срок гестации 28 недель. Это вторая беременность. Первая беременность закончилась индуцированными преждевременными родами в сроке 33 недели по поводу тяжелой поздней преэклампсии (нефропатия II-III степени) и рождения недоношенного ребенка массой 1900 г., ростом 45 см по шкале Апгар 4-5. балеты. Ребенок умер через 3 дня.При отнесении беременной к группе риска по развитию позднего гестоза. Эта беременность протекает без осложнений. Через 28 недель объективно: жалоб нет, АД — 120/80 мм рт. Изобразительное искусство. отеков нет, белка в моче нет, прибавка в весе за неделю — 200 г. По данным США: беременность 28 нед, плод соответствует сроку беременности. Диагноз: беременность 35 недель, риск позднего гестоза. При обследовании заявленным способом ГСПГ в слюне был обнаружен в концентрации 1: 4, что составляет 16 мкг / мл и у этой беременной нет признаков позднего гестоза.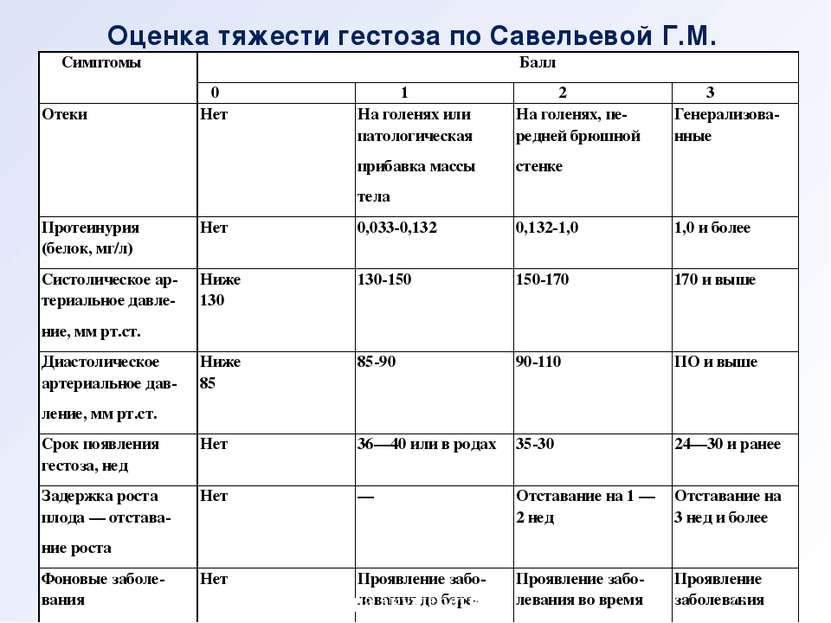 При последующем наблюдении за беременной признаков позднего гестоза не выявлено. Беременность закончилась своевременными родами и рождением доношенного ребенка массой 3500 г и ростом 60 см, по оценке по шкале Апгар 8-9 б беременность 28 недель. Это пятая беременность, желательная во втором браке. Первая беременность закончилась своевременными родами на 39 неделе и рождением ребенка массой 3700 грамм и ростом 62 см, оценка по шкале Апгар 7-8 баллов. Следующие 3 беременности закончились медикаментозным абортом без осложнений.Эта беременность протекает без осложнений. Заключение терапевта: артериальная гипертензия I А стадии. Объективно через 28 недель: состояние удовлетворительное, жалоб нет, АД 140/90 мм рт.ст., видимых отеков нет, общий анализ мочи без отклонений, прибавка в весе за неделю 250, По данным УЗИ: беременность 28 недель, плод соответствует срок беременности. Диагноз: беременность 28 недель. Гипертоническая болезнь 1 А стадии. Риск развития позднего гестоза. При обследовании заявленного способа ГСПГ в слюне женщин обнаружена концентрация 1:64, что составляет 256 мкг / мл, что позволяет диагностировать предтексты этой женщины.
При последующем наблюдении за беременной признаков позднего гестоза не выявлено. Беременность закончилась своевременными родами и рождением доношенного ребенка массой 3500 г и ростом 60 см, по оценке по шкале Апгар 8-9 б беременность 28 недель. Это пятая беременность, желательная во втором браке. Первая беременность закончилась своевременными родами на 39 неделе и рождением ребенка массой 3700 грамм и ростом 62 см, оценка по шкале Апгар 7-8 баллов. Следующие 3 беременности закончились медикаментозным абортом без осложнений.Эта беременность протекает без осложнений. Заключение терапевта: артериальная гипертензия I А стадии. Объективно через 28 недель: состояние удовлетворительное, жалоб нет, АД 140/90 мм рт.ст., видимых отеков нет, общий анализ мочи без отклонений, прибавка в весе за неделю 250, По данным УЗИ: беременность 28 недель, плод соответствует срок беременности. Диагноз: беременность 28 недель. Гипертоническая болезнь 1 А стадии. Риск развития позднего гестоза. При обследовании заявленного способа ГСПГ в слюне женщин обнаружена концентрация 1:64, что составляет 256 мкг / мл, что позволяет диагностировать предтексты этой женщины. При обследовании в сроке 30 недель выявлены симптомы нефропатии первой степени, женщина помещена в стационар. Проведено лечение. Беременность закончилась своевременными родами и при рождении масса тела 3000 г, рост 54 см, оценка по шкале А сведена в таблицу. Таким образом, заявленный способ прост в исполнении и позволяет с высокой точностью диагностировать предтексты, начиная с недели беременности. беременность, что позволит вам выбрать правильную тактику ведения женщин с риском позднего гестоза и поможет снизить частоту этого осложнения беременности, снизить экономические затраты на лечение.Способ диагностики позднего гестоза беременных путем исследования биологической жидкости, отличающийся тем, что в слюне для определения количества слоно-сперматозоидного глобулина и его содержания равного или более 128 мкг / мл, подлежащего диагностике с поздним гестоз беременных.
При обследовании в сроке 30 недель выявлены симптомы нефропатии первой степени, женщина помещена в стационар. Проведено лечение. Беременность закончилась своевременными родами и при рождении масса тела 3000 г, рост 54 см, оценка по шкале А сведена в таблицу. Таким образом, заявленный способ прост в исполнении и позволяет с высокой точностью диагностировать предтексты, начиная с недели беременности. беременность, что позволит вам выбрать правильную тактику ведения женщин с риском позднего гестоза и поможет снизить частоту этого осложнения беременности, снизить экономические затраты на лечение.Способ диагностики позднего гестоза беременных путем исследования биологической жидкости, отличающийся тем, что в слюне для определения количества слоно-сперматозоидного глобулина и его содержания равного или более 128 мкг / мл, подлежащего диагностике с поздним гестоз беременных.Клинические проявления преэклампсии и диагностическая ценность белков и продуктов их метилирования как биомаркеров у беременных с преэклампсией и их новорожденных
Преэклампсия (ПЭ) — это заболевание, которым страдают 1-10% беременных женщин во всем мире. Он характеризуется гипертонией и протеинурией на поздних сроках беременности и может привести к материнской и перинатальной заболеваемости и смертности. Помимо доставки плода и удаления плаценты, на сегодняшний день не существует терапевтических подходов для лечения или профилактики ПЭ. Таким образом, снизить смертность от ПЭ можно только путем раннего выявления, тщательного мониторинга и лечения симптомов. По этим причинам поиск неинвазивных биохимических маркеров, передающихся через кровь или мочу, которые можно было бы использовать для скрининга, пресимптоматической диагностики и прогнозирования развития ПЭ, является очень актуальным.До сих пор для прогнозирования ПЭ был предложен ряд биомаркеров на основе патофизиологических наблюдений, но в большинстве случаев они оказались ненадежными и несовместимыми между различными исследованиями. Клиническая картина ПЭ и данные, собранные для биохимических маркеров фактора роста плаценты (PlGF), растворимой кошачьей саркомы МакДоноу (fms-), подобной тирозинкиназе-1 (sFlt-1), асимметричного диметиларгинина (ADMA) и метил-лизина, являются пересматривается с целью предоставления как клинического, так и биохимического понимания того, как эти биомаркеры могут помочь в диагностике ПЭ или указать на ее тяжесть.
Он характеризуется гипертонией и протеинурией на поздних сроках беременности и может привести к материнской и перинатальной заболеваемости и смертности. Помимо доставки плода и удаления плаценты, на сегодняшний день не существует терапевтических подходов для лечения или профилактики ПЭ. Таким образом, снизить смертность от ПЭ можно только путем раннего выявления, тщательного мониторинга и лечения симптомов. По этим причинам поиск неинвазивных биохимических маркеров, передающихся через кровь или мочу, которые можно было бы использовать для скрининга, пресимптоматической диагностики и прогнозирования развития ПЭ, является очень актуальным.До сих пор для прогнозирования ПЭ был предложен ряд биомаркеров на основе патофизиологических наблюдений, но в большинстве случаев они оказались ненадежными и несовместимыми между различными исследованиями. Клиническая картина ПЭ и данные, собранные для биохимических маркеров фактора роста плаценты (PlGF), растворимой кошачьей саркомы МакДоноу (fms-), подобной тирозинкиназе-1 (sFlt-1), асимметричного диметиларгинина (ADMA) и метил-лизина, являются пересматривается с целью предоставления как клинического, так и биохимического понимания того, как эти биомаркеры могут помочь в диагностике ПЭ или указать на ее тяжесть.
1. Введение
Преэклампсия (ПЭ) — это мультисистемное специфическое для беременности заболевание, которое характеризуется развитием гипертонии и протеинурии (повышенного уровня белка в моче) после 20 недель беременности [1]. ПЭ является ведущей причиной материнской, перинатальной (с 20-й недели беременности до 4-й недели после рождения), а также фетальной / неонатальной смертности и заболеваемости во всем мире [2, 3].
PE — очень серьезное заболевание, которое осложняет от 2% до 5% беременностей в Европе и Америке и может достигать до 10% беременностей в развивающихся странах, в основном из-за отсутствия или недостаточности неотложной помощи [2].Кроме того, ПЭ связана с повышенным риском отслойки плаценты, преждевременных родов, задержки внутриутробного развития плода (ЗВУР), острой почечной недостаточности, цереброваскулярных и сердечно-сосудистых осложнений, диссеминированного внутрисосудистого свертывания крови и смерти матери [4]. Таким образом, возможность ранней диагностики ПЭ имеет жизненно важное значение.
2. Клиническая картина, диагностика и патофизиология ПЭ
Клинически ПЭ проявляется как впервые возникшая гипертензия у ранее нормотензивной женщины с показаниями систолического и диастолического артериального давления ≥140 и ≥90 мм рт.ст., соответственно, на 2 отдельных случаи с интервалом не менее 6 часов, а также протеинурия, развивающаяся после 20 недель беременности [5–7].
Это заболевание может иметь раннее начало (ПЭ начинается до 34 недель беременности) или поздно (после 34 недель беременности) и может быть классифицировано как легкое или тяжелое, в зависимости от тяжести имеющихся симптомов [2] (таблица 1). В случае тяжелой ТЭЛА отмечается более значительное повышение артериального давления и большая степень протеинурии. Другие симптомы тяжелой ТЭЛА, которые могут присутствовать, включают олигурию (менее 500 мл мочи за 24 часа), церебральные или зрительные нарушения, а также отек легких или цианоз [8, 9].
| |||||||||||||||||||||||||||
Кроме того, некоторые клинические проявления ТЭЛА могут протекать быстро или незаметно. у женщин изначально могут отсутствовать симптомы даже после того, как были отмечены гипертензия и протеинурия, в то время как у других с самого начала могут проявляться симптомы тяжелой ТЭЛА [1].Наконец, это состояние может проявляться только как материнское заболевание, при котором наблюдается нормальный рост плода, или же оно может привести к задержке внутриутробного развития или внезапному дистрессу плода [2].
у женщин изначально могут отсутствовать симптомы даже после того, как были отмечены гипертензия и протеинурия, в то время как у других с самого начала могут проявляться симптомы тяжелой ТЭЛА [1].Наконец, это состояние может проявляться только как материнское заболевание, при котором наблюдается нормальный рост плода, или же оно может привести к задержке внутриутробного развития или внезапному дистрессу плода [2].
Гипертонические расстройства во время беременности являются наиболее частыми осложнениями, наблюдаемыми акушерами [10], и все они связаны с более высокими показателями материнской и внутриутробной смертности и заболеваемости [11]. В эту категорию заболеваний входят хроническая гипертензия, ПЭ, ПЭ, наложенная на хроническую гипертензию, и гипертензию беременных [9].Этиология и патология этих нарушений различаются, и, таким образом, получение диагноза ПЭ становится менее трудным, если врачи могут отличить ПЭ от других гипертензивных расстройств беременности (Рисунок 1).
При хронической артериальной гипертензии повышенное артериальное давление может наблюдаться до беременности, наблюдаться до 20 недель беременности или же наблюдаться через 12 недель после родов [9]. Это контрастирует с ПЭ, которая определяется наличием повышенного артериального давления и протеинурии после 20 недель беременности.В тяжелых случаях ПЭ может перерасти в эклампсию, которая является серьезным осложнением, которое характеризуется новым началом эпилептических припадков (генерализованных судорог) из-за спазмов сосудов головного мозга и отека мозга [13] у женщины с ПЭ [1] . Эклампсия обычно возникает во второй половине беременности и является важной причиной материнской смертности, чаще всего в результате кровоизлияния в мозг [14].
PE, наложенная на хроническую гипертензию, характеризуется вновь возникшей протеинурией (или внезапным повышением уровня белка, если протеинурия уже присутствовала), резким повышением артериального давления (при условии, что протеинурия уже существует) или развитием HELLP (гемолиз, повышенный уровень ферментов печени, низкое количество тромбоцитов) синдром [8]. Наконец, гестационную гипертензию можно отличить от ПЭ, поскольку она характеризуется наличием повышенного артериального давления после 20 недель беременности, которое нормализуется в течение 12 недель после родов, а также отсутствием протеинурии [8].
Наконец, гестационную гипертензию можно отличить от ПЭ, поскольку она характеризуется наличием повышенного артериального давления после 20 недель беременности, которое нормализуется в течение 12 недель после родов, а также отсутствием протеинурии [8].
Медицинские состояния, которые могут вызвать микрососудистые заболевания, включая сахарный диабет, хроническую гипертензию, заболевания сосудов и соединительной ткани, а также антифосфолипидный синдром и нефропатию, являются факторами риска развития ПЭ.Ряд других факторов риска развития ПЭ, которые могут быть связаны с самой беременностью или с клиническими характеристиками матери или отца плода, представлены на Рисунке 2 [8, 12, 15].
Хотя патофизиология ПЭ до конца не изучена, проблемы имплантации плаценты и уровень трофобластической инвазии, как следствие эндотелиальной дисфункции, по-видимому, играют центральную роль в развитии и прогрессировании этого заболевания.Во время нормальной беременности цитотрофобласты, происходящие от плода, вторгаются и реконструируют спиральные артерии матки матери, так что эти артерии малого диаметра с высоким сопротивлением превращаются в сосуды с высокой емкостью и низким сопротивлением [16]. Этот процесс завершается около середины беременности, чтобы оптимизировать распределение материнской крови и гарантировать, что развивающаяся маточно-плацентарная единица имеет адекватную доставку кислорода и питательных веществ из материнского кровообращения (Ramsey and Donner (1980), цитируется в [3]).
Этот процесс завершается около середины беременности, чтобы оптимизировать распределение материнской крови и гарантировать, что развивающаяся маточно-плацентарная единица имеет адекватную доставку кислорода и питательных веществ из материнского кровообращения (Ramsey and Donner (1980), цитируется в [3]).
PE будет развиваться в два этапа. Первая, бессимптомная стадия ПЭ включает нарушение трофобластической инвазии децидуальной оболочки (материнское плацентарное ложе), что, по-видимому, связано с местными аномальными взаимодействиями материнского иммунитета в стенке матки [2, 17, 18]. Эта ненормальная неглубокая плацентация снижает перфузию маточно-плацентарной крови и, как следствие, приводит к локальной гипоксии плаценты. Было показано, что этот окислительный стресс еще больше ухудшает функцию сосудов плаценты [19], что, как следствие, приводит к недостаточной перфузии крови, воспалению, апоптозу и структурным повреждениям [17, 20–23].
На второй стадии плацентарные факторы крови, высвобождаемые в материнский кровоток из плаценты с плохой перфузией, вместе с аберрантной экспрессией провоспалительных, антиангиогенных и ангиогенных факторов могут активировать материнский эндотелий и в конечном итоге вызвать эндотелиальную дисфункцию, приводит к основным клиническим симптомам ПЭ: артериальной гипертензии и протеинурии [14, 24]. Было отмечено, что величина дефектной трофобластической инвазии спиральных артерий коррелирует с тяжестью ПЭ [25].
Было отмечено, что величина дефектной трофобластической инвазии спиральных артерий коррелирует с тяжестью ПЭ [25].
Хотя ПЭ нельзя предотвратить, смертность от ПЭ можно снизить за счет раннего выявления и тщательного мониторинга ПЭ [1]. Кроме того, женщины с прогрессирующей или тяжелой ТЭЛА должны быть госпитализированы на ранней стадии, чтобы можно было тщательно контролировать состояние здоровья матери и плода.
3. Биомаркеры PE
Поиск неинвазивных биомаркеров, передающихся через кровь или мочу, которые можно было бы использовать для скрининга и диагностики этого опасного для жизни расстройства беременности, имеет первостепенное значение.Такие биомаркеры могут предсказать развитие ПЭ или помочь в ее обнаружении, что, в свою очередь, может иметь жизненно важное значение для ведения беременных женщин и их будущих детей [2].
Наиболее важно то, что скрининг беременных с использованием биохимических маркеров ПЭ может позволить провести досимптомную диагностику, что, в свою очередь, снизит ненужные страдания и расходы на здравоохранение, связанные с этим заболеванием [26]. Путем постановки более раннего диагноза можно более тщательно отслеживать прогрессирование расстройства вместе с состоянием здоровья матери и плода, что позволяет оптимизировать время для родов с целью сокращения числа преждевременных родов или других осложнений, связанных с ПЭ [ 27].Такие биохимические маркеры также могут позволить классифицировать женщин с ПЭ в соответствии с серьезностью симптомов и / или исходом беременности, что в дальнейшем улучшит их клиническое ведение [28].
Путем постановки более раннего диагноза можно более тщательно отслеживать прогрессирование расстройства вместе с состоянием здоровья матери и плода, что позволяет оптимизировать время для родов с целью сокращения числа преждевременных родов или других осложнений, связанных с ПЭ [ 27].Такие биохимические маркеры также могут позволить классифицировать женщин с ПЭ в соответствии с серьезностью симптомов и / или исходом беременности, что в дальнейшем улучшит их клиническое ведение [28].
Были исследованы многочисленные биохимические маркеры ПЭ, которые были выбраны на основе патофизиологических наблюдений, отмеченных в случаях ПЭ, таких как плацентарная и / или эндотелиальная дисфункция (Таблица 2). Однако надежность этих маркеров в прогнозировании ПЭ не соответствовала различным исследованиям [2].Следовательно, в данном обзоре основное внимание будет уделено тем биохимическим маркерам ПЭ, которые кажутся наиболее клинически значимыми, по отдельности или в комбинации, для диагностики ПЭ, а также их способности указывать на тяжесть этого заболевания, а именно плацентарный фактор роста (PlGF), растворимая кошачья саркома McDonough (fms-), подобная тирозинкиназе-1 (sFlt-1) и асимметричный диметиларгинин (ADMA), а также введение возможности скрининга метиллизина в связанных с беременностью белках .
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
3.1. Фактор роста плаценты (PlGF) и растворимая fms-подобная тирозинкиназа-1 (sFlt-1)
PlGF принадлежит к семейству белков фактора роста эндотелия сосудов (VEGF) и на 53% идентичен росту на основе тромбоцитов. факторподобная область VEGF [29]. На основании этой гомологии с VEGF было высказано предположение, что PlGF является ангиогенным фактором [29–31]. Фактически, PlGF обладает сильными ангиогенными и митогенными свойствами, которые способны индуцировать пролиферацию, миграцию и активацию эндотелиальных клеток [32, 33].
Экспрессия матричной РНК (мРНК) PlGF, по-видимому, ограничена плацентой, трофобластическими опухолями и культивируемыми эндотелиальными клетками человека [29–31]. По существу, PlGF обнаруживается в больших количествах в плаценте, но он также экспрессируется на низком уровне при нормальных физиологических условиях в некоторых других органах, включая сердце, легкие, скелетные мышцы и жировую ткань [34-40].
Проангиогенная активность членов семейства белков VEGF, включая PlGF, достигается за счет связывания и активации рецепторов тирозинкиназ [41, 42].Наиболее важными рецепторами, которые, как было установлено, связывают семейство белков VEGF с высокой аффинностью, являются fms-подобный рецептор тирозинкиназы (Flt-1, также называемый рецептором 1 VEGF, VEGFR1) и область киназного домена (KDR или VEGFR2). ) [43, 44]. Эти рецепторы состоят из одной сигнальной последовательности, трансмембранного домена, 7 иммуноглобулиноподобных доменов во внеклеточном домене (лиганд-связывающий домен) и внутриклеточного тирозинкиназного домена [45].
Однако было отмечено, что кДНК в эндотелиальных клетках пупочной вены человека в плаценте кодирует усеченную форму Flt-1, которая генерируется посредством альтернативного сплайсинга мРНК.Эта растворимая изоформа Flt-1 (sFlt-1) лишена седьмого иммуноглобулиноподобного домена, цитоплазматического домена и трансмембранной последовательности [45].
3.1.1. PlGF и sFlt-1 при болезненных состояниях и беременности
Одним из наиболее важных свойств эндотелиальных клеток сосудов является их способность пролиферировать и образовывать сеть капилляров посредством процесса, называемого ангиогенезом [33]. У нормального взрослого человека ангиогенный процесс строго регулируется и ограничивается эндометрием и яичниками во время различных фаз менструального цикла, а также сердцем и скелетными мышцами после травм из-за длительных и продолжительных физических упражнений [134].Этот процесс особенно заметен во время эмбрионального развития (Ramsey & Donner (1980) и Gilbert (1988), цитируется в [33]), поскольку ангиогенез важен для правильного развития эмбриона и для постнатального роста [134].
Сложное взаимодействие между некоторыми членами семейства белков VEGF, включая PlGF, и их родственными рецепторами, особенно Flt-1, имеет важное значение для возникновения ангиогенеза [2]. С другой стороны, растворимый вариант сплайсинга Flt-1, sFlt-1, секретируется в кровоток и действует как антиангиогенный фактор, поскольку он противодействует и нейтрализует PlGF и VEGF, связываясь с ними и ингибируя их взаимодействие с эндотелиальными рецепторами на клеточная поверхность [36, 45, 57].
PlGF присутствует на раннем этапе эмбрионального развития и на всех этапах беременности, поскольку он высоко экспрессируется плацентой. Было высказано предположение, что присутствие этого проангиогенного фактора служит контролем для роста и дифференцировки трофобластов [31, 37], что в свою очередь подразумевает, что PlGF играет роль во вторжении трофобласта в децидуальную оболочку матери [135]. Одновременно, хотя sFlt-1 секретируется в небольших количествах эндотелиальными клетками и моноцитами, плацента, по-видимому, служит основным источником sFlt-1 в кровотоке во время беременности. Это открытие подтверждается значительным падением уровня циркулирующего sFlt-1 после рождения плаценты [47].
У нормотензивной беременной женщины уровень PlGF в кровотоке матери постепенно увеличивается в течение первых двух триместров и достигает пика в середине беременности, а затем снова снижается по мере наступления срока беременности. С другой стороны, уровень sFlt-1 у беременных с нормальным АД остается относительно стабильным в течение первых двух триместров, после чего он неуклонно увеличивается до срока родов [45, 47, 53].Эту гестационную вариацию можно наблюдать в результатах, представленных на диаграммах ниже, которые были получены в проспективном многоцентровом исследовании: диагностика преэклампсии (исследование Roche № CIM RD000556 / X06P006). В этом исследовании уровни PlGF и sFlt-1 были измерены у нормотензивных женщин из стран Европы, у которых была одноплодная беременность и которые в дальнейшем имели нормальные исходы беременности (без PE / HELLP и без IUGR) (рисунки 3 и 4).
Уровни этих биомаркеров также были исследованы в материнском кровообращении пациентов с ПЭ.Имеются убедительные доказательства снижения встречаемости свободного, биоактивного PlGF вместе с более высокой экспрессией sFlt-1 в плаценте и, как следствие, повышенными уровнями циркулирующего sFlt-1 у пациентов с преэклампсией во время активного заболевания по сравнению с беременными женщинами с нормотензивным давлением [46, 47 , 50, 53, 55, 67].
В большом поперечном исследовании, сравнивающем гестационных женщин соответствующего возраста с активной ТЭЛА и нормотензивной беременностью, уровни PlGF были ниже, а уровни sFlt-1 были выше в преэкламптической группе (средний уровень PlGF 137 пг / мл по сравнению с 669 пг / мл; средний уровень sFlt-1 4382 пг / мл против 1643 пг / мл) [53].Считается, что снижение уровней PlGF связано с повышенной концентрацией циркулирующего sFlt-1 с 33 до 36 недель беременности и, следовательно, с увеличением связывания PlGF с sFlt-1, а не с уменьшением PlGF, вызванным снижением продукции PlGF [ 53].
В 2003 году Maynard et al. вводили экзогенный sFlt-1 беременным крысам, и, что примечательно, это привело к снижению уровней PlGF, гипертензии и протеинурии, симптомам, параллельным тем, которые наблюдаются у пациентов с ПЭ [47]. Это открытие привело к мысли, что материнская эндотелиальная дисфункция, которая отмечается у пациентов с преэклампсией, вызвана дисбалансом уровней про- и антиангиогенных факторов в материнском кровообращении.Существует множество подтверждающих данных, предполагающих, что антагонизм sFlt-1 к PlGF может быть ответственным за эндотелиальную дисфункцию при PE [59, 60].
Дефицит PlGF и избыток sFlt-1, наблюдаемые у пациентов с преэклампсией, также могут быть связаны с гипоксией плаценты, которая связана с неполным ремоделированием спиральных артерий матери. Эта дефектная плацентация в результате неполной ремоделирования артерий оказывает постоянно высокое сопротивление кровотоку в маточной артерии, что, в свою очередь, может предрасполагать к разрыву сосудов в плацентарном ложе, особенно после начала гипертонии [136, 137]. Однако необходимы дополнительные доказательства, чтобы определить, являются ли измененные уровни этих про- и антиангиогенных факторов следствием или причиной дефекта плацентации у женщин с ПЭ.
Однако необходимы дополнительные доказательства, чтобы определить, являются ли измененные уровни этих про- и антиангиогенных факторов следствием или причиной дефекта плацентации у женщин с ПЭ.
Исследования показали, что уровень материнского PlGF был более значительно снижен у пациентов с тяжелыми симптомами ТЭЛА по сравнению с беременными женщинами с нормальным давлением и женщинами с симптомами легкой ТЭЛА. С другой стороны, в случае материнских уровней sFlt-1 было показано, что повышенные уровни коррелируют с тяжестью ПЭ, при этом средние уровни sFlt-1 варьируются от 1.От 50 ± 0,22 нг / мл у беременных с нормальным артериальным давлением до 3,28 ± 0,83 нг / мл у женщин с легкой формой ПЭ и до 7,64 ± 1,5 нг / мл у женщин с тяжелой формой ПЭ [47, 48]. Кроме того, было отмечено, что вариации PlGF и sFlt-1 более выражены при раннем начале ПЭ по сравнению с поздним началом ПЭ, а также у женщин, перенесших ПЭ и позже родивших новорожденных с малым для гестационного возраста (SGA) рождением [53, 56]. Результаты, полученные Levine et al. [53], которые показывают эти различия, представлены на рисунках 5 и 6.
Результаты, полученные Levine et al. [53], которые показывают эти различия, представлены на рисунках 5 и 6.
В исследовании Levine et al.также сообщалось, что увеличение уровней sFlt-1 в кровообращении у пациентов с ПЭ соответствует уменьшению свободного PlGF [53]. Более того, также было замечено, что изменения уровней этих факторов опережают клинический диагноз на несколько недель. Фактически, важным открытием в этом исследовании было то, что повышенный уровень sFlt-1 может быть обнаружен в материнской сыворотке за 5 недель до появления клинических симптомов ПЭ, в то время как пониженный уровень PlGF может быть обнаружен с 13 до 16 недель гестации у беременных. женщины, у которых впоследствии развивается ПЭ.Позже это открытие было обнаружено в ряде других исследований [20, 53, 58, 62–66, 68–72, 138].
Эти данные позволяют предположить, что измерение PlGF и sFlt-1 может быть использовано для прогнозирования развития ПЭ за несколько недель до клинического проявления симптомов этого заболевания (рис. 7). Комбинированное измерение PlGF и sFlt-1 также позволило выявить женщин, у которых впоследствии развилась ПЭ, от женщин, у которых впоследствии развилась гестационная гипертензия, родились новорожденные с SGA или закончилась нормальная, здоровая доношенная беременность [47, 52].
7). Комбинированное измерение PlGF и sFlt-1 также позволило выявить женщин, у которых впоследствии развилась ПЭ, от женщин, у которых впоследствии развилась гестационная гипертензия, родились новорожденные с SGA или закончилась нормальная, здоровая доношенная беременность [47, 52].
Согласно некоторым исследованиям, измененные уровни sFlt-1 специфичны для ПЭ, поскольку не обнаружено никаких изменений у женщин, которые впоследствии родили новорожденных с SGA или чьи беременности были осложнены ЗВУР по сравнению с женщинами с нормальным давлением и нормальным исходом беременности [51, 58] . Однако в отобранной группе пациенток с аномальной перфузией матки с последующей ЗВУР другие исследования выявили аналогичные изменения в уровнях PlGF и sFlt-1 во втором триместре [139].
Комбинация значений sFlt-1 и PlGF в виде отношения, как показано в проспективном многоцентровом исследовании: диагностика преэклампсии (исследование Roche No.CIM RD000556 / X06P006) (рис. 8) также использовался в качестве предиктора PE. В проспективном исследовании Rana et al. [61] было высказано предположение, что соотношение sFlt-1 и PlGF, по-видимому, является лучшим предиктором ПЭ, чем любой другой показатель по отдельности. Kim et al. [24] выявили, что отношение sFlt-1 к PlGF у женщин с преэклампсией было значительно выше по сравнению с нормальным контролем, поскольку медианное значение отношения log [sFlt-1 / PlGF] у женщин с преэклампсией составляло 1,6 (диапазон 1,0 — 2,9). , в то время как среднее значение в контрольной группе с нормальным АД составляло 1.2 (диапазон 0,5 — 1,9). В этом исследовании использовалось пороговое значение 1,4, поскольку оно показало чувствительность 80,4% и специфичность 78%, при этом женщины со значениями материнского логарифмического отношения [sFlt-1 / PlGF] более 1,4 имели более высокий риск развития ПЭ. Следовательно, это соотношение является надежным маркером общего риска ПЭ, и его можно использовать для различения нормальной беременности и беременности, осложненной ПЭ, и для определения степени тяжести ПЭ [2, 140].
В проспективном исследовании Rana et al. [61] было высказано предположение, что соотношение sFlt-1 и PlGF, по-видимому, является лучшим предиктором ПЭ, чем любой другой показатель по отдельности. Kim et al. [24] выявили, что отношение sFlt-1 к PlGF у женщин с преэклампсией было значительно выше по сравнению с нормальным контролем, поскольку медианное значение отношения log [sFlt-1 / PlGF] у женщин с преэклампсией составляло 1,6 (диапазон 1,0 — 2,9). , в то время как среднее значение в контрольной группе с нормальным АД составляло 1.2 (диапазон 0,5 — 1,9). В этом исследовании использовалось пороговое значение 1,4, поскольку оно показало чувствительность 80,4% и специфичность 78%, при этом женщины со значениями материнского логарифмического отношения [sFlt-1 / PlGF] более 1,4 имели более высокий риск развития ПЭ. Следовательно, это соотношение является надежным маркером общего риска ПЭ, и его можно использовать для различения нормальной беременности и беременности, осложненной ПЭ, и для определения степени тяжести ПЭ [2, 140].
Измерение PlGF и sFlt-1 лишь в редких случаях распространялось на младенцев, рожденных от преэкламптической беременности.В 2005 г. Staff et al. измеряли уровни PlGF и sFlt-1 у беременных женщин с нормальным давлением и преэклампсией и их новорожденных [49]. Результаты, полученные для матерей, отражали те же результаты, полученные в исследованиях, упомянутых в предыдущих разделах, при этом более низкие уровни PlGF и более высокие уровни sFlt-1 были отмечены в группе преэклампсии. В этом исследовании образцы пуповины, полученные от всех новорожденных, имели уровни PlGF, которые были ниже концентрации самого низкого стандарта набора для ELISA, использованного в исследовании (15,6 пг / мл), и, таким образом, сравнение между контрольными группами с преэклампсией и нормотензией не могло быть достигнуто.С другой стороны, средняя концентрация sFlt-1, полученная для плодов, рожденных от матерей с ПЭ, оказалась значительно выше, чем средняя концентрация, полученная для плодов, рожденных от матерей с нормальным АД (246 пг / мл, 95% ДИ для медианы 163– 255 против 163 пг / мл, 95% ДИ для медианы 136–201).
В то же время, хотя уровни sFlt-1 были выше у плодов, рожденных от матерей с ПЭ, концентрации sFlt-1, измеренные в образцах пуповины, были очень низкими по сравнению с концентрациями sFlt-1 у матери.Это открытие предполагает, что плод не вносит значительного вклада в повышенную концентрацию sFlt-1 у матери при ПЭ, что дополнительно подтверждает предположение о том, что повышение концентрации циркулирующего sFlt-1 у матерей с ПЭ происходит в основном из плаценты [49]. Этот вывод также согласуется с идеей о том, что у плода не наблюдается гипертонии или протеинурии, как у их преэклампсических матерей, потому что они не подвергаются воздействию высоких концентраций антиангиогенных факторов, включая sFlt-1, которые, хотя и имеют плацентарное происхождение, должны в первую очередь ограничиваться материнская сосудистая сеть [141].
3.2. Продукты метилирования белков
Метилирование белков — это посттрансляционная модификация (PTM), которая включает перенос метильных групп от S-аденозил-L-метионина (SAM) к определенному остатку белка под контролем определенных ферментов метилтрансферазы [142]. Это приводит к образованию метилированного субстрата и побочного продукта, S-аденозил-L-гомоцистеина (SAH), который затем расщепляется ферментом S-аденозилгомоцистеин гидролазой с образованием аденозина и гомоцистеина [143] (Рисунок 9).Такие PTM преимущественно нацелены на боковые цепи аргинина и лизина, но было показано, что другие аминокислотные остатки, включая гистидин, аспарагин, глутамин и цистеин, служат второстепенными мишенями для метилирования.
Это приводит к образованию метилированного субстрата и побочного продукта, S-аденозил-L-гомоцистеина (SAH), который затем расщепляется ферментом S-аденозилгомоцистеин гидролазой с образованием аденозина и гомоцистеина [143] (Рисунок 9).Такие PTM преимущественно нацелены на боковые цепи аргинина и лизина, но было показано, что другие аминокислотные остатки, включая гистидин, аспарагин, глутамин и цистеин, служат второстепенными мишенями для метилирования.
3.2.1. Асимметричный диметиларгинин (ADMA)
Различные типы метиларгинина синтезируются после метилирования аргинина, которое представляет собой PTM атома азота, составляющего часть гуанидиновой части группы аргинина (R) в белках. Белки, которые подвергаются метилированию аргинина, участвуют в ряде различных клеточных процессов, включая регуляцию транскрипции, метаболизм РНК и восстановление повреждений ДНК [144].Этот процесс включает добавление одной или двух метильных групп, полученных из S-аденозилметионина (SAM) [145], к гуанидиновому атому азота аргинина и достигается с помощью ферментов протеин-аргинин-N-метилтрансферазы (PRMT), которые относятся к семейство метилтрансфераз, связанных с последовательностью [146]..PNG)
ADMA частично выводится с мочой, но в основном метаболизируется путем гидролитического расщепления до цитруллина и диметиламина. Эта метаболическая реакция катализируется ферментом NG-диметиларгининдиметиламиногидролазой (DDAH) [147] (рис. 11). Существует 2 изоформы DDAH: DDAH-1 и DDAH-2. Ткани, экспрессирующие нейрональную синтазу оксида азота (NOS), обычно содержат DDAH-1, тогда как ткани, содержащие эндотелиальную изоформу NOS (eNOS), преимущественно содержат DDAH-2 [148].Таким образом, было замечено, что DDAH-1 обнаруживается в больших количествах в почках и печени, тогда как DDAH-2 является наиболее распространенной изоформой в эндотелии [145].
(1) ADMA при болезненных состояниях и беременности . В 1992 г. сообщалось, что АДМА является эндогенным конкурентным ингибитором NOS [149]. NOS отвечает за синтез оксида азота в эндотелиальных клетках, поскольку он катализирует превращение L-аргинина в L-цитруллин и NO [150]. ADMA является аналогом L-аргинина, который также синтезируется и высвобождается эндотелиальными клетками.
В 1992 г. сообщалось, что АДМА является эндогенным конкурентным ингибитором NOS [149]. NOS отвечает за синтез оксида азота в эндотелиальных клетках, поскольку он катализирует превращение L-аргинина в L-цитруллин и NO [150]. ADMA является аналогом L-аргинина, который также синтезируется и высвобождается эндотелиальными клетками.
NO играет несколько ролей в сердечно-сосудистой системе [144]. Это мощный вазоактивный медиатор, который высвобождается в ответ на стресс [151] и важен для поддержания эндотелиального гомеостаза [145]. Помимо индукции расширения сосудов для регулирования тонуса сосудов и тканевого кровотока [150–152], эндотелиальный NO также подавляет агрегацию тромбоцитов [153], ингибирует адгезию лейкоцитов и моноцитов к эндотелию [154] и подавляет пролиферацию гладкомышечных клеток [155]. .
Было отмечено, что снижение уровня или ингибирование DDAH, фермента, катализирующего гидролиз ADMA, приводит к более высоким уровням ADMA в кровотоке и вызывает постепенное сужение сосудов [156]. Это происходит потому, что повышенный уровень ADMA в кровотоке приводит к обратимому ингибированию эндогенного синтеза NO, что, в свою очередь, может привести к эндотелиальной дисфункции [157]. Низкий уровень NO приводит к повышению системного сосудистого сопротивления и артериального давления [75]. Высокие уровни АДМА наблюдались у лиц с сердечно-сосудистыми заболеваниями, включая атеросклероз, гипертензию и гиперхолестеринемию, а также у лиц с хронической почечной недостаточностью [145]. Обычные сердечно-сосудистые факторы риска могут снижать активность ДДАГ за счет увеличения окислительного стресса, что, в свою очередь, также приводит к повышенным уровням АДМА [148, 158–160].
Это происходит потому, что повышенный уровень ADMA в кровотоке приводит к обратимому ингибированию эндогенного синтеза NO, что, в свою очередь, может привести к эндотелиальной дисфункции [157]. Низкий уровень NO приводит к повышению системного сосудистого сопротивления и артериального давления [75]. Высокие уровни АДМА наблюдались у лиц с сердечно-сосудистыми заболеваниями, включая атеросклероз, гипертензию и гиперхолестеринемию, а также у лиц с хронической почечной недостаточностью [145]. Обычные сердечно-сосудистые факторы риска могут снижать активность ДДАГ за счет увеличения окислительного стресса, что, в свою очередь, также приводит к повышенным уровням АДМА [148, 158–160].
В исследовании 1998 года Holden et al. [73], было установлено, что у беременных женщин концентрация ADMA в кровообращении ниже, чем у небеременных. Их результаты показали, что, хотя средняя концентрация АДМА у небеременных женщин составляла 0,82 ± 0,31 мкМ моль / л, средние значения АДМА у беременных женщин находились в диапазоне 0,40 ± 0,15 мк моль / л в первом триместре, 0,52 ± 0,20 мкМ моль / л во втором триместре и 0,56 ± 0,22 мк моль / л в третьем триместре. Аналогичное наблюдение позже было сделано Маэдой и соавт. [79], которые также отметили более низкие средние концентрации АДМА у беременных (0,29 ± 0,05 мкг моль / л в первом и третьем триместрах и 0,32 ± 0,05 мкл моль / л в сроке) по сравнению со средними уровнями АДМА у небеременных. женщины (0,41 ± 0,06 мк моль / л). В то же время результаты Holden et al. выявили, что, хотя средние уровни АДМА ниже у беременных, они имеют тенденцию к увеличению в течение нормального гестационного периода [73].Этот вывод не отражен в результатах, полученных Maeda et al. поскольку последняя группа не отметила изменения средних уровней ADMA с первого по третий триместр (0,29 ± 0,05 мкг моль / л в первом и третьем триместрах), с единственным увеличением, отмеченным при доношенных сроках (0,32 ± 0,05 мкм моль / л при доношении) [79]. С другой стороны, повышение средних уровней ADMA во время беременности было обнаружено позже в исследовании Rizos et al. в 2012 году, которые показали, что средний уровень АДМА у беременных увеличился с 0.
 51 ± 0,14 мкм моль / л в первом триместре до 0,52 ± 0,13 мкм моль / л во втором триместре и, наконец, до 0,58 ± 0,16 мкм моль / л в третьем триместре [81] (Рисунок 12) . Такие данные позволяют предположить, что ADMA может играть роль в расширении сосудов и регуляции артериального давления во время беременности [73].
51 ± 0,14 мкм моль / л в первом триместре до 0,52 ± 0,13 мкм моль / л во втором триместре и, наконец, до 0,58 ± 0,16 мкм моль / л в третьем триместре [81] (Рисунок 12) . Такие данные позволяют предположить, что ADMA может играть роль в расширении сосудов и регуляции артериального давления во время беременности [73].
Многочисленные исследования измеряли уровень ADMA у беременных женщин, чтобы определить, существует ли значительная разница в концентрациях ADMA в кровообращении у женщин с ПЭ по сравнению с женщинами с неосложненной беременностью.
Наблюдалось противоречивых выводов. В отдельных исследованиях 1998 года Holden et al. [73] и Петтерссон и др. [80] наблюдали повышенные средние уровни АДМА в третьем триместре у пациенток с преэклампсией (1,17 ± 0,42 мк моль / л и 0,55 ± 0,02 мк моль / л соответственно) по сравнению с контрольной беременной с нормальным АД в течение того же периода гестации. (0,56 ± 0,22 мкм моль / л и 0,36 ± 0,01 мкм моль / л соответственно). Точно так же исследование Rizos et al.[81] также показали повышенные средние уровни АДМА во всех трех триместрах у пациентов с преэклампсией (0,58 ± 0,10 мкг моль / л в первом триместре, 0,63 ± 0,14 мкг моль / л во втором триместре и 0,68 ± 0,11 μ моль / л в третьем триместре) по сравнению с женщинами с неосложненной беременностью (0,51 ± 0,14 μ моль / л в первом триместре, 0,52 ± 0,13 μ моль / л во втором триместре и 0,58 ± 0,16 μ моль / л в третьем триместре). Однако в ряде других исследований, хотя медианные уровни ADMA продемонстрировали аналогичную тенденцию к увеличению у пациентов с преэклампсией, эти результаты не были статистически значимыми [74, 76, 77].
Точно так же исследование Rizos et al.[81] также показали повышенные средние уровни АДМА во всех трех триместрах у пациентов с преэклампсией (0,58 ± 0,10 мкг моль / л в первом триместре, 0,63 ± 0,14 мкг моль / л во втором триместре и 0,68 ± 0,11 μ моль / л в третьем триместре) по сравнению с женщинами с неосложненной беременностью (0,51 ± 0,14 μ моль / л в первом триместре, 0,52 ± 0,13 μ моль / л во втором триместре и 0,58 ± 0,16 μ моль / л в третьем триместре). Однако в ряде других исследований, хотя медианные уровни ADMA продемонстрировали аналогичную тенденцию к увеличению у пациентов с преэклампсией, эти результаты не были статистически значимыми [74, 76, 77].
Кроме того, повышенные концентрации ADMA были отмечены в кровообращении беременных женщин, у которых развилась ПЭ. Эта повышенная концентрация ADMA была отмечена до развития клинических признаков и симптомов ПЭ [82, 83], что позволяет предположить, что ADMA может играть роль в патогенезе этого состояния. Поскольку известно, что оксид азота играет важную роль в поддержании кровотока и тонуса сосудов матери и плода, а также в поддержании фето-материнского кровообращения, было высказано предположение, что повышенные уровни АДМА во время беременности, а также, как следствие, снижение уровней NO в кровообращении , может вносить вклад в патофизиологические особенности ПЭ [75, 79].
Поскольку известно, что оксид азота играет важную роль в поддержании кровотока и тонуса сосудов матери и плода, а также в поддержании фето-материнского кровообращения, было высказано предположение, что повышенные уровни АДМА во время беременности, а также, как следствие, снижение уровней NO в кровообращении , может вносить вклад в патофизиологические особенности ПЭ [75, 79].
Измерение уровней ADMA в образцах пуповинной крови может быть важным для объяснения регуляторных механизмов системы кровообращения в перинатальный период [84]. Однако данные об уровне ADMA у новорожденных ограничены. В ранее упомянутом исследовании Maeda et al. [79], также было замечено, что уровень ADMA, измеренный в пуповинной крови, был значительно выше, чем у матери, который был самым высоким в срок (1,02 ± 0,18 мк моль / л по сравнению с 0.32 ± 0,05 мкм моль / л соответственно). Позже это открытие было обнаружено Tsukahara et al. [84], которые отметили, что уровни ADMA, измеренные в пуповинной крови у контрольных новорожденных (новорожденных, рожденных от матерей с нормальным АД после неосложненной беременности), были примерно в два раза выше, чем уровни ADMA, измеренные у кормящих женщин, здоровых детей и здоровых взрослых (1,71 ± 0,47 мкм моль / л против 0,71 ± 0,06 мкм моль / л, 0,71 ± 0,11 мкм моль / л и 0,52 ± 0,12 мкм моль / л соответственно).
При сравнении уровней ADMA, измеренных в пуповинной крови контрольных новорожденных и новорожденных, рожденных от матерей с ПЭ, Tsukahara et al. [84] не обнаружили значительной разницы между ними, так как их соответствующие средние значения составляли 1,71 ± 0,47 мк моль / л и 1,66 ± 0,33 мк моль / л. Однако в недавнем исследовании Gumus et al. [78], медианные значения ADMA были значительно выше в пуповинной крови у новорожденных, рожденных от матерей с ПЭ, чем у новорожденных из контрольной группы (8.344 нг / л против 4,603 нг / л). Также было отмечено, что уровень ADMA, измеренный в образце пуповинной крови, коррелировал с тяжестью преэкламптического расстройства.
3.2.2. Метил-лизин
В случае метилирования лизина специфические белковые лизинметилтрансферазы (KMT) катализируют перенос одной, двух или трех метильных групп от SAM к эпсилон ( ε ) -аминовой группе боковой цепи конкретный остаток лизина [142]. Это приводит к образованию различных форм метилированных лизинов, а именно, монометил-, диметил- и триметил-лизинов соответственно [142] (Рисунок 13). Некоторые белковые KMT специфичны для одной или двух из этих модификаций, в то время как другие могут приводить к образованию всех трех производных [161]. Таким образом, было показано, что эти ферменты проявляют специфичность продукта, поскольку тип производимого метил-лизина зависит от конкретного фермента, катализирующего реакцию [162].
Некоторые белковые KMT специфичны для одной или двух из этих модификаций, в то время как другие могут приводить к образованию всех трех производных [161]. Таким образом, было показано, что эти ферменты проявляют специфичность продукта, поскольку тип производимого метил-лизина зависит от конкретного фермента, катализирующего реакцию [162].
Было идентифицировано девять функциональных членов семейства PRMT (PRMT1-9), и специфичность этих ферментов в отношении белковых субстратов варьирует и обычно намного шире, чем у KMT.Например, было показано, что PRMT1, 2, 3, 4, 6 и 8 катализируют асимметрическое диметилирование остатков аргинина, тогда как фермент PRMT5 катализирует симметричное диметилирование, а PRMT7 может катализировать только монометилирование [163–165].
Большинство ферментов метилтрансфераз сгруппированы в соответствии с их структурными особенностями в три больших семейства, а именно: семь бета ( β ) цепей [166], SET ( s супрессор пестролистности 3-9 (Su (var) 3-9 ), e nhancer zeste (E (z)) и t rithorax (Trx)) ферменты, содержащие домен [167], и SPOUT домен [168]. Однако, хотя все PRMT принадлежат к семейству ферментов из семи цепей β , большинство KMT содержат консервативный домен SET [169], который несет ферментативную активность этих белков [170], и, следовательно, принадлежат домену SET — содержащее семейство [171, 172]. Более того, было показано, что все большее количество ферментов, принадлежащих к семейству семи цепей β , катализируют сходные реакции метилирования [173–176]. Таким образом, KMT могут быть в широком смысле разделены в соответствии с их ферментативным доменом на белки, содержащие домен SET и не содержащие домен SET.
Однако, хотя все PRMT принадлежат к семейству ферментов из семи цепей β , большинство KMT содержат консервативный домен SET [169], который несет ферментативную активность этих белков [170], и, следовательно, принадлежат домену SET — содержащее семейство [171, 172]. Более того, было показано, что все большее количество ферментов, принадлежащих к семейству семи цепей β , катализируют сходные реакции метилирования [173–176]. Таким образом, KMT могут быть в широком смысле разделены в соответствии с их ферментативным доменом на белки, содержащие домен SET и не содержащие домен SET.
KMT, содержащие домен SET, были классифицированы на ряд семейств в соответствии с мотивами последовательностей, окружающих домен SET. Члены одного и того же семейства имеют сходные мотивы последовательностей, окружающие домен SET, и часто также имеют более высокий уровень сходства в домене SET. Известно семь основных семейств, в том числе супрессор пестроты (Su (var)) 3-9 (SUV39), SET1, SET2, энхансер zeste (E (z)), белок цинковых пальцев, взаимодействующий с ретинобластомой (RIZ), SET и белок, содержащий домен Myeloid-Nervy-DEAF1 (MYND) (SMYD), и супрессор семейств пестроты (Su (var)) 4-20 (SUV4-20). Эти семейства сопровождаются SET7 / 9 и SET8 (также известными как PR-SET7), которые представляют собой KMT, содержащие домен SET, но не вписываются в ранее упомянутые семейства [177]. Табулированный список KMTs, обнаруженных у людей, которые принадлежат к каждому семейству KMT, а также SET7 / 9 и SET8, вместе с их свойствами был представлен Dillon et al. [177].
Эти семейства сопровождаются SET7 / 9 и SET8 (также известными как PR-SET7), которые представляют собой KMT, содержащие домен SET, но не вписываются в ранее упомянутые семейства [177]. Табулированный список KMTs, обнаруженных у людей, которые принадлежат к каждому семейству KMT, а также SET7 / 9 и SET8, вместе с их свойствами был представлен Dillon et al. [177].
Хотя подавляющее большинство KMT содержат домен SET, многие другие белки не содержат домен SET, включая d isruptor o f t эломерный сайленсинг (DOT) 1-подобный (DOT1L) [169 , 178] и белки семейства метилтрансферазоподобных (METTL) [179] также обладают лизинметилтрансферазной активностью.
(1) Метилирование лизина при болезненных состояниях и беременности. На протяжении многих лет были идентифицированы многочисленные KMT и лизин-деметилазы (KDM), и их активность, как сообщается, важна в нескольких биологических процессах, включая регуляцию экспрессии генов, прогрессию клеточного цикла, репликацию ДНК и дифференцировку [180–18]. 185]. В нормальном, здоровом состоянии метилирование лизина строго контролируется, а баланс метилирования лизина поддерживается за счет противоположных действий KMT и KDM [186].В то же время паттерны экспрессии генов должны быть способны реагировать на требования развития и изменения окружающей среды, чтобы поддерживать здоровое состояние [187].
185]. В нормальном, здоровом состоянии метилирование лизина строго контролируется, а баланс метилирования лизина поддерживается за счет противоположных действий KMT и KDM [186].В то же время паттерны экспрессии генов должны быть способны реагировать на требования развития и изменения окружающей среды, чтобы поддерживать здоровое состояние [187].
Нарушение регуляции PTMs в форме несоответствующей экспрессии (включение или исключение), а также мутации многих KMTs и KDMs могут быть критическим детерминантом различных заболеваний, включая старение и рак [186–191]. Фактически, потеря этого необходимого баланса метилирования во взрослых стволовых клетках, как полагают, вносит вклад в снижение функции тканей с возрастом [192].Исследования также показали, что аберрантное метилирование связано с повышенной частотой различных типов рака и плохой выживаемостью [193, 194]. Например, метилтрансфераза, ответственная за триметилирование гистона 3 лизина 27 (h4K27me3), активируется при раке простаты [195], раке груди [196] и лимфомах [197].
Геном человека кодирует более 200 метилтрансфераз [198], и хотя большинство исследований сосредоточено на метилировании гистонов, ряд сообщений показал, что эти ферменты также ответственны за регуляцию метилирования негистоновых белков [199].Было замечено, что ряд негистоновых белков подвергаются метилированию по своим лизиновым остаткам, что, в свою очередь, приводит к изменениям функции и / или стабильности этих негистоновых белков [199, 200]. Сообщалось о доказательствах зависимой от метилирования лизина регуляции для постоянно увеличивающегося числа негистоновых белков, и в некоторых случаях эти изменения также могут иметь отношение к стрессу, гипертонии и ПЭ, как описано ниже.
Метилирование лизина р53 . Белок-супрессор опухолей р53 функционирует как специфичный для последовательности фактор транскрипции, который регулирует важные клеточные процессы, включая остановку клеточного цикла, репарацию ДНК, апоптоз и старение в ответ на сигналы стресса.В нормальных условиях уровень р53 в клетке поддерживается на низком уровне; однако р53 быстро стабилизируется и активируется в ответ на клеточные стрессы, такие как повреждение ДНК и гипоксические состояния [143].
Было показано, что апоптоз трофобластов в плаценте человека увеличивается во время гестационного периода [201]. Более того, при беременности, осложненной ТЭЛА, отмечается нарушение регуляции клеточного обмена, что приводит к усилению апоптоза [202–204] и уменьшению площади синцитиотрофобластов [205].Влияние чрезмерного апоптоза на патологию плаценты при ТЭЛА неясно; однако это может в конечном итоге предотвратить восполнение синцитиотрофобласта, способствовать дегенерации синцития и привести к высвобождению вазоактивных или воспалительных факторов в кровоток матери [206]. Поскольку p53 является жизненно важным регулятором апоптотического пути, его уровень был измерен в случаях PE, и было замечено, что на уровне белка уровень p53 значительно повышен в плаценте, полученной от беременностей, осложненных PE [207] .Такое увеличение экспрессии р53 отмечалось также в случаях ЗВУР плода [208, 209]. Также увеличение уровней p53 было связано с повышенной экспрессией нижестоящих элементов апоптотического пути, включая уровень нижестоящего эффекторного белка p21 [207].
Метилирование p53 с помощью SET7 (KMT7) было первым описанным KMT-опосредованным метилированием негистонового белка [210]. С тех пор появился ряд других KMT, включая SET9 (KMT5), SMYD2 (KMT3C) и SET 8 (KMT5A), которые метилируют p53 по определенным C-концевым лизинам, вместе с лизин-специфической деметилазой KDM1 (LSD1), которая опосредует деметилирование р53 также было идентифицировано [143] (рис. 14).
P53 подвергается множественным PTM, включая метилирование лизина, которые регулируют его стабильность, межбелковые взаимодействия и транскрипционную активность. Фактически, транскрипционная активность р53 усиливается или подавляется в зависимости от сайта метилирования. Кроме того, взаимодействие p53 с его коактиватором p53-связывающим белком 1 (53BP1) для индукции апоптоза опосредуется действием лизиндеметилазы KDM1. Баланс между метилированием и деметилированием в сочетании с другими PTMs важен для ответа p53 на клеточные стрессы, поскольку его активность важна для предотвращения образования опухолей [143].
Метилирование лизином белка теплового шока (HSP) 70 . HSP в первую очередь известны как внутриклеточные белки, которые обладают молекулярными шаперонами и цитопротекторными функциями [211] и необходимы для восстановления клеток, выживания и поддержания гомеостаза [212]. Белки HSP70 являются повсеместными, зависимыми от аденозинтрифосфата (АТФ) молекулярными шаперонами, которые составляют одно из наиболее эволюционно консервативных семейств белков [213]. Внеклеточный HSP70 может способствовать развитию аутоиммунного заболевания и может служить индикатором состояния врожденной иммунной системы [214–216].У человека эти белки кодируются 13 генами, и они либо индуцируются в ответ на стресс (например, тепловой шок), либо экспрессируются конститутивно [217]. Белки HSP70 осуществляют множество биологических процессов, включая белок-белковые взаимодействия, деградацию белков и транслокацию через мембраны [218].
Было показано, что уровень HSP70 повышен при ПЭ [212, 219]. Park et al. [220] предположили, что повышенные уровни системного HSP70 у пациентов с преэклампсией происходят из синцитиотрофобластов и эндотелиальных клеток ворсинок преэклампсической плаценты, поскольку они, как было показано, имеют более высокие уровни белков HSP70 по сравнению с плацентой от нормальной, здоровой беременности.Другие исследования также обнаружили более высокие уровни HSP70 в тканях плаценты у пациентов с преэклампсией [221, 222]. Это увеличение сывороточного HSP70 отражает системное воспаление и окислительный стресс, которые отмечаются при ПЭ [212, 219]. Первоначально экспрессия HSP70 играет защитную роль против оксидативного стресса плаценты; однако избыточная экспрессия HSP70 может приводить к дисфункции межворсинчатого эндотелия и может играть роль в патогенезе ПЭ [220].
Park et al. [220] предположили, что повышенные уровни системного HSP70 у пациентов с преэклампсией происходят из синцитиотрофобластов и эндотелиальных клеток ворсинок преэклампсической плаценты, поскольку они, как было показано, имеют более высокие уровни белков HSP70 по сравнению с плацентой от нормальной, здоровой беременности.Другие исследования также обнаружили более высокие уровни HSP70 в тканях плаценты у пациентов с преэклампсией [221, 222]. Это увеличение сывороточного HSP70 отражает системное воспаление и окислительный стресс, которые отмечаются при ПЭ [212, 219]. Первоначально экспрессия HSP70 играет защитную роль против оксидативного стресса плаценты; однако избыточная экспрессия HSP70 может приводить к дисфункции межворсинчатого эндотелия и может играть роль в патогенезе ПЭ [220].
Было показано, что HSP70 может быть посттрансляционно модифицирован множеством способов, и сообщалось о многочисленных метилированных лизинах (Рисунок 15).Например, сообщалось, что остаток лизина K561, который обнаружен в нескольких белках HSP70 человека, может быть метилирован. Метилирование лизина белков HSP70 физиологически важно, особенно при онкогенезе. В частности, диметилирование K561 HSP70 с помощью SETD1A регулирует субклеточную локализацию этого белка и способствует пролиферации раковых клеток благодаря его взаимодействию с Aurora Kinase B (AURKB) [143, 223].
Метилирование лизина белков HSP70 физиологически важно, особенно при онкогенезе. В частности, диметилирование K561 HSP70 с помощью SETD1A регулирует субклеточную локализацию этого белка и способствует пролиферации раковых клеток благодаря его взаимодействию с Aurora Kinase B (AURKB) [143, 223].
Метилирование лизином рецепторов фактора роста эндотелия сосудов 1 (VEGFR-1) и 2 (VEGFR-2). Как было описано в предыдущих разделах, VEGFR-1 (или Flt-1) и VEGFR-2 представляют собой мембранные рецепторы, которые принадлежат к подсемейству рецепторных тирозинкиназ (RTK). VEGRF-1 способен прочно связываться со своими лигандами, VEGF (включая VEGF-A) и PlGF, но обладает слабой тирозинкиназной активностью и, следовательно, генерирует более слабый сигнал, чем другие RTK [224]. Благодаря взаимодействию со своими лигандами, VEGFR-1 играет важную роль как в физиологическом, так и в патологическом ангиогенезе, процессе, посредством которого новые кровеносные сосуды формируются из уже существующих сосудов [43, 225, 226]. Ангиогенез имеет решающее значение для нормальных физиологических функций тканей, но он также важен для прогрессирования некоторых заболеваний, включая рак и воспаление [227, 228].
Ангиогенез имеет решающее значение для нормальных физиологических функций тканей, но он также важен для прогрессирования некоторых заболеваний, включая рак и воспаление [227, 228].
VEGFR-1, как было показано, играет важную роль в регуляции васкулогенеза, который представляет собой процесс, посредством которого новые кровеносные сосуды формируются из клеток-предшественников во время раннего эмбриогенеза [225]. В 1995 году Фонг и др. [229] продемонстрировали, что мутантные мыши, которые не экспрессируют VEGFR-1 (Flt-1-null, Flt-1 — / — мыши), умирают внутриутробно из-за неконтролируемого роста эндотелиальных клеток сосудов и дезорганизации кровеносных сосудов, что указывает на то, что VEGFR-1 может играть отрицательную регуляторную роль в ангиогенезе на раннем этапе эмбриогенеза.
VEGFR-1 вместе со своим лигандом VEGF и другими рецепторами для VEGF экспрессируется в течение гестационного периода в плаценте, и они необходимы для развития сосудов эмбриона [34, 35]. Во время нормальной, неосложненной беременности VEGFR-1 может в первую очередь обнаруживаться в синцитиотрофобластах плаценты [230]. Измененные уровни VEGF и его рецепторов во время беременности могут привести к нарушению ангиогенеза, что приводит к плацентарной недостаточности и эндотелиальной дисфункции, которые наблюдаются при беременности, осложненной ПЭ [231].В исследовании Helske et al. [230], экспрессия VEGFR-1 увеличивалась в синцитиотрофобластах плаценты, полученных в ряде случаев ПЭ, но не во всех.
Измененные уровни VEGF и его рецепторов во время беременности могут привести к нарушению ангиогенеза, что приводит к плацентарной недостаточности и эндотелиальной дисфункции, которые наблюдаются при беременности, осложненной ПЭ [231].В исследовании Helske et al. [230], экспрессия VEGFR-1 увеличивалась в синцитиотрофобластах плаценты, полученных в ряде случаев ПЭ, но не во всех.
VEGFR-1 подвергается метилированию по нескольким остаткам лизина, и было замечено, что это метилирование важно для регуляции активности VEGFR-1 (фиг. 16). Например, было показано, что VEGFR-1 является негистоновой мишенью для метилтрансферазы SMYD3, поскольку лизин 831 VEGFR-1 метилируется с помощью SMYD3 in vitro [232].Это метилирование VEGFR-1 усиливает его киназную активность, поскольку лизин 831 расположен в киназном домене этой RTK.
VEGFR-2 представляет собой мощный ангиогенный RTK, что делает его одним из наиболее важных RTK в эндотелиальных клетках [233, 234]. Было отмечено, что активность VEGFR-2 играет важную роль как в васкулогенезе, так и в патологическом ангиогенезе во время рака и нейроваскуляризации глаз [226].
Следовательно, экспрессия и функция VEGFR-2 строго регулируются, поскольку усиленный ангиогенез играет значительную роль в прогрессировании рака и других заболеваний, включая возрастную дегенерацию желтого пятна, тогда как недостаточный ангиогенез связан с ишемической болезнью сердца и замедляется. заживление ран [234].VEGFR-2 подвергается метилированию по множеству остатков лизина, и было показано, что это метилирование важно для регуляции активности VEGFR-2 [233]. Фактически, Hartsough et al. [233] также определили, что метилирование лизина 1043 необходимо для контроля активации VEGFR-2, поскольку эта реакция метилирования важна для фосфорилирования тирозина этой RTK. Следовательно, вмешательство этого метилирования VEGFR-2 приводит к неспособности VEGFR-2 стимулировать ангиогенез.
4. Заключение
Как и все биомаркеры, их эффективность определяется способностью диагностировать заболевание задолго до появления клинических симптомов, а преимущество заключается в том, что изменения могут быть обнаружены с помощью минимально инвазивных анализов крови, выполняемых как часть плановых проверок. До сих пор PlGF и sFlt-1, по отдельности или в комбинации, не только показали перспективу для ранней диагностики ПЭ, но также показали, что они хорошо коррелируют с тяжестью этого состояния, при этом данные из разных когорт сопоставимы.Точно так же скрининг на ADMA привел к интересным тенденциям и может считаться полезным кандидатом в биомаркеры, также основываясь на знании его роли в биохимии NO. Наша лаборатория также заинтересована в изучении метилирования лизина в сочетании с вышеупомянутыми потенциальными биомаркерами, чтобы расширить понимание роли метилирования белка в нормальной биохимии и биохимии ПЭ. Помимо выбранных биомаркеров, конечной целью является улучшение течения и исхода беременности, а также снижение рисков для матери и плода.Этого можно достичь только путем раскрытия и лучшего понимания основных механизмов, ведущих к преэклампсическому состоянию.
До сих пор PlGF и sFlt-1, по отдельности или в комбинации, не только показали перспективу для ранней диагностики ПЭ, но также показали, что они хорошо коррелируют с тяжестью этого состояния, при этом данные из разных когорт сопоставимы.Точно так же скрининг на ADMA привел к интересным тенденциям и может считаться полезным кандидатом в биомаркеры, также основываясь на знании его роли в биохимии NO. Наша лаборатория также заинтересована в изучении метилирования лизина в сочетании с вышеупомянутыми потенциальными биомаркерами, чтобы расширить понимание роли метилирования белка в нормальной биохимии и биохимии ПЭ. Помимо выбранных биомаркеров, конечной целью является улучшение течения и исхода беременности, а также снижение рисков для матери и плода.Этого можно достичь только путем раскрытия и лучшего понимания основных механизмов, ведущих к преэклампсическому состоянию.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов в отношении публикации этой статьи.

 найденный.Это приводит к путанице, непониманию и непониманию.
предотвращает сравнение результатов и тем самым прогресс
ίπ исследования.
найденный.Это приводит к путанице, непониманию и непониманию.
предотвращает сравнение результатов и тем самым прогресс
ίπ исследования. Гипертоническая сосудистая болезнь Наложенный
токсемия
Гипертоническая сосудистая болезнь Наложенный
токсемия  Токсемия, токсикоз.
Токсемия, токсикоз.  д..) В неблагополучных районах кровь
аппарат под давлением, стетоскоп и инструкция
как использовать и то, и другое — это неслыханная вещь. В
показания артериального давления были значительно выше
оценка (Решение: ο быть
упал)
д..) В неблагополучных районах кровь
аппарат под давлением, стетоскоп и инструкция
как использовать и то, и другое — это неслыханная вещь. В
показания артериального давления были значительно выше
оценка (Решение: ο быть
упал)  EC)
Мы знаем об очень редких случаях молчания
эклампсия. (Решение: не принимать во внимание)
EC)
Мы знаем об очень редких случаях молчания
эклампсия. (Решение: не принимать во внимание)  .. osis). И если
эта нарушенная беременность имеет признаки и симптомы
EdemaJ и / или
Протеинурия и / или
Гипертония, тогда это ΕΡΗ -гестоз, который мы можем
подразделяют на несколько групп:
.. osis). И если
эта нарушенная беременность имеет признаки и симптомы
EdemaJ и / или
Протеинурия и / или
Гипертония, тогда это ΕΡΗ -гестоз, который мы можем
подразделяют на несколько групп:  ]
] ст., более 20 недель беременности (у женщины с ранее нормальным артериальным давлением)
ст., более 20 недель беременности (у женщины с ранее нормальным артериальным давлением) A
A