Цефалоспорины: фармакологическая группа
Описание
В зависимости от особенностей антимикробного спектра выделяют 5 поколений цефалоспоринов.
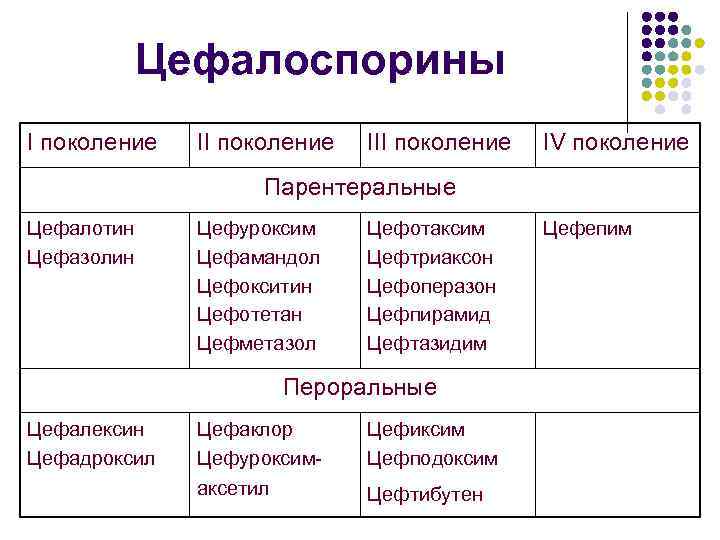
Цефалоспорины I поколения: парентеральные — цефазолин, пероральные — цефалексин.
Цефалоспорины II поколения: парентеральные — цефуроксим, пероральные — цефуроксима аксетил, цефаклор.
Цефалоспорины III поколения: парентеральные — цефотаксим, цефтриаксон, цефоперазон, цефоперазон/сульбактам, цефтазидим, пероральные — цефдиторен, цефиксим, цефподоксим, цефтибутен.
Цефалоспорины IV поколения: парентеральные — цефепим, цефпиром.
Цефалоспорины V поколения (анти-MRSA-цефемы): парентеральные — цефтаролин, цефтобипрол.
Цефалоспорины I поколения обладают преимущественной активностью в отношении грамположительных кокков — стафилококков и стрептококков. Грамотрицательные бактерии резистентны, исключение составляют некоторые внебольничные штаммы Е. coli и Р. mirabilis. Применяют при инфекциях кожи и мягких тканей, костей и суставов, для периоперационной профилактики. В качестве альтернативных средств используют при эндокардите и сепсисе, вызванных метициллиночувствительными стафилококками и зеленящими стрептококками. Цефазолин плохо проникает через ГЭБ. Выводится преимущественно с мочой, Т1/2 — 2 ч, вводят 2–3 раза в сутки. Цефалексин имеет высокую биодоступность при пероральном приеме. Основные показания к применению цефалексина: стрептококковый фарингит, стрептококковые и стафилококковые неосложненные внебольничные инфекции кожи и мягких тканей.
В качестве альтернативных средств используют при эндокардите и сепсисе, вызванных метициллиночувствительными стафилококками и зеленящими стрептококками. Цефазолин плохо проникает через ГЭБ. Выводится преимущественно с мочой, Т1/2 — 2 ч, вводят 2–3 раза в сутки. Цефалексин имеет высокую биодоступность при пероральном приеме. Основные показания к применению цефалексина: стрептококковый фарингит, стрептококковые и стафилококковые неосложненные внебольничные инфекции кожи и мягких тканей.
Цефалоспорины II поколения, обладая сходной с цефалоспоринами I поколения активностью в отношении грамположительных кокков, превосходят их по действию на грамотрицательные бактерии, прежде всего Н. influenzae. Хорошо распределяются (кроме ЦНС), выделяются преимущественно почками, имеют близкие Т1/2 (около 1 ч). Применяют для лечения внебольничных инфекций, для периоперационной профилактики.
Парентеральные цефалоспорины III поколения имеют высокую природную активность в отношении грамотрицательных бактерий (семейство Enterobacteriaceae, Н.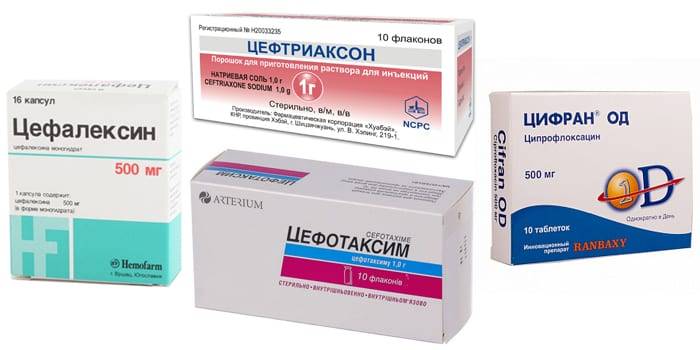 influenzae, N. gonorrhoeae, N. meningitidis), не инактивируются многими β-лактамазами. Разрушаются β-лактамазами расширенного спектра и β-лактамазами класса С (AmpС). Цефтазидим и цефоперазон активны в отношении Р. aeruginosa. По активности в отношении стафилококков значительно уступают ЛС I и II поколений, но в отношении стрептококков и пневмококков цефотаксим и цефтриаксон превосходят другие цефалоспорины и действуют на многие пенициллинорезистентные штаммы. Цефтазидим практически неактивен против грамположительных бактерий. Все ЛС этой группы хорошо распределяются в организме, проникают (кроме цефоперазона) через ГЭБ и могут использоваться для лечения инфекций ЦНС. Цефотаксим и цефтазидим выводятся почками, цефоперазон и цефтриаксон — почками и печенью. Все цефалоспорины III поколения имеют сходные Т1/2 (1,2–2 ч), за исключением цефтриаксона (около 7 ч). Применяют для лечения тяжелых внебольничных и нозокомиальных инфекций, вызванных грамотрицательными микроорганизмами.
influenzae, N. gonorrhoeae, N. meningitidis), не инактивируются многими β-лактамазами. Разрушаются β-лактамазами расширенного спектра и β-лактамазами класса С (AmpС). Цефтазидим и цефоперазон активны в отношении Р. aeruginosa. По активности в отношении стафилококков значительно уступают ЛС I и II поколений, но в отношении стрептококков и пневмококков цефотаксим и цефтриаксон превосходят другие цефалоспорины и действуют на многие пенициллинорезистентные штаммы. Цефтазидим практически неактивен против грамположительных бактерий. Все ЛС этой группы хорошо распределяются в организме, проникают (кроме цефоперазона) через ГЭБ и могут использоваться для лечения инфекций ЦНС. Цефотаксим и цефтазидим выводятся почками, цефоперазон и цефтриаксон — почками и печенью. Все цефалоспорины III поколения имеют сходные Т1/2 (1,2–2 ч), за исключением цефтриаксона (около 7 ч). Применяют для лечения тяжелых внебольничных и нозокомиальных инфекций, вызванных грамотрицательными микроорганизмами. Цефоперазон/сульбактам — комбинация цефалоспорина III поколения с ингибитором β-лактамаз сульбактамом — по сравнению с цефалоспоринами обладает расширенным спектром активности, включая анаэробы и многие нозокомиальные штаммы бактерий, в т.ч. большинство штаммов, продуцирующих β-лактамазы расширенного спектра.
Цефоперазон/сульбактам — комбинация цефалоспорина III поколения с ингибитором β-лактамаз сульбактамом — по сравнению с цефалоспоринами обладает расширенным спектром активности, включая анаэробы и многие нозокомиальные штаммы бактерий, в т.ч. большинство штаммов, продуцирующих β-лактамазы расширенного спектра.
Пероральные цефалоспорины III поколения цефиксим и цефтибутен активны в отношении энтеробактерий и гемофильной палочки, но в отношении грамположительных микроорганизмов, включая пневмококки, стрептококки и стафилококки, их активность невысока; поэтому их не следует применять при грамположительных инфекциях, особенно при внебольничной пневмонии. Цефдиторен, в отличие от цефиксима и цефтибутена, обладает высокой активностью против стафилококков и стрептококков (в т.ч. пневмококков), в связи с чем не имеет вышеуказанных ограничений.
Цефалоспорины IV поколения характеризуются высокой активностью в отношении грамотрицательных бактерий, включая Р. aeruginosa, и повышенной по сравнению с препаратами III поколения (цефтазидим) активностью в отношении грамположительной флоры.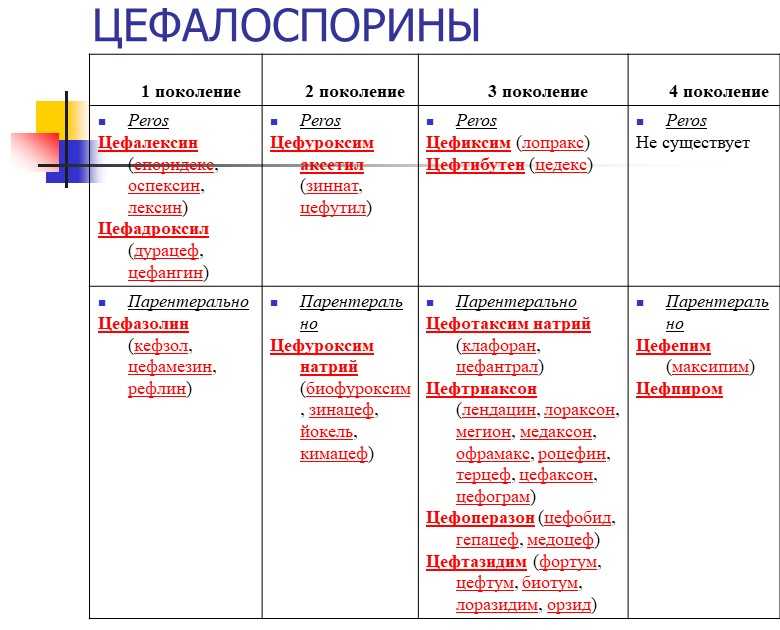 Активны в отношении некоторых нозокомиальных штаммов Enterobacteriaceae, резистентных к цефалоспоринам III поколения. Разрушаются β-лактамазами расширенного спектра, но устойчивы к действию β-лактамаз класса С. Применяют для лечения тяжелых нозокомиальных инфекций, в т.ч. в отделении интенсивной терапии и у пациентов с нейтропенией. Цефпиром уступает цефепиму по активности в отношении большинства возбудителей.
Активны в отношении некоторых нозокомиальных штаммов Enterobacteriaceae, резистентных к цефалоспоринам III поколения. Разрушаются β-лактамазами расширенного спектра, но устойчивы к действию β-лактамаз класса С. Применяют для лечения тяжелых нозокомиальных инфекций, в т.ч. в отделении интенсивной терапии и у пациентов с нейтропенией. Цефпиром уступает цефепиму по активности в отношении большинства возбудителей.
Цефалоспорины V поколения (анти-MRSA-цефемы) включают только препараты для парентерального введения — цефтаролин и цефтобипрол. Основной отличительной чертой цефалоспоринов V поколения является наиболее высокая среди β-лактамов in vitro активность в отношении грамположительных бактерий, включая большинство штаммов MRSA. Активность цефтаролина и цефтобипрола против грамотрицательных бактерий в целом эквивалентна таковой цефотаксима и цефтриаксона.
Наиболее частые побочные действия — аллергические реакции. Примерно у 10% больных с гиперчувствительностью к пенициллину возникают перекрестные аллергические реакции на цефалоспорины I поколения.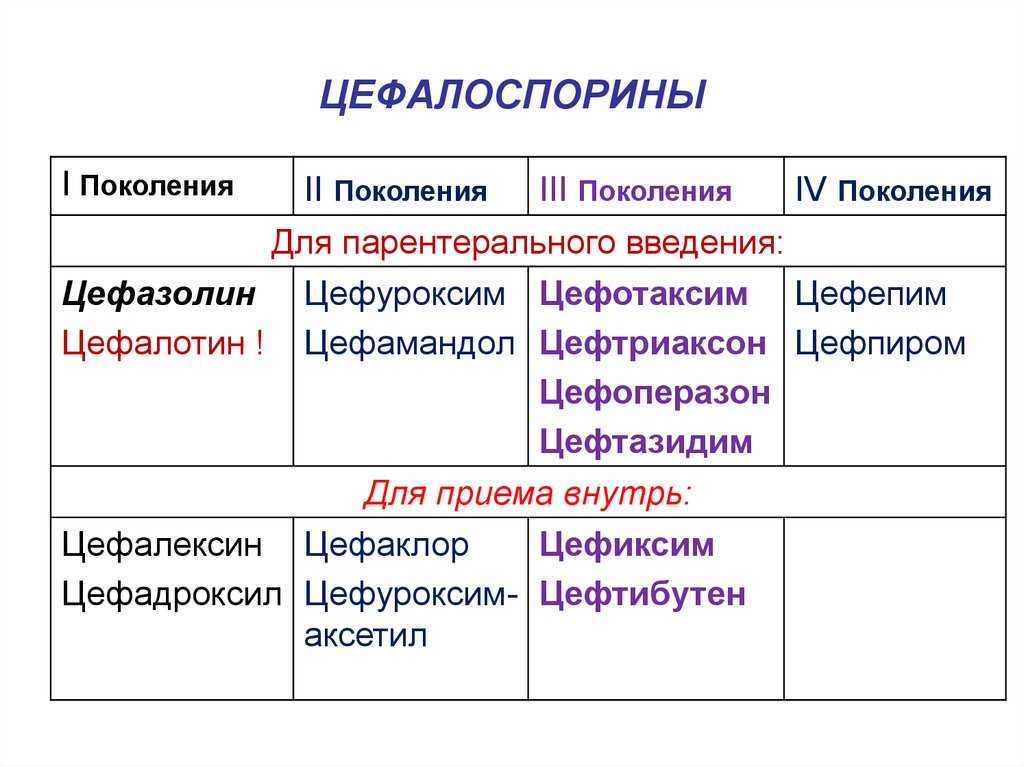 Цефоперазон может вызывать гипопротромбинемию и дисульфирамоподобный эффект.
Цефоперазон может вызывать гипопротромбинемию и дисульфирамоподобный эффект.
Оральные антибактериальные препараты при бронхолегочных заболеваниях у детей | Середа Е.В., Катосова Л.К.
Совершенствование терапевтической тактики при острых и хронических бронхолегочных заболеваниях является одной из важных и далеко не решенных проблем. Антибиотикотерапия – один из важнейших компонентов комплексного лечения заболеваний органов дыхания у детей. Выбор антибактериального препарата и пути его введения до сих пор представляют для врача сложную задачу. В настоящее время фармацевтическая промышленность располагает огромным арсеналом антибактериальных пероральных средств, которые находят широкое применение в педиатрической практике в связи с наличием детских лекарственных форм в виде суспензий, сиропов, таблеток с соответствующей дозировкой. В табл. 1 приведены антибиотики для орального применения. Оценивая классические пути введения антибиотиков, а именно, парентеральный и пероральный, в ряде случаев у детей следует отдать предпочтение последнему, как наиболее щадящему, исключающему прсихотравмирующий эффект.
Трудно переоценить значение создания новых пролонгированных форм антибиотиков, способствующих сокращению кратности их введения, которые обладают не только широким спектром действия, но и низкой токсичностью, что особенно важно для детей. Особого внимания заслуживает внедрение в практику “ступенчатого” метода лечения, сокращающего сроки парентерального введения антибиотиков до 1–3 дней.
Однако следует подчеркнуть, что оральная антибактериальная терапия, как стартовое лечение, наиболее показана при легких и среднетяжелых формах заболевания, в том числе при неосложненных острых пневмониях и обострениях хронических воспалительных бронхолегочных заболеваний.
Этиологическая структура заболеваний органов дыхания у детей имеет свои особенности в зависимости от формы, тяжести заболевания и возраста ребенка, что необходимо учитывать при решении вопроса о назначении антибиотиков. Наиболее частыми возбудителями внебольничной пневмонии, особенно осложненных ее форм, в первые месяцы жизни ребенка являются
 Значительно реже выделяются Streptococcus pneumoniae и Haemophilus influenzae (10–15%). В более старшем возрасте увеличивается роль Streptococcus pneumoniae (35–60% и более). Атипические возбудители пневмонии у детей в возрасте 1–6 месяцев выявляются более чем у 10–20%, чаще это Chlamidia trachomatis, реже Mycoplasma hominis [1–3]. Mycoplasma pneumoniae определяется у 10–15% больных в возрасте 1–6 лет. В школьном возрасте (7–15 лет) увеличивается частота атипичных пневмоний, особенно вызванных
Значительно реже выделяются Streptococcus pneumoniae и Haemophilus influenzae (10–15%). В более старшем возрасте увеличивается роль Streptococcus pneumoniae (35–60% и более). Атипические возбудители пневмонии у детей в возрасте 1–6 месяцев выявляются более чем у 10–20%, чаще это Chlamidia trachomatis, реже Mycoplasma hominis [1–3]. Mycoplasma pneumoniae определяется у 10–15% больных в возрасте 1–6 лет. В школьном возрасте (7–15 лет) увеличивается частота атипичных пневмоний, особенно вызванных 
Данные, накопленные специалистами разных стран, свидетельствуют о распространении и возрастающей роли устойчивых штаммов микроорганизмов (пневмококка, гемофильной палочки, и бранхамеллы катаралис) при различных инфекциях верхних и нижних дыхательных путей. Однако при выборе адекватной антибиотикотерапии следует ориентироваться на региональные данные о резистентности пневмотропных микроорганизмов, полученные в России. Мониторинг определения чувствительности основных пневмотропных бактерий, проведенный нами, позволил выявить, что
 Отмечается также высокая чувствительность Streptococcus pneumoniae к макролидам и цефалоспоринам, при их природной резистентности к аминогликозидам. Haemophilus influenzae также сохраняет высокую чувствительность к ампициллину, амоксициллину, амоксициллину/клавуланату, азитромицину, левомицетину, аминогликозидам и цефалоспоринам II–III поколений. Почти все штаммы
Отмечается также высокая чувствительность Streptococcus pneumoniae к макролидам и цефалоспоринам, при их природной резистентности к аминогликозидам. Haemophilus influenzae также сохраняет высокую чувствительность к ампициллину, амоксициллину, амоксициллину/клавуланату, азитромицину, левомицетину, аминогликозидам и цефалоспоринам II–III поколений. Почти все штаммы
Проведенное нами изучение чувствительности выделяемых бактерий при заболеваниях органов дыхания показывает, что препараты пенициллинового ряда остаются препаратами выбора при лечении пневмонии и ряда других инфекций у детей, вызванных грамположительными кокками (пневмококками, стафилококками, стрептококками).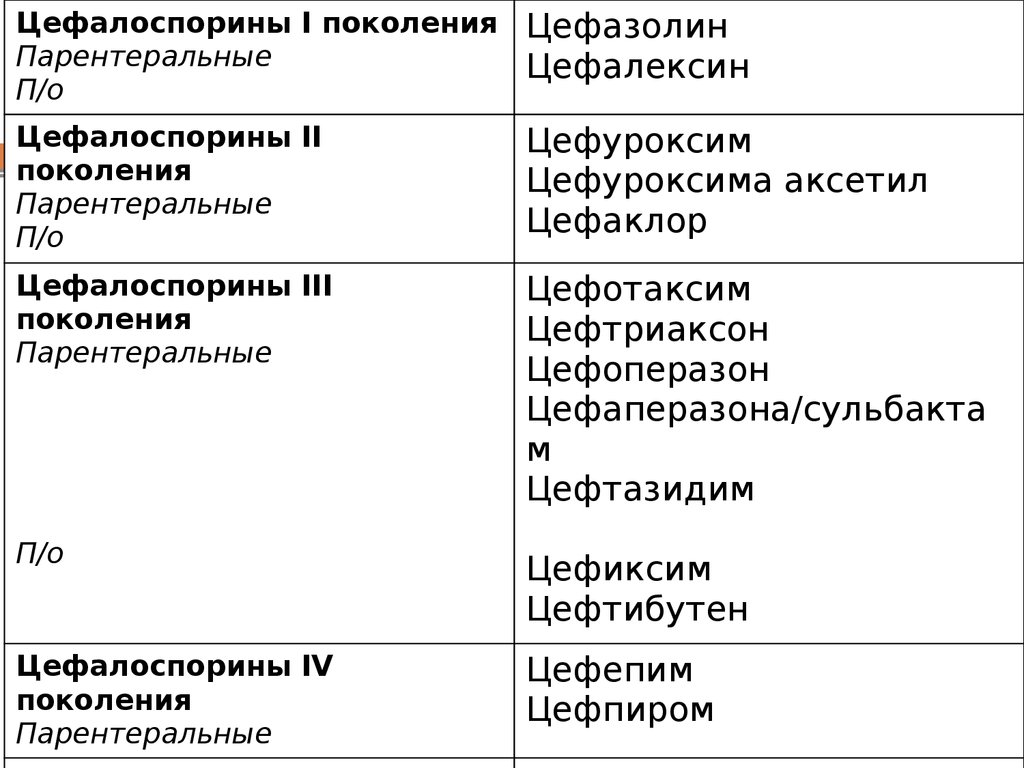 Среди остальных антибиотиков наиболее широкое применение при лечении заболеваний органов дыхания, в частности, при внебольничной пневмонии, получили аминопенициллины (ампициллин, амоксициллин и амоксициллин/клавуланат). При неосложненных внебольничных пневмониях легкой и средней тяжести, особенно в амбулаторных условиях, предпочтительно применение этих антибиотиков с учетом чувствительности Streptococcus pneumoniae, являющегося наиболее частым возбудителем внебольничных пневмоний [6].
Среди остальных антибиотиков наиболее широкое применение при лечении заболеваний органов дыхания, в частности, при внебольничной пневмонии, получили аминопенициллины (ампициллин, амоксициллин и амоксициллин/клавуланат). При неосложненных внебольничных пневмониях легкой и средней тяжести, особенно в амбулаторных условиях, предпочтительно применение этих антибиотиков с учетом чувствительности Streptococcus pneumoniae, являющегося наиболее частым возбудителем внебольничных пневмоний [6].
Комбинированный антибиотик пенициллиновой группы амоксициллин/клавуланат привлекает особое внимание педиатров, поскольку он решает проблему бета–лактамазной устойчивости основных патогенных организмов, являясь при этом антибиотиком широкого спектра действия. Он удобен для применения у детей, так как наряду с парентеральной формой имеются таблетки и сироп. Это позволяет применять его в качестве эмпирической терапии как при тяжелых инфекциях органов дыхания (в том числе с использованием “ступенчатого” метода), так и при легких — внутрь.
Внедрение в лечебную практику новых макролидов позволило расширить возможности применения пероральных антибактериальных препаратов, что способствует снижению потребности в парентеральных методах введения антибиотиков. Кроме того, макролиды считаются одной из самых безопасных групп антибиотиков и обладают высокой активностью к
16-членные макролиды (мидекамицин, джозамицин и др.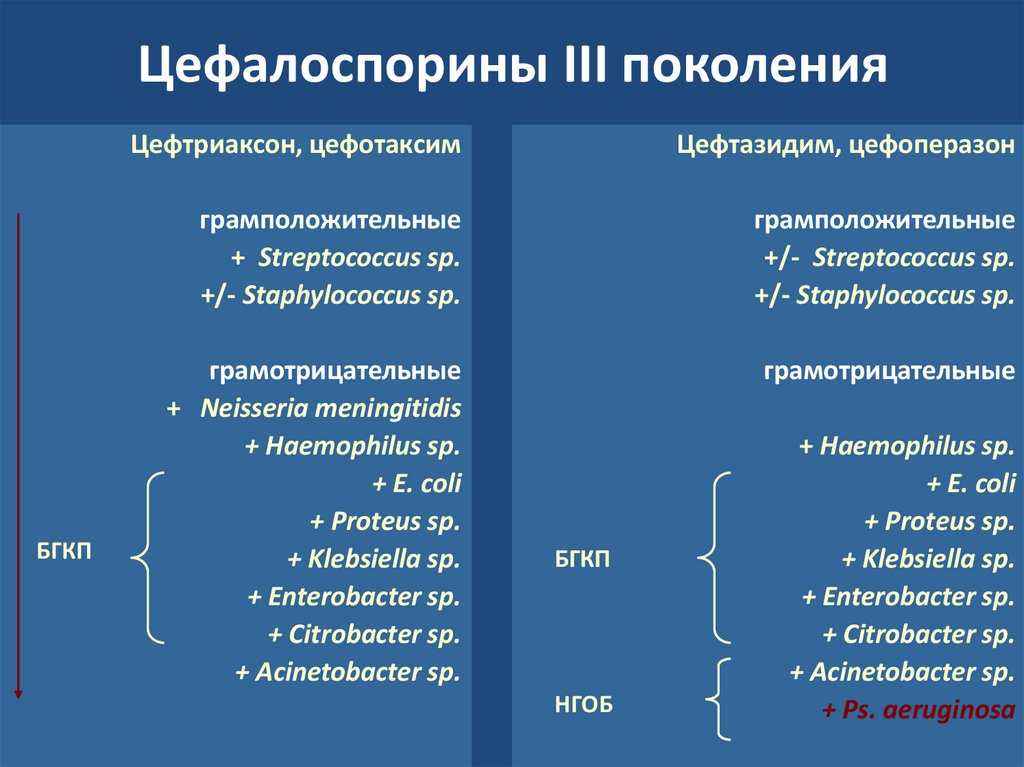 ), в отличие от 14- и 15-членных макролидов, не выводятся из бактериальной клетки ее мембранными насосами, дольше оказывая свое действие. Будучи 16-членным макролидом, мидекамицин не взаимодействует с другими лекарственными препаратами, в отличие от эритромицина и некоторых других макролидов, которые могут замедлять метаболизм теофиллина, антигистаминных (терфенадина, астемизола) и других препаратов, вызывая серьезные нежелательные эффекты.
), в отличие от 14- и 15-членных макролидов, не выводятся из бактериальной клетки ее мембранными насосами, дольше оказывая свое действие. Будучи 16-членным макролидом, мидекамицин не взаимодействует с другими лекарственными препаратами, в отличие от эритромицина и некоторых других макролидов, которые могут замедлять метаболизм теофиллина, антигистаминных (терфенадина, астемизола) и других препаратов, вызывая серьезные нежелательные эффекты.
Макролидные антибиотики являются препаратами выбора при атипичных пневмониях, вызванных внутриклеточными возбудителями (микоплазменной, хламидийной инфекциями), а также при внебольничной пневмонии, вызванной пневмококком и бранхамеллой катаралис, особенно у детей с аллергическими проявлениями и повышенной чувствительностью к пенициллинам [7-9].
Проведенное нами сравнительное изучение эффективности макролидов подтвердило их высокую эффективность при лечении детей раннего возраста с острой пневмонией и при обострениях хронической инфекции.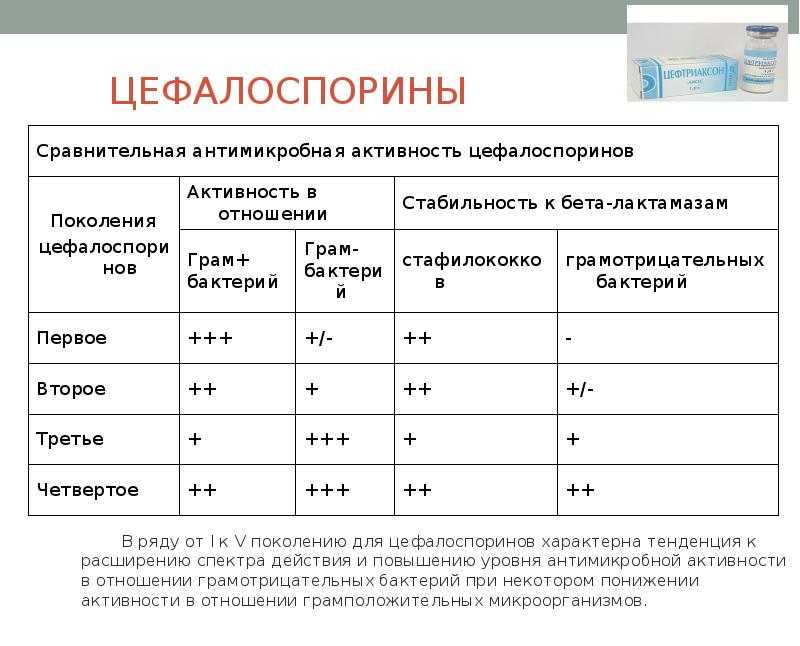 При этом полное рассасывание пневмонии происходило происходило в те же сроки, что и при парентеральном применении других антибиотиков [6]. При оральном применении эритромицина в случаях внебольничной острой пневмонии и обострении хронической пневмонии была получена клиническая эффективность 75% и 71%, соответственно. Но при этом у 16% и 19% больных наблюдались побочные реакции, потребовавшие отмены препарата. Высокая частота нежелательных реакций ограничивает применение эритромицина, особенно у детей раннего возраста. Более высокая эффективность была достигнута при применении новых макролидов: мидекамицин – 82%, рокситромицин – 90%, спирамицин – 89%, азитромицин – 93,4%. Наряду с этим отмечалась хорошая переносимость этих препаратов и редкость нежелательных реакций (3–5%). Подтверждаются данные литературы об эффективности и безопасности макролидных антибиотиков при лечении детей [7-9].
При этом полное рассасывание пневмонии происходило происходило в те же сроки, что и при парентеральном применении других антибиотиков [6]. При оральном применении эритромицина в случаях внебольничной острой пневмонии и обострении хронической пневмонии была получена клиническая эффективность 75% и 71%, соответственно. Но при этом у 16% и 19% больных наблюдались побочные реакции, потребовавшие отмены препарата. Высокая частота нежелательных реакций ограничивает применение эритромицина, особенно у детей раннего возраста. Более высокая эффективность была достигнута при применении новых макролидов: мидекамицин – 82%, рокситромицин – 90%, спирамицин – 89%, азитромицин – 93,4%. Наряду с этим отмечалась хорошая переносимость этих препаратов и редкость нежелательных реакций (3–5%). Подтверждаются данные литературы об эффективности и безопасности макролидных антибиотиков при лечении детей [7-9].
Цефалоспориновые препараты являются в настоящее время одними из наиболее активных антибиотиков широкого спектра действия, применяемых для лечения заболеваний органов дыхания у детей, однако при внебольничных пневмониях цефалоспорины могут применяться в случае неэффективности стартовых препаратов. Среди цефалоспоринов II и III поколений, доказавших свою высокую эффективность на практике, следует отметить пероральные антибиотики – цефуроксим, цефаклор и цефтибутен. Если при острой пневмонии или бронхите цефалоспорины I, II и III поколений рассматриваются, как препараты резерва, то при хронической бронхолегочной патологии, особенно связанной с пороками развития легких и бронхов, а также у детей с иммунодефицитными состояниями цефалоспорины II и III поколений являются одними из основных антибиотиков с учетом их широкого спектра действия, устойчивости к бета–лактамазам, высокой эффективности и хорошей переносимости [10].
Среди цефалоспоринов II и III поколений, доказавших свою высокую эффективность на практике, следует отметить пероральные антибиотики – цефуроксим, цефаклор и цефтибутен. Если при острой пневмонии или бронхите цефалоспорины I, II и III поколений рассматриваются, как препараты резерва, то при хронической бронхолегочной патологии, особенно связанной с пороками развития легких и бронхов, а также у детей с иммунодефицитными состояниями цефалоспорины II и III поколений являются одними из основных антибиотиков с учетом их широкого спектра действия, устойчивости к бета–лактамазам, высокой эффективности и хорошей переносимости [10].
При тяжелых формах заболевания пероральные препараты могут использоваться также для продолжения лечения при необходимости стартового парентерального назначения антибиотиков широкого спектра действия, их смены, комбинирования препаратов и методов введения, в том числе при “ступенчатом” методе лечения.
Следует подчеркнуть тот факт, что детям с острыми рецидивирующими и особенно с хроническими бронхолегочными заболеваниями нередко приходится назначать повторные курсы антибактериальных препаратов. В связи с этим возникает ряд сложностей, связанных не только с развитием устойчивости возбудителей воспалительного процесса в бронхах и легких, но и продиктованных необходимостью обеспечить наиболее обоснованное, щадящее лечение. Наиболее адекватное лечение проводится с учетом антибиотикограммы. При невозможности получения этих данных и в экстренных случаях рекомендуется использование антибиотиков широкого спектра действия.
В связи с этим возникает ряд сложностей, связанных не только с развитием устойчивости возбудителей воспалительного процесса в бронхах и легких, но и продиктованных необходимостью обеспечить наиболее обоснованное, щадящее лечение. Наиболее адекватное лечение проводится с учетом антибиотикограммы. При невозможности получения этих данных и в экстренных случаях рекомендуется использование антибиотиков широкого спектра действия.
В заключение следует отметить, что имеются большие резервы для повышения эффективности лечения детей с бронхолегочными заболеваниями. Создание и внедрение в педиатрическую практику эффективных пероральных антимикробных препаратов широкого спектра действия, в том числе детских лекарственных форм для приема внутрь, будет способствовать совершенствованию терапевтической тактики при заболеваниях органов дыхания у детей не только в стационарах, но и в амбулаторно – поликлинических условиях.
1. Таточенко В.К., Середа Е.В., Федоров А.М., Катосова Л.К., Самсыгина Г.А., Дементьева Г.М., Страчунский Л.С. Антибактериальная терапия пневмоний у детей. Антибиотики и химиотерапия, 2000; 5: 33–40.
Таточенко В.К., Середа Е.В., Федоров А.М., Катосова Л.К., Самсыгина Г.А., Дементьева Г.М., Страчунский Л.С. Антибактериальная терапия пневмоний у детей. Антибиотики и химиотерапия, 2000; 5: 33–40.
2. Таточенко В.К. Антибактериальная терапия внебольничной пневмонии у детей. Материалы Международной конференции “Антибактериальная терапия в педиатрической практике.” Москва, 1999: 45–9.
3. Вербицки С. Антибактериальная терапия внебольничной пневмонии у детей. Материалы Международной конференции “Антибактериальная терапия в педиатрической практике.” Москва, 1999: 42–4.
4. Середа Е.В., Катосова Л.К. Современные подходы к применению макролидов при заболеваниях органов дыхания у детей. Русский медицинский журнал, 2000; 1: 34–9.
5. Кречикова О.И. Состояние антибиотикорезистентности Streptococcus pneumoniae в России. Русский медицинский журнал Пульмонология VIII Российский национальный конгресс “Человек и лекарство” 2001: 8–10.
6. Таточенко В. К., Федоров А.М., Хайрулин Б.Е. Об использовании оральных антибактериальных средств в лечении острой пневмонии у детей. Педиатрия, 1992; 4–6: 38–41.
К., Федоров А.М., Хайрулин Б.Е. Об использовании оральных антибактериальных средств в лечении острой пневмонии у детей. Педиатрия, 1992; 4–6: 38–41.
7. Страчунский Л.С., Козлов С.Н. Макролиды в современной клинической практике. Русич, Смоленск, 1998: 302с.
8. Йерман А., Дриновец Й. Клинические аспекты применения макролидных антибиотиков. KrKa Med Farm 1996; 16(28): 26–32.
9. Кишимото К. Место макролидов в педиатрической практике. Материалы Международной конференции “Антибактериальная терапия в педиатрической практике.” Москва, 1999: 52–5.
10. Середа Е.В., Рачинский С.В., Волков И.К., Катосова Л.К., Лукина О.Ф. Лечение пороков развития легких и бронхов у детей. Русский медицинский журнал, 1999; 11: 510– 4.
Мидекамицин –
Макропен (торговое название)
(KRKA)
(торговое название)Цефалоспориновые антибиотики (в/в или в/м)
| Общее название | Торговая марка |
| ___ цефуроксим | Цефтин® |
| ___ цефотетан | Цефотан® |
| ___ цефокситин | Мефоксин® |
| ___ цефотаксим | Клафоран® |
| ___ цефтриаксон | Роцефин® |
| ___ цефтазидим | Фортаз® Тазицеф® Тазидим® |
Как действует это лекарство?
Цефалоспорины ( seh -fah-low- spor -ins) — это антибиотики, используемые для лечения широкого спектра бактериальных инфекций, таких как инфекции кожи, дыхательных путей и мочевыводящих путей.
Антибиотики работают лучше всего, когда их количество поддерживается на постоянном уровне в организме, поэтому лекарство принимается по установленному графику каждый день.
Как дается?
Эти лекарства вводят внутривенно (в/в) в больнице или клинике.
Цефтриаксон (sef-try- ax -self) также можно вводить в виде укола в мышцу (IM) в клинике. Если его вводят внутримышечно, к нему смешивают лекарство под названием лидокаин ( ly -doe-cane), чтобы уменьшить боль от инъекции.
Примечание: Были ли у вашего ребенка когда-либо аллергические реакции немедленного типа на пенициллин или какой-либо цефалоспорин, такие как перечисленные выше? Если так, пожалуйста, дайте нам знать. Ваш ребенок будет находиться под наблюдением в течение 20-30 минут после приема лекарства на наличие признаков аллергической реакции.
Если вашему ребенку требуется больше доз, вас могут попросить приходить в клинику каждый день или вас могут научить, как давать лекарство ребенку дома. Инструкции см. в других письменных материалах, предоставленных вам.
Инструкции см. в других письменных материалах, предоставленных вам.
Используйте это лекарство точно так, как это предписано, даже если ваш ребенок чувствует себя лучше, чтобы быть уверенным, что вся инфекция исчезла.
Может потребоваться дополнительный контроль дозы или состояния вашего ребенка, если он или она также принимает варфарин (Coumadin®).
Проконсультируйтесь с врачом или фармацевтом, прежде чем давать любые другие лекарства, отпускаемые по рецепту или без рецепта, витамины или травы.
Избегайте употребления спиртосодержащих продуктов, напитков или безрецептурных лекарств (таких как сироп от кашля) во время приема этого лекарства.
Что делать, если пропущена доза?
Если пропущена одна доза, дайте ее, как только вспомните. Никогда не давайте двойную дозу. Если ваш ребенок пропустил 2 дозы, позвоните в клинику или медсестре по уходу на дому за инструкциями.
Каковы побочные эффекты?
Обычный
- раздражение вен
- болезненность или покраснение в месте инъекции
Иногда
- тошнота (расстройство желудка)
- рвота (рвота)
- диарея
- сыпь
- газ
Редко
- снижение показателей крови
- головная боль
- изменения функции печени или почек
Когда следует вызвать врача?
- тошнота или рвота
- сильные желудочные спазмы
- водянистая или кровавая диарея
- необычная слабость
- необычные синяки или кровотечения
- желтизна кожи или глаз
- признаки инфекции не улучшаются в течение нескольких дней или ухудшаются
- признаки аллергической реакции:
- сыпь или крапивница
- свистящее дыхание
- проблемы с дыханием — звоните 911
Что еще мне нужно знать?
Перед применением этого лекарства сообщите своему лечащему врачу обо всех возможных аллергиях, которые могут быть у вашего ребенка.
Образцы крови могут потребоваться для проверки функции печени или почек, если ваш ребенок будет получать цефалоспорины более 10–14 дней.
Вы и ваш ребенок должны знать названия всех лекарств, которые он принимает. Важно поделиться этой информацией со всеми, кто занимается уходом за вашим ребенком. Пожалуйста, не забудьте взять с собой список лекарств вашего ребенка или контейнеры, когда ваш ребенок приходит в клинику или отделение неотложной помощи.
Обеспечьте безопасное хранение и утилизацию игл, трубок и расходных материалов. Используйте контейнер для острых предметов для игл, например:
- 2-литровая пластиковая бутылка с крышкой
- банка для кофе с крышкой
- пластиковая бутылка для моющего средства с крышкой
- специальный контейнер для этой цели
Храните это лекарство в холодильнике, если вам не даны другие инструкции.
___ другие инструкции по хранению:
Проверяйте срок годности и время перед использованием каждой дозы. Выбрасывайте просроченные лекарства в контейнер для острых предметов вместе с иглами, а не выбрасывайте их в мусор.
Выбрасывайте просроченные лекарства в контейнер для острых предметов вместе с иглами, а не выбрасывайте их в мусор.
Если вы приняли слишком много или не того лекарства, позвоните в токсикологический центр по телефону 1-800-222-1222.
Другие инструкции:
Есть вопросы?
Если у вас есть какие-либо вопросы, позвоните в клинику или: ________________________________________
Children’s Hospitals and Clinics of Minnesota
Patient/Family Education
2525 Chicago Avenue South
Minneapolis, MN 55404
Последнее рассмотрение 8/2015 ©Copyright
Вернуться к началу
Применение цефалоспоринов третьего поколения для лечения неонатальных инфекций | JAMA Pediatrics
Использование цефалоспоринов третьего поколения для лечения неонатальных инфекций | ДЖАМА Педиатрия | Сеть ДЖАМА [Перейти к навигации]Эта проблема
- Скачать PDF
- Полный текст
Поделиться
Твиттер Фейсбук Эл.
 адрес
LinkedIn
адрес
LinkedIn- Процитировать это
- Разрешения
Артикул
ноябрь 1985 г.
ДЖОРДЖ Х. МАККРАКЕН МЛАДШИЙ, MD
Принадлежности автора
Факультет педиатрии Техасского университета Медицинский научный центр в Далласе 5323 Harry Hines Blvd Dallas, TX 75235
Am J Dis Чайлд. 1985;139(11):1079-1080. doi:10.1001/archpedi.1985.02140130017019
Полный текст
Абстрактный
Появление новых цефалоспоринов третьего поколения (цефотаксим, цефтизоксим, цефоперазон, цефтриаксон, цефтазидим и моксалактам) вызвало интерес у врачей, ухаживающих за новорожденными. Эти новые соединения чрезвычайно активны в отношении кишечных грамотрицательных бактерий и следующих важных патогенов: Haemophilus influenzae, Streptococcus agalactiae (стрептококки группы B), Neisseria meningitidis и Streptococcus pneumoniae .
